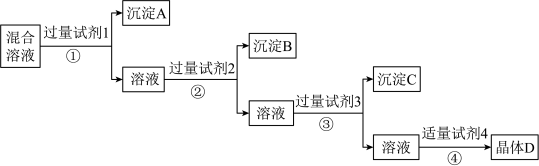
常见气体的发生装置
辨认下列常见的气体发生装置,完成下列问题:
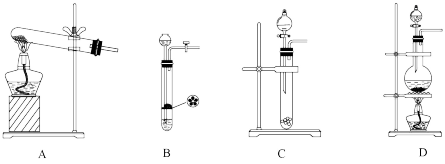
(1)①用氯化铵与消石灰制取氨气,化学方程式:_______ ,选用装置:_______ (填字母,下同)。
②用浓氨水与碱石灰制取氨气,选用装置:_______ 。
(2)①用碳酸钠与稀硫酸制取二氧化碳,选用装置:_______ 。
②用石灰石与稀盐酸制取二氧化碳,选用装置:_______ 。
(3)①用浓盐酸与二氧化锰制取氯气,化学方程式:_______ ,选用装置:_______ 。
②用漂白粉与浓盐酸制取少量氯气,化学方程式:_______ ,选用装置:_______ 。
(4)铜与浓硝酸反应制取二氧化氮,选用装置:_______ 。
(5)实验室制取乙烯的装置,可以通过选用上面哪个装置进行改进_______ ?若橡皮塞最多只允许打两个孔,应如何改进所选实验装置:_______ 。
(6)上述B装置还能制取的气体有:_______ 。
辨认下列常见的气体发生装置,完成下列问题:

(1)①用氯化铵与消石灰制取氨气,化学方程式:
②用浓氨水与碱石灰制取氨气,选用装置:
(2)①用碳酸钠与稀硫酸制取二氧化碳,选用装置:
②用石灰石与稀盐酸制取二氧化碳,选用装置:
(3)①用浓盐酸与二氧化锰制取氯气,化学方程式:
②用漂白粉与浓盐酸制取少量氯气,化学方程式:
(4)铜与浓硝酸反应制取二氧化氮,选用装置:
(5)实验室制取乙烯的装置,可以通过选用上面哪个装置进行改进
(6)上述B装置还能制取的气体有:
2023高三·全国·专题练习 查看更多[1]
(已下线)第十章 化学综合实验 第63讲 物质制备综合实验探究
更新时间:2023-02-12 14:02:13
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】下图为实验室制取氨气,二氧化硫及有关性质实验的组合装置。

(1)如果A、E是气体制取装置,则按照题目要求,A中制取气体的化学反应方程式为_______ ;
(2)B仪器称为_______ ,在此实验中B应加入_______ (写名称);
(3)先加热A装置,使产生气体通入烧瓶F中,此时弹簧夹a、b打开、c关闭。当F中充满A中气体后,A停止制气,关闭a,打开弹簧夹c,使E中气体通入F中;
①如何测知F中已充满大量A中气体:_______ ;
②D的作用是干燥气体,D中盛的是_______ (写名称);
(4)A、E中产生的气体都是有污染性的,吸收A尾气的试剂是_______ ,吸收E尾气的离子方程式为_______ 。
(5)生石灰与水反应生成 并放出热量。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
并放出热量。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是_______ (填“a”“b”或“c”)。


(1)如果A、E是气体制取装置,则按照题目要求,A中制取气体的化学反应方程式为
(2)B仪器称为
(3)先加热A装置,使产生气体通入烧瓶F中,此时弹簧夹a、b打开、c关闭。当F中充满A中气体后,A停止制气,关闭a,打开弹簧夹c,使E中气体通入F中;
①如何测知F中已充满大量A中气体:
②D的作用是干燥气体,D中盛的是
(4)A、E中产生的气体都是有污染性的,吸收A尾气的试剂是
(5)生石灰与水反应生成
 并放出热量。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
并放出热量。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
您最近一年使用:0次
【推荐2】氨在人类的生产和生活中有着广泛的应用。某化学兴趣小组探究制备氨气的方法并利用图1装置探究氨气的有关性质。

(1)图1中盛装浓氨水的仪器名称:___________ ,装置A中烧瓶内试剂可选用___________ (填序号),反应方程式为:___________ 。
A.生石灰 B.烧碱溶液 C.碱石灰 D.浓硫酸
(2)若实验室利用图2装置制备 ,试管中所加的试剂为(填名称):
,试管中所加的试剂为(填名称):___________ 。
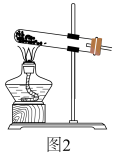
(3)实验中观察到C中 粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为
粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为___________ 。该反应证明氨气具有___________ 性(填“氧化”或“还原”)。
(4)图1的实验装置图存在的明显不足是___________ 。
(5)氨气极易溶于水,若标准状况下,将 的氨气溶于水配成
的氨气溶于水配成 溶液,所得溶液的物质的量浓度为
溶液,所得溶液的物质的量浓度为___________  。
。
(6)向浓 溶液中通入
溶液中通入 气体没现象,但若先通入
气体没现象,但若先通入 ,再通入
,再通入 则可制备纳米级碳酸钙。试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:
则可制备纳米级碳酸钙。试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:___________ 。

(1)图1中盛装浓氨水的仪器名称:
A.生石灰 B.烧碱溶液 C.碱石灰 D.浓硫酸
(2)若实验室利用图2装置制备
 ,试管中所加的试剂为(填名称):
,试管中所加的试剂为(填名称):
(3)实验中观察到C中
 粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为
粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为(4)图1的实验装置图存在的明显不足是
(5)氨气极易溶于水,若标准状况下,将
 的氨气溶于水配成
的氨气溶于水配成 溶液,所得溶液的物质的量浓度为
溶液,所得溶液的物质的量浓度为 。
。(6)向浓
 溶液中通入
溶液中通入 气体没现象,但若先通入
气体没现象,但若先通入 ,再通入
,再通入 则可制备纳米级碳酸钙。试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:
则可制备纳米级碳酸钙。试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出N2的电子式:___ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是___ (填字母)。
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
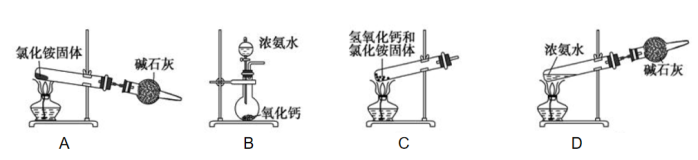
(3)如图是实验室制取氨气的装置和选用的试剂,其中错误的是___ (填字母)。
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放氨气而降低肥效。检验 的方法是
的方法是___ 。
(1)写出N2的电子式:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
(3)如图是实验室制取氨气的装置和选用的试剂,其中错误的是

(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放氨气而降低肥效。检验
 的方法是
的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室用乙醇制备1,2-二溴乙烷的反应原理如下:①乙醇在浓硫酸的存在下制取乙烯、②乙烯与溴反应制得1,2-二溴乙烷。可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:

回答下列问题:
(1)写出乙醇在浓硫酸的存在下制取乙烯的化学方程式______________ ;浓硫酸所起的作用是___________ 。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_______ ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)反应一段时间后三颈烧瓶A中的液体混合物会逐渐变黑,此时会发生另一个副反应生成其他酸性杂质气体,该反应的化学方程式为_________ 。
(4)在装置C中应加入______ ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)判断该制备反应已经结束的最简单方法是________________ ;
(6)若产物中有少量副产物乙醚,可用_____________ 的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是________________ ;但又不能过度冷却(如用冰水),其原因是___________________ 。

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm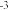 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)写出乙醇在浓硫酸的存在下制取乙烯的化学方程式
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)反应一段时间后三颈烧瓶A中的液体混合物会逐渐变黑,此时会发生另一个副反应生成其他酸性杂质气体,该反应的化学方程式为
(4)在装置C中应加入
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)判断该制备反应已经结束的最简单方法是
(6)若产物中有少量副产物乙醚,可用
(7)反应过程中应用冷水冷却装置D,其主要目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】1,2—二氯乙烷(CH2ClCH2Cl)外观为无色或浅黄色透明液体,难溶于水,易溶于有机溶剂,碱性条件下水解程度较大,主要用作氯乙烯(聚氯乙烯单体)制取过程的中间体。实验室制备1,2—二氯乙烷的主要原理:C2H5OH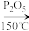 CH2=CH2+H2O;Cl2+CH2=CH2→CH2ClCH2Cl。
CH2=CH2+H2O;Cl2+CH2=CH2→CH2ClCH2Cl。

(1)写出装置A中发生反应的离子方程式___ 。
(2)B装置中的作用是___ 。
(3)根据制备原理,G装置中应该添加的仪器是___ 。
(4)D装置中多孔球泡的作用是___ 。
(5)A装置橡皮管的作用___ 。
(6)D装置排出尾气可以通过盛有__ 、NaOH溶液的洗气瓶进行吸收。
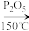 CH2=CH2+H2O;Cl2+CH2=CH2→CH2ClCH2Cl。
CH2=CH2+H2O;Cl2+CH2=CH2→CH2ClCH2Cl。
(1)写出装置A中发生反应的离子方程式
(2)B装置中的作用是
(3)根据制备原理,G装置中应该添加的仪器是
(4)D装置中多孔球泡的作用是
(5)A装置橡皮管的作用
(6)D装置排出尾气可以通过盛有
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
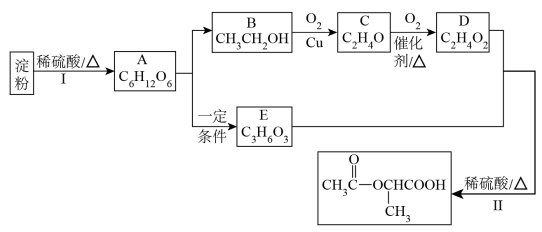
【推荐1】有机化合物F是一种食用香料,可用淀粉为原料,路线如图:
(1)A为 ,所含官能团的结构简式为
,所含官能团的结构简式为___________ 、 。
。
(2)反应Ⅱ为酯化反应,写出反应Ⅱ的化学方程式___________ 。
(3)3.45gB与足量钠反应,能生成标准状况下 的体积为
的体积为___________ L。
(4)下列说法不正确的是___________ (填字母)。
a.淀粉分子式为 ,属于天然有机高分子
,属于天然有机高分子
b.反应Ⅰ为水解反应
c.E分别于足量的Na和NaOH反应,消耗的Na和NaOH的物质的量相等
d.D、E互为同系物
(5)淀粉在酸性条件下发生水解反应生成A,要证明淀粉已经水解完全向水解后的溶液中加入___________ (填试剂名称)。
(1)A为
 ,所含官能团的结构简式为
,所含官能团的结构简式为 。
。(2)反应Ⅱ为酯化反应,写出反应Ⅱ的化学方程式
(3)3.45gB与足量钠反应,能生成标准状况下
 的体积为
的体积为(4)下列说法不正确的是
a.淀粉分子式为
 ,属于天然有机高分子
,属于天然有机高分子b.反应Ⅰ为水解反应
c.E分别于足量的Na和NaOH反应,消耗的Na和NaOH的物质的量相等
d.D、E互为同系物
(5)淀粉在酸性条件下发生水解反应生成A,要证明淀粉已经水解完全向水解后的溶液中加入
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】Bi2O3常用作可见光催化剂,NaBiO3是一种强氧化剂。以辉铋矿(主要成分是Bi2S3,含少量的Bi2O3、SiO2和铁的氧化物)为原料制备Bi2O3和NaBiO3的流程如下:
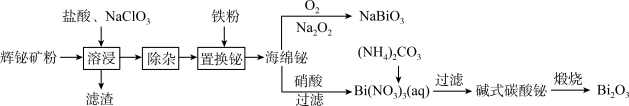
已知:①Bi2O3能溶于酸;②碱式碳酸铋的化学组成:(BiO)2CO3;③Bi2S3+6HCl+NaClO3=2BiCl3+3S+NaCl+3H2O。
Ⅰ.请回答下列问题:
(1)滤渣的成分有_______ (填化学式,下同);“溶浸”时可能产生一种有毒气体单质,它是_______ 。
(2)“溶浸”时浸出速率与温度的关系如图所示。
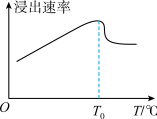
温度高于T0℃时,浸出速率突然减小的原因是_______ 。
(3)若将“置换铋”的反应设计成原电池,则负极反应式为_______ 。
(4)写出“煅烧”中反应的化学方程式:_______ 。
(5)实验室常用下列方法鉴别Mn2+:在硫酸酸化的MnSO4溶液中加入NaBiO3粉末(难溶于水),溶液变成紫红色,还原产物为Bi3+,该反应的离子方程式为_______ 。
Ⅱ.石油是重要的化工原料,被称为“工业的血液”。下图中A的产量被用作衡量一个国家石油化工产业发展水平的标志。回答下列问题:

(6)过程②这种获得有机化工原料的方法在工业上叫做_______ ,物质D中含有的官能团名称为_______ ,过程③发生的反应类型是_______ 。
(7)石油气的成分中含有一种电子总数为42的烷烃,该烷烃共有_______ 种同分异构体,其中一氯代物共有4种的名称是_______ 。
(8)以淀粉为原料经水解生成葡萄糖,葡萄糖在酒化酶的作用下可分解生成B,写出生成B的化学方程式_______ 。实验室实现过程④反应的化学方程式为_______ 。
(9)实验室常用下列装置实现过程⑥发生的化学反应。

①实验时,先在大试管中加入B、浓硫酸、D的混合物,再加入_______ 。
②反应结束后,将收集到的产品倒入分液漏斗中振荡、静置、分液,_______ 从分液漏斗上口倒出。
③相对于a装置,用b装置进行制备的缺点有_______ (答一条即可)。

已知:①Bi2O3能溶于酸;②碱式碳酸铋的化学组成:(BiO)2CO3;③Bi2S3+6HCl+NaClO3=2BiCl3+3S+NaCl+3H2O。
Ⅰ.请回答下列问题:
(1)滤渣的成分有
(2)“溶浸”时浸出速率与温度的关系如图所示。

温度高于T0℃时,浸出速率突然减小的原因是
(3)若将“置换铋”的反应设计成原电池,则负极反应式为
(4)写出“煅烧”中反应的化学方程式:
(5)实验室常用下列方法鉴别Mn2+:在硫酸酸化的MnSO4溶液中加入NaBiO3粉末(难溶于水),溶液变成紫红色,还原产物为Bi3+,该反应的离子方程式为
Ⅱ.石油是重要的化工原料,被称为“工业的血液”。下图中A的产量被用作衡量一个国家石油化工产业发展水平的标志。回答下列问题:

(6)过程②这种获得有机化工原料的方法在工业上叫做
(7)石油气的成分中含有一种电子总数为42的烷烃,该烷烃共有
(8)以淀粉为原料经水解生成葡萄糖,葡萄糖在酒化酶的作用下可分解生成B,写出生成B的化学方程式
(9)实验室常用下列装置实现过程⑥发生的化学反应。

①实验时,先在大试管中加入B、浓硫酸、D的混合物,再加入
②反应结束后,将收集到的产品倒入分液漏斗中振荡、静置、分液,
③相对于a装置,用b装置进行制备的缺点有
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示.
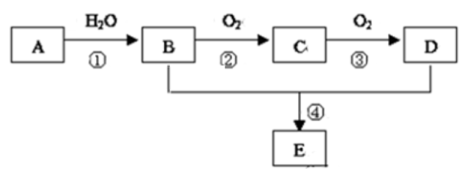
请回答下列问题:
(1)写出A的电子式______________ ;
(2)D、E分子中官能团的名称是_______ 、 _________ ;
(3)写出下列反应的化学方程式:
②_______________________________________ ,反应类型:____________ 。
④_______________________________________ ,反应类型_____________ 。

请回答下列问题:
(1)写出A的电子式
(2)D、E分子中官能团的名称是
(3)写出下列反应的化学方程式:
②
④
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】锗和硅同一主族,也是重要的半导体材料,应用于航空航天测控、光纤通讯等领域。一种以铅锌矿含锗烟尘(主要含GeO2、ZnO 、SiO2)为原料制备GeO2的工艺如下:

已知:①GeO2为两性氧化物;
②H4SiO4和H2GeO3在高酸度时易聚合形成多聚硅酸和多聚锗酸;
③GeCl4易水解。
试回答下列问题:
(1)锗的原子序数为32 ,在元素周期表中的位置为___________ 。
(2)第①步为提高稀硫酸的浸出效果可以采取的措施有___________ (任写一条)。
(3)第①步所得滤液中锗以Ge4+存在,写出其水解的离子方程式___________ 。
(4)测得锗的浸出率(%)与硫酸的物质的量浓度(mol/L)的关系如图所示:

浸出率高时的硫酸浓度为___________ mol/L,的原因是___________ 。
(5)工业上与蒸馏操作相关的设备有___________(填选项)。
(6)第⑤步发生的化学反应方程式为___________ 。

已知:①GeO2为两性氧化物;
②H4SiO4和H2GeO3在高酸度时易聚合形成多聚硅酸和多聚锗酸;
③GeCl4易水解。
试回答下列问题:
(1)锗的原子序数为32 ,在元素周期表中的位置为
(2)第①步为提高稀硫酸的浸出效果可以采取的措施有
(3)第①步所得滤液中锗以Ge4+存在,写出其水解的离子方程式
(4)测得锗的浸出率(%)与硫酸的物质的量浓度(mol/L)的关系如图所示:

浸出率高时的硫酸浓度为
(5)工业上与蒸馏操作相关的设备有___________(填选项)。
| A.蒸馏釜 | B.离心萃取机 | C.冷凝塔 | D.加压过滤机 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】层状结构 薄膜能用于制作电极材料。
薄膜能用于制作电极材料。 薄膜由辉钼矿(主要含
薄膜由辉钼矿(主要含 及少量FeO、
及少量FeO、 )制得
)制得 后再与S经气相反应并沉积得到,其流程如下。
后再与S经气相反应并沉积得到,其流程如下。
(1)“焙烧”产生的 用
用 溶液吸收生成
溶液吸收生成 的离子方程式为
的离子方程式为___________ 。
(2)“焙烧”后的固体用氨水“浸取”得到重钼酸铵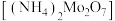 溶液,为提高“浸取”速率,可采用的措施是
溶液,为提高“浸取”速率,可采用的措施是___________ (举一例)。
(3)“灼烧”过程中需回收利用的气体是___________ (填化学式)。
(4)在650℃下“气相沉积”生成 的反应需在特定气流中进行,选用Ar而不选用
的反应需在特定气流中进行,选用Ar而不选用 形成该气流的原因是
形成该气流的原因是___________ 。
(5)层状 晶体与石墨晶体结构类似,层状
晶体与石墨晶体结构类似,层状 的晶体类型为
的晶体类型为___________ 。将 嵌入层状
嵌入层状 充电后得到的
充电后得到的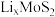 可作电池负极,该负极放电时的电极反应式为
可作电池负极,该负极放电时的电极反应式为___________ 。结合原子结构分析, 能嵌入
能嵌入 层间可能的原因是
层间可能的原因是___________ 。
 薄膜能用于制作电极材料。
薄膜能用于制作电极材料。 薄膜由辉钼矿(主要含
薄膜由辉钼矿(主要含 及少量FeO、
及少量FeO、 )制得
)制得 后再与S经气相反应并沉积得到,其流程如下。
后再与S经气相反应并沉积得到,其流程如下。
(1)“焙烧”产生的
 用
用 溶液吸收生成
溶液吸收生成 的离子方程式为
的离子方程式为(2)“焙烧”后的固体用氨水“浸取”得到重钼酸铵
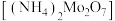 溶液,为提高“浸取”速率,可采用的措施是
溶液,为提高“浸取”速率,可采用的措施是(3)“灼烧”过程中需回收利用的气体是
(4)在650℃下“气相沉积”生成
 的反应需在特定气流中进行,选用Ar而不选用
的反应需在特定气流中进行,选用Ar而不选用 形成该气流的原因是
形成该气流的原因是(5)层状
 晶体与石墨晶体结构类似,层状
晶体与石墨晶体结构类似,层状 的晶体类型为
的晶体类型为 嵌入层状
嵌入层状 充电后得到的
充电后得到的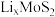 可作电池负极,该负极放电时的电极反应式为
可作电池负极,该负极放电时的电极反应式为 能嵌入
能嵌入 层间可能的原因是
层间可能的原因是
您最近一年使用:0次