氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。
已知:①乙醇水蒸气重整制氢的部分反应过程如图1所示。
②反应I和反应II的平衡常数(K)随温度(T)的变化曲线如图2所示。
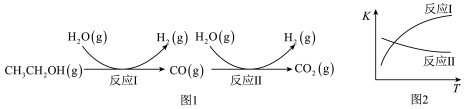
(1)反应I中,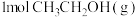 参与反应后的热量变化是256 kJ,则该反应的热化学方程式为
参与反应后的热量变化是256 kJ,则该反应的热化学方程式为_______ 。
(2)一定温度下,在一恒容密闭容器中发生反应I,下列叙述能说明此反应达到化学平衡状态的是_______(填选项字母)。
(3)在一恒容密闭容器中按不同进料比通入 与
与 发生反应II,在不同温度时测得CO的平衡转化率如图3所示。
发生反应II,在不同温度时测得CO的平衡转化率如图3所示。
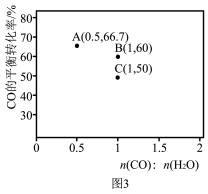
①B、C两点对应的反应温度分别为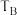 和
和 ,则
,则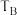
_______  (填“<”“=”或“>”)。
(填“<”“=”或“>”)。
②A点对应温度下,反应II的化学平衡常数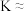
_______ 。
③若向A点对应的平衡体系中再充入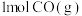 、
、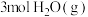 、
、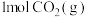 和
和 ,此时平衡向
,此时平衡向_______ (填“正反应”或“逆反应”)方向移动。
④实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以增大 的体积分数,其原因为
的体积分数,其原因为_______ 。
已知:①乙醇水蒸气重整制氢的部分反应过程如图1所示。
②反应I和反应II的平衡常数(K)随温度(T)的变化曲线如图2所示。

(1)反应I中,
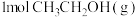 参与反应后的热量变化是256 kJ,则该反应的热化学方程式为
参与反应后的热量变化是256 kJ,则该反应的热化学方程式为(2)一定温度下,在一恒容密闭容器中发生反应I,下列叙述能说明此反应达到化学平衡状态的是_______(填选项字母)。
A. | B.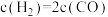 |
C.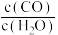 不再发生变化 不再发生变化 | D.混合气体密度不再发生变化 |
 与
与 发生反应II,在不同温度时测得CO的平衡转化率如图3所示。
发生反应II,在不同温度时测得CO的平衡转化率如图3所示。
①B、C两点对应的反应温度分别为
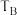 和
和 ,则
,则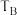
 (填“<”“=”或“>”)。
(填“<”“=”或“>”)。②A点对应温度下,反应II的化学平衡常数
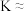
③若向A点对应的平衡体系中再充入
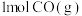 、
、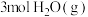 、
、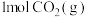 和
和 ,此时平衡向
,此时平衡向④实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以增大
 的体积分数,其原因为
的体积分数,其原因为
更新时间:2023-02-20 14:18:54
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】CH4、NH3、H2O、HF是第二周期的氢化物,也是生产生活中的重要物质。
(1)在25 ℃、101 kPa时,16 g CH4完全燃烧生成液态水时放出的热量是890.31 kJ,则CH4的燃烧热为________________ 。
(2) NH3和H2O中稳定性较高的是:___________ ,NH3和PH3中沸点较高的是:__________ 。
(3)如图所示组成闭合回路,其中,甲装置是由CH4、O2和CO2为反应物,稀土金属材料为电极,以熔融碳酸盐为电解质形成的原电池;乙装置中a、b为石墨,b极上有红色物质析出,CuSO4溶液的体积为200 mL。

①装置中气体A为________ (填“CH4”或“O2和CO2”),d极上的电极反应式为_______________________________________ 。
②乙装置中a极上的电极反应式为___________________ 。
若在a极产生112 mL(标准状况)气体,则甲装置中消耗CH4________ mL(标准状况),乙装置中所得溶液的pH=________ (忽略电解前后溶液体积变化)。
(1)在25 ℃、101 kPa时,16 g CH4完全燃烧生成液态水时放出的热量是890.31 kJ,则CH4的燃烧热为
(2) NH3和H2O中稳定性较高的是:
(3)如图所示组成闭合回路,其中,甲装置是由CH4、O2和CO2为反应物,稀土金属材料为电极,以熔融碳酸盐为电解质形成的原电池;乙装置中a、b为石墨,b极上有红色物质析出,CuSO4溶液的体积为200 mL。

①装置中气体A为
②乙装置中a极上的电极反应式为
若在a极产生112 mL(标准状况)气体,则甲装置中消耗CH4
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.回答下列问题:
(1)用括号内的字母代号填空:中和热测定实验时,若用环形铜丝代替环形玻璃搅拌棒,会导致测定的数值___________ (A.偏高;B.偏低)
Ⅱ.甲醚(CH3OCH3)是重要的化工原料,可用CO和H2制得,总反应的热化学方程式如为2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) ΔH=-206.0kJ·mol-1。该过程可分为以下两步反应完成:
CH3OCH3(g)+H2O(g) ΔH=-206.0kJ·mol-1。该过程可分为以下两步反应完成:
ⅰ.甲醇合成反应:2CO(g)+4H2(g) 2CH3OH(g) ΔH=-182.0 kJ·mol-1
2CH3OH(g) ΔH=-182.0 kJ·mol-1
ⅱ.甲醇脱水反应:
(2)请写出ⅱ中甲醇脱水反应的热化学方程式:___________ 。
(3)在一定条件下,将CO和H2按体积比1∶2充入恒容 密闭容器中,反应生成CH3OCH3(g)和H2O(g)。下列不能说明该反应达到平衡状态的是___________(填字母)。
(4)生产甲醚的过程中还存在以下副反应,与甲醇脱水反应形成竞争:CH3OH(g)+H2O(g)  CO2(g)+3H2(g) ΔH=+48.8 kJ·mol-1,将反应物混合气按进料比n(CO)∶n(H2)=1∶2通入反应装置,选择合适的催化剂。在不同温度和压强下,测得甲醚的选择性分别如图1、图2所示。
CO2(g)+3H2(g) ΔH=+48.8 kJ·mol-1,将反应物混合气按进料比n(CO)∶n(H2)=1∶2通入反应装置,选择合适的催化剂。在不同温度和压强下,测得甲醚的选择性分别如图1、图2所示。
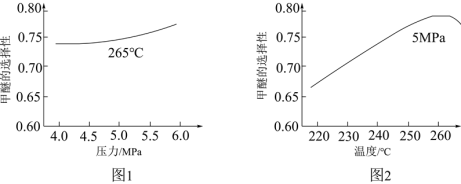
资料:甲醚的选择性是指转化为甲醚的CO在全部CO反应物中所占的比例。
①图1中,温度一定,压强增大,甲醚选择性增大的原因是___________ 。
②图2中,温度高于265℃后,甲醚选择性降低的原因是___________ 。
(1)用括号内的字母代号填空:中和热测定实验时,若用环形铜丝代替环形玻璃搅拌棒,会导致测定的数值
Ⅱ.甲醚(CH3OCH3)是重要的化工原料,可用CO和H2制得,总反应的热化学方程式如为2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g) ΔH=-206.0kJ·mol-1。该过程可分为以下两步反应完成:
CH3OCH3(g)+H2O(g) ΔH=-206.0kJ·mol-1。该过程可分为以下两步反应完成:ⅰ.甲醇合成反应:2CO(g)+4H2(g)
 2CH3OH(g) ΔH=-182.0 kJ·mol-1
2CH3OH(g) ΔH=-182.0 kJ·mol-1ⅱ.甲醇脱水反应:
(2)请写出ⅱ中甲醇脱水反应的热化学方程式:
(3)在一定条件下,将CO和H2按体积比1∶2充入
| A.混合气体的总物质的量保持不变 |
| B.混合气体的密度保持不变 |
| C.CH3OCH3(g)和H2O(g)的物质的量之比保持不变 |
| D.每生成1 mol CH3OCH3(g),同时生成2 mol CO |
 CO2(g)+3H2(g) ΔH=+48.8 kJ·mol-1,将反应物混合气按进料比n(CO)∶n(H2)=1∶2通入反应装置,选择合适的催化剂。在不同温度和压强下,测得甲醚的选择性分别如图1、图2所示。
CO2(g)+3H2(g) ΔH=+48.8 kJ·mol-1,将反应物混合气按进料比n(CO)∶n(H2)=1∶2通入反应装置,选择合适的催化剂。在不同温度和压强下,测得甲醚的选择性分别如图1、图2所示。
资料:甲醚的选择性是指转化为甲醚的CO在全部CO反应物中所占的比例。
①图1中,温度一定,压强增大,甲醚选择性增大的原因是
②图2中,温度高于265℃后,甲醚选择性降低的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
① 甲硅烷(SiH4)固态时属于___________ 晶体。
② 已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则其热化学方程式为______________________ 。
(2)甲醇燃料电池的总反应为:2CH3OH+3O2═2CO2↑+4H2O,其工作原理如下图所示。

①图中CH3OH从_____________ (填a或b)通入,该电池的正极是____________ (填M或N)电极,其中在N极发生的电极反应式是_____________________ 。
②如果在外电路中有1mol电子转移,则消耗标准状况下O2的体积为_______ L。
(3)25℃,101kPa条件下,14g N2和3g H2反应生成NH3的能量变化如下图所示:

已知:① x = 1127;
② 25℃ 101 kPa下,N2(g)+3H2(g) 2NH3(g) △H=-92kJ·mol—1。
2NH3(g) △H=-92kJ·mol—1。
则 y =__________ 。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
① 甲硅烷(SiH4)固态时属于
② 已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则其热化学方程式为
(2)甲醇燃料电池的总反应为:2CH3OH+3O2═2CO2↑+4H2O,其工作原理如下图所示。

①图中CH3OH从
②如果在外电路中有1mol电子转移,则消耗标准状况下O2的体积为
(3)25℃,101kPa条件下,14g N2和3g H2反应生成NH3的能量变化如下图所示:

已知:① x = 1127;
② 25℃ 101 kPa下,N2(g)+3H2(g)
 2NH3(g) △H=-92kJ·mol—1。
2NH3(g) △H=-92kJ·mol—1。则 y =
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】NO2和N2O4之间发生反应:N2O4 2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。
2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。
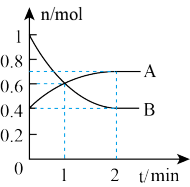
(1)曲线_______ (填“A”或“B”)表示NO2的物质的量随时间的变化曲线。在0到1min中内用A表示该反应的速率是______ ,该反应达最大限度时B的转化率___ 。
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(NO2)=0.3 mol·L-1·min-1,乙中v(N2O4)=0.2 mol·L-1·min-1,则__________ 中反应更快。
(3)下列描述能表示反应达平衡状态的是____ 。
A 容器中A与B的物质的量相等
B 容器内气体的颜色不再改变
C 2v(A)=v(B)
D 容器内气体的平均相对分子质量不再改变
E 容器内气体的密度不再发生变化
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨Ⅱ电极上生成氧化物Y(N2O5),则石墨I电极是_______ (填“正极”或“负极”),石墨Ⅱ的电极反应式为____ 。

 2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。
2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。
(1)曲线
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(NO2)=0.3 mol·L-1·min-1,乙中v(N2O4)=0.2 mol·L-1·min-1,则
(3)下列描述能表示反应达平衡状态的是
A 容器中A与B的物质的量相等
B 容器内气体的颜色不再改变
C 2v(A)=v(B)
D 容器内气体的平均相对分子质量不再改变
E 容器内气体的密度不再发生变化
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨Ⅱ电极上生成氧化物Y(N2O5),则石墨I电极是

您最近一年使用:0次
【推荐2】氢气作为清洁能源有着广泛的应用前景,采用天然气制备氢气的流程如下。请回答下列问题:
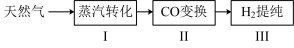
I.蒸汽转化:在催化剂的作用下,水蒸气将CH4氧化,结合图表信息回答问题。

(1)该过程的热化学方程式是_______________________ 。
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T1和T2的大小关系:T1__________ T2(选填“>”“<”或“=”),并说明理由:______________ 。
(3)一定温度下,在1 L恒容的密闭容器中充入1 mol CH4和1 mol水蒸气充分反应达到平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为__________ 。
II.CO变换:500℃时,CO进一步与水反应生成CO2和H2。反应的方程式如下:CO(g)+H2O(g) CO2(g)+H2(g) △H=-41 k/mol,在一定温度下的容积固定的密闭容器中进行上述反应。
CO2(g)+H2(g) △H=-41 k/mol,在一定温度下的容积固定的密闭容器中进行上述反应。
(4)写出一种可以提高CO转化率的措施:__________________ ,下列说法可以证明该反应已达到平衡状况的是__________ 。
A.断裂2 mol H-O键的同时断裂1 mol H-H键
B.容器内气体压强不再改变
C.H2的浓度不再改变
D.CO2和H2的浓度之比为1:1
III.模拟H2提纯工艺:将CO2和H2分离得到H2的过程如下。
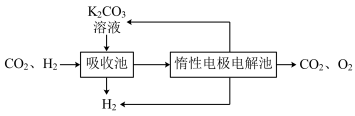
依据图示信息回答:
(5)吸收池中发生反应的离子方程式是_____________________ 。
(6)写出电解池中阳极发生的电极反应式:_____________________ 。

I.蒸汽转化:在催化剂的作用下,水蒸气将CH4氧化,结合图表信息回答问题。

(1)该过程的热化学方程式是
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T1和T2的大小关系:T1
(3)一定温度下,在1 L恒容的密闭容器中充入1 mol CH4和1 mol水蒸气充分反应达到平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为
II.CO变换:500℃时,CO进一步与水反应生成CO2和H2。反应的方程式如下:CO(g)+H2O(g)
 CO2(g)+H2(g) △H=-41 k/mol,在一定温度下的容积固定的密闭容器中进行上述反应。
CO2(g)+H2(g) △H=-41 k/mol,在一定温度下的容积固定的密闭容器中进行上述反应。(4)写出一种可以提高CO转化率的措施:
A.断裂2 mol H-O键的同时断裂1 mol H-H键
B.容器内气体压强不再改变
C.H2的浓度不再改变
D.CO2和H2的浓度之比为1:1
III.模拟H2提纯工艺:将CO2和H2分离得到H2的过程如下。

依据图示信息回答:
(5)吸收池中发生反应的离子方程式是
(6)写出电解池中阳极发生的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】甲醇(CH3OH)是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g);
CH3OH(g)+H2O(g);
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g);
CO(g)+H2O(g);
反应Ⅲ:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
回答下列问题:
(1)反应I进行的过程中体系内化学能减少,则反应I为______ (填“吸热”或“放热”)反应。
(2)已知反应Ⅱ为吸热反应,若反应Ⅱ在一绝热恒容密闭容器中进行,能说明反应已达到平衡状态的是______ (填字母)。
a.v(CO)=v(H2O)
b.温度不变
c.容器内CO2的体积分数保持不变
(3)250℃时,向体积为2L的恒容密闭容器中充入3molH2和1molCO2发生反应Ⅱ。经过5min达到平衡状态,平衡时测得CO2的转化率为50%。
①该温度下,反应开始至5min时,该反应的平均反应速率v(H2)=______ 。
②平衡时,H2的体积分数为_______ %,CO的物质的量浓度为______ mol•L-1。
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。
①Li-CO2电池中,研究表明该电池反应产物为碳酸锂和单质碳,正极CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ中CO2与CO 反应的离子方程式。
反应的离子方程式。
I.2CO2+2e-=C2O
Ⅱ.C2O =CO2+CO
=CO2+CO
Ⅲ._______
Ⅳ.CO +2Li+=Li2CO3
+2Li+=Li2CO3
②根据①中反应步骤,可以判断Li-CO2电池中,在负极参与反应的物质为_______ (填“Li”或“CO2”)。
反应I:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g);
CH3OH(g)+H2O(g);反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g);
CO(g)+H2O(g);反应Ⅲ:CO(g)+2H2(g)
 CH3OH(g)。
CH3OH(g)。回答下列问题:
(1)反应I进行的过程中体系内化学能减少,则反应I为
(2)已知反应Ⅱ为吸热反应,若反应Ⅱ在一绝热恒容密闭容器中进行,能说明反应已达到平衡状态的是
a.v(CO)=v(H2O)
b.温度不变
c.容器内CO2的体积分数保持不变
(3)250℃时,向体积为2L的恒容密闭容器中充入3molH2和1molCO2发生反应Ⅱ。经过5min达到平衡状态,平衡时测得CO2的转化率为50%。
①该温度下,反应开始至5min时,该反应的平均反应速率v(H2)=
②平衡时,H2的体积分数为
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。
①Li-CO2电池中,研究表明该电池反应产物为碳酸锂和单质碳,正极CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ中CO2与CO
 反应的离子方程式。
反应的离子方程式。I.2CO2+2e-=C2O

Ⅱ.C2O
 =CO2+CO
=CO2+CO
Ⅲ.
Ⅳ.CO
 +2Li+=Li2CO3
+2Li+=Li2CO3②根据①中反应步骤,可以判断Li-CO2电池中,在负极参与反应的物质为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中NO(g)和CO(g)反应生成无毒的 和
和 。
。
(1)已知:
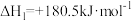
CO的燃烧热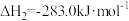
则

_______  。
。
(2)实验测得,反应 的
的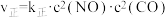 ,
,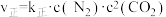 。(
。( 、
、 为速率常数,只与温度有关)
为速率常数,只与温度有关)
①达到平衡后,仅升高温度, 增大的倍数
增大的倍数_______ (填“>”、“<”或“=”)  增大的倍数。
增大的倍数。
②若在2 L的密闭容器中充入1 mol CO和1 mol NO,一定温度下达到平衡时,CO的转化率为40%,则
_______ (精确到0.1)。
(3)化学研究小组在三个容积为5 L的恒容密闭容器中,分别充入0.4 mol NO和0.4 mol CO,发生反应 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
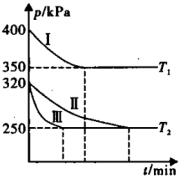
①温度:T1_______ T2(填“<”、“=”或“>”,下同)。
②CO的平衡转化率:Ⅰ_______ Ⅱ_______ Ⅲ。
③T2时的平衡常数
_______ (列出计算式即可)。
(4)碘蒸气存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: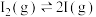 (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程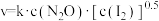 (k为速率常数)。下列表述正确的是_______(填字母)。
(k为速率常数)。下列表述正确的是_______(填字母)。
 和
和 。
。(1)已知:

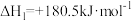
CO的燃烧热
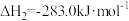
则


 。
。(2)实验测得,反应
 的
的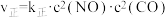 ,
,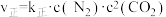 。(
。( 、
、 为速率常数,只与温度有关)
为速率常数,只与温度有关)①达到平衡后,仅升高温度,
 增大的倍数
增大的倍数 增大的倍数。
增大的倍数。②若在2 L的密闭容器中充入1 mol CO和1 mol NO,一定温度下达到平衡时,CO的转化率为40%,则

(3)化学研究小组在三个容积为5 L的恒容密闭容器中,分别充入0.4 mol NO和0.4 mol CO,发生反应
 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
①温度:T1
②CO的平衡转化率:Ⅰ
③T2时的平衡常数

(4)碘蒸气存在能大幅度提高
 的分解速率,反应历程为:
的分解速率,反应历程为:第一步:
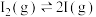 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
 (快反应)
(快反应)实验表明,含碘时
 分解速率方程
分解速率方程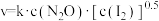 (k为速率常数)。下列表述正确的是_______(填字母)。
(k为速率常数)。下列表述正确的是_______(填字母)。A. 分解反应速率与是否含碘蒸气无关 分解反应速率与是否含碘蒸气无关 |
| B.第二步对总反应速率起决定作用 |
| C.第二步活化能最小 |
| D.IO为反应的催化剂 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Fe是日常生活中最常用的金属之一。回答下列问题:
(1)深埋在潮湿土壤中的铁管道,在硫酸盐还原菌(该还原菌最佳生存环境在pH为7~8之间)作用下,能被SO42-腐蚀,其电化学腐蚀原理如下图所示,写出正极的电极反应式___________________ 。

(2)在1800K时,2Fe(s)+3/2O2(g)=Fe2O3(s) ∆H=-354.2kJ/mol;3Fe(s)+2O2(g)=Fe3O4(s) ∆H=-550.9kJ/mol则反应:2Fe3O4(s)+1/2O2(g) ===3Fe2O3(s)的∆H为_____ kJ·mol−1,四氧化三铁在充满氧气的集气瓶中反应生成Fe2O3_____ (填“能”或“不能”)自发进行。
(3)Fe3+和I-在水溶液中的反应如下:2I-+2Fe3+ 2Fe2+ +I2(在水溶液中)。
2Fe2+ +I2(在水溶液中)。
①298K时,向5mL 0.1mol∙L−1 的KI溶液中滴加0.1mol∙L−1 FeCl3溶液,得到c(Fe2+)与加入FeCl3 溶液体积关系如下图所示:

该温度下滴加5mL FeCl3溶液时,Fe3+的平衡转化率=_____ %,平衡常数K=_____ ,若要提高Fe3+的转化率,可采取的措施是________________________ 。
②在已经达到平衡的上述反应体系中,加入苯对I2进行萃取,保持温度不变,反应速率_____ (填“增大”、“减小”或“不变”),此时υ(正)_____ υ(逆)(填“大于”、“小于”或“等于”)。
③υ(正)与Fe3+、I−的浓度关系为υ=kc(I-)mc(Fe3+)n(k为常数)
通过分析所给数据计算可知:在υ=kc(I-)mc(Fe3+)n 中,m,n的值为_____ (填字母代号)。
A.m=1,n=1 B.m=2,n=1 C.m=2,n=2 D.m=1,n=2
(1)深埋在潮湿土壤中的铁管道,在硫酸盐还原菌(该还原菌最佳生存环境在pH为7~8之间)作用下,能被SO42-腐蚀,其电化学腐蚀原理如下图所示,写出正极的电极反应式

(2)在1800K时,2Fe(s)+3/2O2(g)=Fe2O3(s) ∆H=-354.2kJ/mol;3Fe(s)+2O2(g)=Fe3O4(s) ∆H=-550.9kJ/mol则反应:2Fe3O4(s)+1/2O2(g) ===3Fe2O3(s)的∆H为
(3)Fe3+和I-在水溶液中的反应如下:2I-+2Fe3+
 2Fe2+ +I2(在水溶液中)。
2Fe2+ +I2(在水溶液中)。①298K时,向5mL 0.1mol∙L−1 的KI溶液中滴加0.1mol∙L−1 FeCl3溶液,得到c(Fe2+)与加入FeCl3 溶液体积关系如下图所示:

该温度下滴加5mL FeCl3溶液时,Fe3+的平衡转化率=
②在已经达到平衡的上述反应体系中,加入苯对I2进行萃取,保持温度不变,反应速率
③υ(正)与Fe3+、I−的浓度关系为υ=kc(I-)mc(Fe3+)n(k为常数)
| c(I−)mol∙L−1 | c(Fe3+)mol∙L−1 | υ (mol∙L−1∙s−1 ) | |
| (1) | 0.20 | 0.80 | 0.032k |
| (2) | 0.60 | 0.40 | 0.144k |
| (3) | 0.80 | 0.20 | 0.128k |
通过分析所给数据计算可知:在υ=kc(I-)mc(Fe3+)n 中,m,n的值为
A.m=1,n=1 B.m=2,n=1 C.m=2,n=2 D.m=1,n=2
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】草酸(H2C2O4)是生物体的一种代谢产物,广泛分布于植物、动物和真菌中,并在不同的生物体中发挥着不同的作用。
(Ⅰ)草酸是一种二元有机弱酸,具有还原性。
(1)已知:25℃时,草酸的电离平衡常数Ka1=5.0×10-2,Ka2=5.4×10-5;碳酸(H2CO3)的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11。
①向Na2CO3溶液中加入少量草酸溶液,发生反应的离子方程式为___ 。
②常温下,用0.01mol•L-1的NaOH标准溶液滴定20mL0.01mol•L-1的草酸溶液,滴定曲线如图所示。

a点溶液呈___ (填“酸”“碱”或“中”)性;b点溶液中各离子浓度的大小关系为___ 。
(2)酸性KMnO4溶液可将草酸氧化为CO2,还原产物为Mn2+,该反应的离子方程式为___ 。
(Ⅱ)草酸分解生成CO和CO2,以CO或CO2,为原料均可制得甲醇。
(3)已知:i.2H2(g)+O2(g)=2H2O(l) ΔH1=-285.0kJ·mol-1;ii.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) ΔH2=-726.0kJ·mol-1。则二氧化碳与氢气反应生成液态甲醇和液态水(该反应为可逆反应)的热化学方程式为
O2(g)=CO2(g)+2H2O(l) ΔH2=-726.0kJ·mol-1。则二氧化碳与氢气反应生成液态甲醇和液态水(该反应为可逆反应)的热化学方程式为___ 。
(4)利用CO与H2合成甲醇的反应原理为CO(g)+2H2(g)⇌CH3OH(g)。现向一容积可变的密闭容器中充入10molCO(g)和20molH2(g)发生上述反应,CO的平衡转化率(α)与温度(T)、压强(p)的变化关系如图所示。

①该反应为___ (填“放热”或“吸热”)反应,A、B、C三点的平衡常数K(A)、K(B)、K(C)的大小关系为___ ,压强的大小关系为p1___ (填“大于”“小于”或“等于”)p2。
②若A点时,保持容器容积和温度不变,向容器中再充入2molCO(g)、4molH2(g)和2molCH3OH(g),则v正___ (填“>”或“<”)v逆。
(Ⅰ)草酸是一种二元有机弱酸,具有还原性。
(1)已知:25℃时,草酸的电离平衡常数Ka1=5.0×10-2,Ka2=5.4×10-5;碳酸(H2CO3)的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11。
①向Na2CO3溶液中加入少量草酸溶液,发生反应的离子方程式为
②常温下,用0.01mol•L-1的NaOH标准溶液滴定20mL0.01mol•L-1的草酸溶液,滴定曲线如图所示。

a点溶液呈
(2)酸性KMnO4溶液可将草酸氧化为CO2,还原产物为Mn2+,该反应的离子方程式为
(Ⅱ)草酸分解生成CO和CO2,以CO或CO2,为原料均可制得甲醇。
(3)已知:i.2H2(g)+O2(g)=2H2O(l) ΔH1=-285.0kJ·mol-1;ii.CH3OH(l)+
 O2(g)=CO2(g)+2H2O(l) ΔH2=-726.0kJ·mol-1。则二氧化碳与氢气反应生成液态甲醇和液态水(该反应为可逆反应)的热化学方程式为
O2(g)=CO2(g)+2H2O(l) ΔH2=-726.0kJ·mol-1。则二氧化碳与氢气反应生成液态甲醇和液态水(该反应为可逆反应)的热化学方程式为(4)利用CO与H2合成甲醇的反应原理为CO(g)+2H2(g)⇌CH3OH(g)。现向一容积可变的密闭容器中充入10molCO(g)和20molH2(g)发生上述反应,CO的平衡转化率(α)与温度(T)、压强(p)的变化关系如图所示。

①该反应为
②若A点时,保持容器容积和温度不变,向容器中再充入2molCO(g)、4molH2(g)和2molCH3OH(g),则v正
您最近一年使用:0次



