 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。(1)
 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与
与 反应的化学方程式
反应的化学方程式(2)将一定量的
 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有(3)查阅资料知:
 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
①已知
 能发生如下反应:
能发生如下反应: 。
。上述反应中氧化剂是
②根据上述反应鉴别
 和NaCl。可选用的物质有
和NaCl。可选用的物质有A.水 B.碘化钾淀粉试纸 C.淀粉 D.白酒 E.食用白醋
③某厂废液中含有3%—6%的
 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是A.浓硫酸 B.
 C.
C. D.
D.
(4)某学习小组以过氧化钠为原料制备出了一定量的纯碱,不小心混入了少量的
 ,现欲对其纯度进行测定,将ag样品加热至质量不再发生变化,其质量变为bg,则该纯碱样品的纯度(即质量分数)为
,现欲对其纯度进行测定,将ag样品加热至质量不再发生变化,其质量变为bg,则该纯碱样品的纯度(即质量分数)为
更新时间:2023-02-28 06:48:30
|
相似题推荐
【推荐1】回答下列问题:
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO4 K2MnO4+MnO2+O2↑,其中被氧化的元素是
K2MnO4+MnO2+O2↑,其中被氧化的元素是___________ (填元素符号),还原产物是___________ (填化学式)。
(2)反应方程式:K2Cr2O7+14HCl 2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是
2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是___________ ,氧化产物是___________ 。
(3)下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
1、反应②的离子方程式为___________ 。
II、反应①中,氧化产物与还原产物的质量比为___________ 。
III、已知反应④:4HCl+O2 2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为___________ 。
IV、配平③______KMnO4+_____HCl(浓)=_____KCl+____MnCl2+_____Cl2↑+____H2O,___________
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO4
 K2MnO4+MnO2+O2↑,其中被氧化的元素是
K2MnO4+MnO2+O2↑,其中被氧化的元素是(2)反应方程式:K2Cr2O7+14HCl
 2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是
2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是(3)下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
1、反应②的离子方程式为
II、反应①中,氧化产物与还原产物的质量比为
III、已知反应④:4HCl+O2
 2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为IV、配平③______KMnO4+_____HCl(浓)=_____KCl+____MnCl2+_____Cl2↑+____H2O,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究物质时会涉及物质的组成、分类、性质和用途等方面。请填写下列空白:
(1)二氧化氮气体的颜色为:______ ;二氧化氮溶于水时生成硝酸和一氧化氮,工业上利用这一原理生产_____ 。
(2)Na2O属于______ (填“酸性”或“碱性”)氧化物;在潜水艇和消防员呼吸面具中,Na2O2与CO2反应的化学方程式为______ 。
(3)生活中不锈钢广告牌上的图形或文字是用氯化铁溶液蚀刻而成的,反应原理为2FeCl3+Fe=3FeCl2,其中FeCl3做______ (填“氧化剂”或“还原剂”),若有lmolFe发生反应,则转移电子的物质的量为______ mol。
(1)二氧化氮气体的颜色为:
(2)Na2O属于
(3)生活中不锈钢广告牌上的图形或文字是用氯化铁溶液蚀刻而成的,反应原理为2FeCl3+Fe=3FeCl2,其中FeCl3做
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】目前,能较稳定存在的氯的氧化物有Cl2O、ClO2、Cl2O7等。有关数据见表:
请回答下列问题:
(1)常温、常压下,三种氧化物中属于气体的是_______ 。
(2)Cl2O7属于酸性氧化物,它与水反应的离子方程式为_______ 。
(3)ClO2是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。在消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,说明ClO2具有_______ 性。
(4)工业上可以用下列反应制备ClO2:2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,请用单线桥法表示出该反应电子转移的方向和数目_______ 。
(5)工业上制备ClO2的反应原理为:2NaClO3+4HCl(浓)=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是_______ (填序号)。
A.还原性 B.氧化性 C.酸性
②若上述反应中产生2个ClO2,则转移的电子数为_______ 。
| 化学式 | Cl2O | ClO2 | Cl2O7 |
| 沸点/℃ | 3.8 | 11.0 | 82.0 |
请回答下列问题:
(1)常温、常压下,三种氧化物中属于气体的是
(2)Cl2O7属于酸性氧化物,它与水反应的离子方程式为
(3)ClO2是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。在消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,说明ClO2具有
(4)工业上可以用下列反应制备ClO2:2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,请用单线桥法表示出该反应电子转移的方向和数目
(5)工业上制备ClO2的反应原理为:2NaClO3+4HCl(浓)=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是
A.还原性 B.氧化性 C.酸性
②若上述反应中产生2个ClO2,则转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钠及其化合物是重要的化学物质。回答下列问题:
(1) 、
、 、
、 、
、 久置空气中最终都变为
久置空气中最终都变为_________ (填化学式)。
(2)小块金属钠投入水中发生反应的离子方程式为_________ 。
(3) 、
、 都属于
都属于_________ (“碱性氧化物”或“氧化物”),可用蒸馏水检验 中混有少量
中混有少量 ,试用化学方程式解释含有
,试用化学方程式解释含有 的现象:
的现象:_________ 。
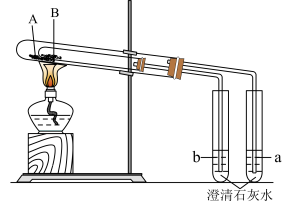
(4)如图装置可用于鉴别 和
和 ,这是根据它们具有不同的
,这是根据它们具有不同的_________ 性质加以鉴别。实验中可观察到b中澄清石灰水变浑浊,则物质A为_________ (填名称)。
(5) 溶液与
溶液与 溶液混合产生
溶液混合产生 白色沉淀。生成
白色沉淀。生成 的反应过程:
的反应过程: 、
、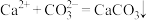 。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
(1)
 、
、 、
、 、
、 久置空气中最终都变为
久置空气中最终都变为(2)小块金属钠投入水中发生反应的离子方程式为
(3)
 、
、 都属于
都属于 中混有少量
中混有少量 ,试用化学方程式解释含有
,试用化学方程式解释含有 的现象:
的现象:(4)如图装置可用于鉴别
 和
和 ,这是根据它们具有不同的
,这是根据它们具有不同的
(5)
 溶液与
溶液与 溶液混合产生
溶液混合产生 白色沉淀。生成
白色沉淀。生成 的反应过程:
的反应过程: 、
、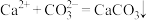 。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:| 实验步骤 | 实验现象 |
ⅰ.取少量 溶液,向其中加入适量 溶液,向其中加入适量 溶液 溶液 | 无明显现象 |
| ⅱ.向上述溶液中滴加 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1) 20世纪前,黑火药是世界上唯一的火箭推进剂,黑火药是由硝酸钾、硫磺、木炭组成,黑火药爆炸的化学方程式为:S+2KNO3+3C═K2S+N2↑+3CO2。
①写出N2的电子式 :___________
②已知SO2和氯水反应会生成两种强酸,其离子方程式为___________
③请设计实验检验上述含氧酸根离子:___________
(2)排放二氧化硫、氮氧化物均会危害环境,必须对它们进行处理。。处理氮氧化物的方法很多,以下列举几种常见方法。
①用过量NaOH溶液吸收NO2气体。所得溶液中除含有NaOH和NaNO2,还含有___________ 。
②为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。
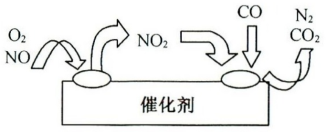
写出净化过程中的总化学反应方程式:___________
③请写出NH3与少量氯气反应的化学方程式:___________
(3)写出过氧化钠与水反应的化学方程式:___________
①写出N2的电子式 :
②已知SO2和氯水反应会生成两种强酸,其离子方程式为
③请设计实验检验上述含氧酸根离子:
(2)排放二氧化硫、氮氧化物均会危害环境,必须对它们进行处理。。处理氮氧化物的方法很多,以下列举几种常见方法。
①用过量NaOH溶液吸收NO2气体。所得溶液中除含有NaOH和NaNO2,还含有
②为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。

写出净化过程中的总化学反应方程式:
③请写出NH3与少量氯气反应的化学方程式:
(3)写出过氧化钠与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.有关Na2O2和H2O的反应,由实验现象可得出的结论如下:a.有O2生成;b.反应放热
(1)Na2O2与水反应的化学方程式是___________ 。
(2)某学习小组拟用如图装置进行实验,以证明上述结论。

①用以验证结论a的实验方法:打开分液漏斗活塞,使水流入试管,___________ 。(填验证方法和步骤)
②用以验证结论b的实验方法:反应前将q导管口连接一橡胶管,浸入盛有水的水槽中,分液漏斗滴入水后,观察到___________ ,证明反应是放热的。
Ⅱ.在两份相同的滴加了酚酞的Ba(OH)2溶液中,分别缓慢滴入导电能力几乎相等的H2SO4和NaHSO4溶液,混合溶液的导电能力随滴入溶液体积变化的曲线如图所示。
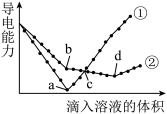
(3)若缓缓滴入NaHSO4溶液至过量,则滴入过程中的导电能力用图中的___________ 曲线表示(填“①”或“②”)。
(4)d点溶液中大量存在的离子是___________
(1)Na2O2与水反应的化学方程式是
(2)某学习小组拟用如图装置进行实验,以证明上述结论。

①用以验证结论a的实验方法:打开分液漏斗活塞,使水流入试管,
②用以验证结论b的实验方法:反应前将q导管口连接一橡胶管,浸入盛有水的水槽中,分液漏斗滴入水后,观察到
Ⅱ.在两份相同的滴加了酚酞的Ba(OH)2溶液中,分别缓慢滴入导电能力几乎相等的H2SO4和NaHSO4溶液,混合溶液的导电能力随滴入溶液体积变化的曲线如图所示。

(3)若缓缓滴入NaHSO4溶液至过量,则滴入过程中的导电能力用图中的
(4)d点溶液中大量存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图为一个五圆环,每个环中的物质依次为 、NaCl、
、NaCl、 、
、 、
、 ,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
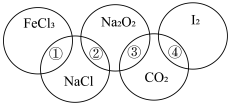
(1)关于上述相交部分的说法不正确的是______(填选项),
(2)上述五种物质中,有两种物质可以发生氧化还原反应,其化学方程式为____________ ;
(3)用洁净的烧杯取少量蒸馏水。用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol/L上图中某物质M的溶液,继续煮沸得到红褐色透明液体。
①物质M的化学式为______ ,向上述所得红褐色透明液体中加入电极通电后, 胶体粒子移向
胶体粒子移向______ 极;(填“阴极”或“阳极”)
②检验该红褐色透明液体是胶体的方法为__________________ ;
③往该红褐色透明液体中逐滴加入稀硫酸溶液至过量,现象是________________ ,此反应的离子反应方程式为____________
 、NaCl、
、NaCl、 、
、 、
、 ,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
(1)关于上述相交部分的说法不正确的是______(填选项),
| A.①表示盐类 | B.②表示钠的化合物 | C.③表示氧化物 | D.④表示单质 |
(3)用洁净的烧杯取少量蒸馏水。用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol/L上图中某物质M的溶液,继续煮沸得到红褐色透明液体。
①物质M的化学式为
 胶体粒子移向
胶体粒子移向②检验该红褐色透明液体是胶体的方法为
③往该红褐色透明液体中逐滴加入稀硫酸溶液至过量,现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列七种物质:①CO2 ②过氧化钠 ③氧化铁 ④0.5 mol/LNaOH溶液 ⑤碳酸氢钠 ⑥0.5 mol/LNaHSO4溶液 ⑦次氯酸钠。请根据上述物质回答下列问题:
(1)写出物质对应的用途(填序号)。
②______ ③_______ ⑤________ ⑦________ 。
(2)含有0.4 mol氧原子的①在标准状况下的体积为______ L。
(3)④⑥两种溶液混合可以发生反应,离子方程式为______ 。
(4)废水脱氮工艺有一种方法是在废水中加入过量⑦使 完全转化为N2,此方法可用离子方程式表示为:2
完全转化为N2,此方法可用离子方程式表示为:2 +3ClO-=N2↑+3Cl-+2H++3H2O。该反应中氧化剂与还原剂的物质的量之比为
+3ClO-=N2↑+3Cl-+2H++3H2O。该反应中氧化剂与还原剂的物质的量之比为______ ;用单线桥法在离子方程式上标出电子转移的方向和数目______ ;
(5)某同学帮助水质检测站配制240 mL④溶液以备使用。
①该同学应用托盘天平称取NaOH固体______  。
。
②下列图示对应的操作规范的是______ (填序号)。
A.称量 B.溶解
B.溶解
C.转移 D.定容
D.定容
③定容时加水不慎超过了刻度线,用胶头滴管吸出少量溶液,所配制溶液的浓度会______ (填“偏大”“偏小”或“无影响”)。
(1)写出物质对应的用途(填序号)。
| 物质 用途 ② a.面粉发酵粉 ③ b.84消毒液的有效成分 ⑤ c.呼吸面具中作供氧剂 ⑦ d.红色油漆和涂料 |
②
(2)含有0.4 mol氧原子的①在标准状况下的体积为
(3)④⑥两种溶液混合可以发生反应,离子方程式为
(4)废水脱氮工艺有一种方法是在废水中加入过量⑦使
 完全转化为N2,此方法可用离子方程式表示为:2
完全转化为N2,此方法可用离子方程式表示为:2 +3ClO-=N2↑+3Cl-+2H++3H2O。该反应中氧化剂与还原剂的物质的量之比为
+3ClO-=N2↑+3Cl-+2H++3H2O。该反应中氧化剂与还原剂的物质的量之比为(5)某同学帮助水质检测站配制240 mL④溶液以备使用。
①该同学应用托盘天平称取NaOH固体
 。
。②下列图示对应的操作规范的是
A.称量
 B.溶解
B.溶解
C.转移
 D.定容
D.定容
③定容时加水不慎超过了刻度线,用胶头滴管吸出少量溶液,所配制溶液的浓度会
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学方程式、电离方程式、离子方程式都是非常重要的化学用语。
(1)常温常压下,现有下列十种物质:
①Al②NaHSO4③乙醇④CO2⑤醋酸⑥小苏打⑦Fe(OH)3⑧NaOH⑨氨水⑩(NH4)2SO4
上述状态下可导电的物质是______________ (填编号,下同);属于非电解质的是______________ 属于弱电解质的是________ ;⑤在水中的电离方程式为________ 。
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为__________ 。
(3)过氧化钠可作为呼吸面具和潜水艇中的供氧剂,写出过氧化钠与二氧化碳反应的化学方程式____________ 。
(4)请写出实验室制备Fe(OH)3胶体的离子方程式___________ 。
(5)已知PbSO4不溶于水,但可溶于醋酸铵溶液,反应方程式如下:PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,现将Na2S溶液与醋酸铅溶液混合有沉淀生成,则其反应的离子方程式应为___________ 。
(1)常温常压下,现有下列十种物质:
①Al②NaHSO4③乙醇④CO2⑤醋酸⑥小苏打⑦Fe(OH)3⑧NaOH⑨氨水⑩(NH4)2SO4
上述状态下可导电的物质是
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为
(3)过氧化钠可作为呼吸面具和潜水艇中的供氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(4)请写出实验室制备Fe(OH)3胶体的离子方程式
(5)已知PbSO4不溶于水,但可溶于醋酸铵溶液,反应方程式如下:PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,现将Na2S溶液与醋酸铅溶液混合有沉淀生成,则其反应的离子方程式应为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】溶液常 用作氧化还原反应滴定的标准液,利用
用作氧化还原反应滴定的标准液,利用 氧化
氧化 制备
制备 的装置如图所示(加热、夹持装置略):
的装置如图所示(加热、夹持装置略):
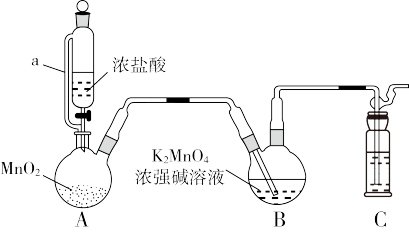
已知: 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
(1) 的化学名称为
的化学名称为_______ 。
(2)装置A中所发生反应的化学方程式为_______ ;其中a的作用是_______ 。
(3)装置C中盛装的试剂是_______ 。
(4)分析发现该装置有不足之处,改进的方法是_______ 。
(5)为测定某 固体的纯度,现用
固体的纯度,现用 的酸性
的酸性 溶液进行滴定。(已知:
溶液进行滴定。(已知: )称取
)称取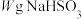 固体溶于水配成500mL溶液,取
固体溶于水配成500mL溶液,取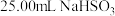 溶液置于锥形瓶中,用
溶液置于锥形瓶中,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液V mL。滴定终点的现象为
溶液V mL。滴定终点的现象为_______ , 固体的纯度为
固体的纯度为_______ 。
 用作氧化还原反应滴定的标准液,利用
用作氧化还原反应滴定的标准液,利用 氧化
氧化 制备
制备 的装置如图所示(加热、夹持装置略):
的装置如图所示(加热、夹持装置略):
已知:
 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
(1)
 的化学名称为
的化学名称为(2)装置A中所发生反应的化学方程式为
(3)装置C中盛装的试剂是
(4)分析发现该装置有不足之处,改进的方法是
(5)为测定某
 固体的纯度,现用
固体的纯度,现用 的酸性
的酸性 溶液进行滴定。(已知:
溶液进行滴定。(已知: )称取
)称取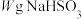 固体溶于水配成500mL溶液,取
固体溶于水配成500mL溶液,取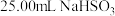 溶液置于锥形瓶中,用
溶液置于锥形瓶中,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液V mL。滴定终点的现象为
溶液V mL。滴定终点的现象为 固体的纯度为
固体的纯度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁是人类利用最为广泛的金属之一,工业炼铁一般用一氧化碳作还原剂。
(1)已知Fe2O3在高炉中有下列反应:Fe2O3+CO 2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是
2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是_________ 。
a.7:3 b.21: 8 c.14: 5 d.7:2
(2)若m(Fe):m(O)=3:1,则Fe2O3与FeO的物质的量之比为_________ ,Fe2O3被CO还原的物质的量分数为____________ 。
(3)3.04 g Fe2O3和FeO的混合固体粉末在加热条件下用足量CO使金属氧化物完全还原,生成的CO2气体通入含0.04 mol Ca(OH)2的澄清石灰水后,产生3.00 g白色沉淀。计算固体粉末中Fe2O3的质量。(保留1位小数)____________
(4)常温下,称取不同铁锈样品溶入足量盐酸,向溶液中加入足量NaOH溶液生成沉淀,然后过滤、洗涤、灼烧,得到Fe2O3固体,实验过程中产品无损失。
实验数据记录如下:
上述实验①②③④所用铁锈均不含杂质,且实验数据可靠。通过计算,分析和比较上表4组数据,给出结论。_______________
(1)已知Fe2O3在高炉中有下列反应:Fe2O3+CO
 2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是
2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是a.7:3 b.21: 8 c.14: 5 d.7:2
(2)若m(Fe):m(O)=3:1,则Fe2O3与FeO的物质的量之比为
(3)3.04 g Fe2O3和FeO的混合固体粉末在加热条件下用足量CO使金属氧化物完全还原,生成的CO2气体通入含0.04 mol Ca(OH)2的澄清石灰水后,产生3.00 g白色沉淀。计算固体粉末中Fe2O3的质量。(保留1位小数)
(4)常温下,称取不同铁锈样品溶入足量盐酸,向溶液中加入足量NaOH溶液生成沉淀,然后过滤、洗涤、灼烧,得到Fe2O3固体,实验过程中产品无损失。
实验数据记录如下:
实验序号 | 铁锈质量/g | 氧化铁质量/g |
① | 0.856 | 0.640 |
② | 1.424 | 1.280 |
③ | 0.979 | 0.880 |
④ | 1.070 | 0.800 |
上述实验①②③④所用铁锈均不含杂质,且实验数据可靠。通过计算,分析和比较上表4组数据,给出结论。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某铝合金中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:
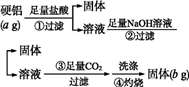
(1)写出上述第①②③步反应的离子方程式及第④步反应的化学方程式:
①___________ , __________ ;
②____________ , ____________ ,
Al3++4OH-=Al+2H2O;
③________ ,AlO2-+CO2+2H2O Al(OH)3↓+HCO3-;
Al(OH)3↓+HCO3-;
④_____________ 。
(2)该样品中铝的质量分数是_______ 。
(3)第②步中加入的NaOH溶液不足时,会使测定结果_____ ;第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果_____ ;第④步对沉淀灼烧不充分时,会使测定结果_____ 。(填选项)
A.偏高 B.偏低 C.无影响

(1)写出上述第①②③步反应的离子方程式及第④步反应的化学方程式:
①
②
Al3++4OH-=Al+2H2O;
③
 Al(OH)3↓+HCO3-;
Al(OH)3↓+HCO3-; ④
(2)该样品中铝的质量分数是
(3)第②步中加入的NaOH溶液不足时,会使测定结果
A.偏高 B.偏低 C.无影响
您最近一年使用:0次



