25℃时,对于pH相同的盐酸与醋酸溶液,下列说法正确的是
| A.水的电离程度:盐酸>醋酸 |
| B.加水稀释10倍后pH的大小:盐酸>醋酸 |
C.与等量Zn粉反应,相同时间内产生 的量:盐酸>醋酸 的量:盐酸>醋酸 |
| D.与足量NaOH溶液反应,消耗NaOH的量:盐酸>醋酸 |
22-23高二上·广东肇庆·期末 查看更多[2]
广东省肇庆市2022-2023学年高二上学期期末教学质量检测化学试题(已下线)专题06 电离平衡 水的电离和溶液的pH-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
更新时间:2023-03-02 23:26:23
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在25℃时,某稀溶液中由水电离产生的c(OH-)=10-10 mol•L-1.下列有关该溶液的叙述正确的是( )
| A.该溶液一定呈酸性 |
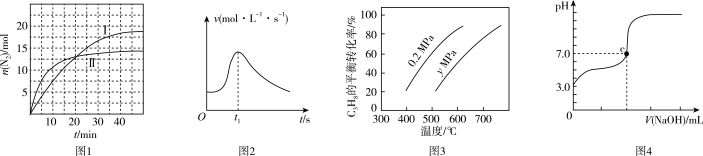
B.该溶液中 可能等于 可能等于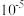  |
| C.该溶液的pH可能为4也可能为10 |
| D.该溶液有可能呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】关于水的电离,下列叙述中,正确的是
| A.升高温度,Kw增大,c(H+)不变 |
| B.向水中加入少量硫酸,c(H+)增大,Kw不变 |
| C.向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低 |
| D.向水中加入少量固体NaCl,平衡向逆反应方向移动,c(H+)降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知在25℃时,醋酸溶液中存在CH3COOH CH3COO-+H+,Ka=1.75×10-5。以下说法正确的是
CH3COO-+H+,Ka=1.75×10-5。以下说法正确的是
 CH3COO-+H+,Ka=1.75×10-5。以下说法正确的是
CH3COO-+H+,Ka=1.75×10-5。以下说法正确的是| A.向溶液中加入一定量的盐酸,平衡左移,Ka减小 |
| B.若CH3COOH的初始浓度为0.01mol/L,则平衡时c(H+)的数量级为10-4 |
| C.加水稀释,所有离子浓度均减小 |
D.加入少量冰醋酸, 值增大 值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法中不正确 的是
| A.常温下,0.1mol/L NaA溶液的pH为10 ,说明HA是弱酸 |
| B.用蒸馏水稀释1mol/L的醋酸溶液,c(CH3COOH)/c(H+)始终增大 |
| C.室温下,0.1mol/L 的HCl溶液与0.1mol/L NaOH溶液中水的电离程度相等 |
| D.任何温度下,利用H+和OH-浓度的相对大小均可以判断溶液的酸碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,将pH=3的CH3COOH溶液加水稀释至原体积的100倍后,溶液的
| A.pH=5 | B.pH>5 | C.pH<5 | D.pH=7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下列图示所得出的结论正确的是

| A.若图1表示不同温度下恒容密闭容器中,反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g)中n(N2)随时间的变化关系,说明平衡常数:KⅠ<KⅡ |
| B.若图2表示铝条与盐酸反应的化学反应速率随反应时间的变化关系,说明t1时刻溶液的温度最高 |
| C.若图3表示C3H8(g)⇌C2H4(g)+CH4(g)中C3H8的平衡转化率随温度、压强的变化关系,可以判断y>0.2 |
| D.若图4表示室温下用0.1000mol·L−1NaOH溶液滴定20.00mL0.1000mol·L−1某一元酸HX的滴定曲线,可以判断c点时消耗的V(NaOH)=20mL |
您最近一年使用:0次

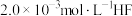 溶液的pH(忽略体积变化),该溶液中c(HF)、
溶液的pH(忽略体积变化),该溶液中c(HF)、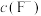 与pH的变化关系如下图所示。则下列说法不正确的是
与pH的变化关系如下图所示。则下列说法不正确的是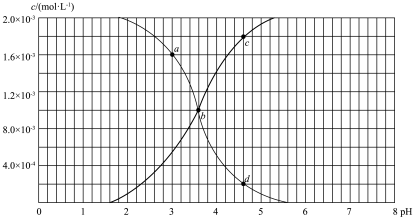


 相同的氨水和氢氧化钠溶液加水稀释相同倍数:
相同的氨水和氢氧化钠溶液加水稀释相同倍数: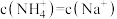
 和NaHS的混合溶液中:
和NaHS的混合溶液中:
 的强酸(HA)和
的强酸(HA)和 的一元碱等体积混合:c(OH-)≥c(H+)
的一元碱等体积混合:c(OH-)≥c(H+)

