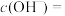求100℃下,NaCl水溶液中c(H+)=_______ ,pH=_______ 。
22-23高二·全国·课时练习 查看更多[1]
(已下线)第三章水溶液中的离子反应与平衡——整体认识
更新时间:2023-03-08 17:53:02
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知pOH也可以用来表示溶液的酸碱度,规定pOH=−lgc平(OH-)。不同温度下,水溶液中pOH与pH的关系如图所示。
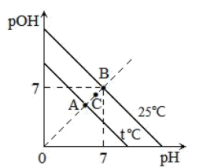
回答下列问题:
(1)t___________ 25(填“>”或“<”),图中A、B、C三点对应水的电离程度由大到小的顺序是___________ 。
(2)25℃时,向 溶液中逐滴加入等浓度的
溶液中逐滴加入等浓度的 溶液至
溶液至 恰好沉淀完全。
恰好沉淀完全。
①此过程中水的电离平衡___________ (填“正向”、“逆向”或“不”)移动。
②写出该过程发生反应的离子方程式___________ ;若反应前后溶液体积的变化忽略不计,则反应后所得溶液的pH值为___________ (已知 )。
)。
(3)已知80℃时,水的离子积常数 。该温度下,0.1mol/L某一元酸(HA)溶液中
。该温度下,0.1mol/L某一元酸(HA)溶液中 ,该溶液中由水电离的c平(H+)为
,该溶液中由水电离的c平(H+)为___________ ,用电离方程式表示该溶液中存在的电离平衡___________ 。

回答下列问题:
(1)t
(2)25℃时,向
 溶液中逐滴加入等浓度的
溶液中逐滴加入等浓度的 溶液至
溶液至 恰好沉淀完全。
恰好沉淀完全。①此过程中水的电离平衡
②写出该过程发生反应的离子方程式
 )。
)。(3)已知80℃时,水的离子积常数
 。该温度下,0.1mol/L某一元酸(HA)溶液中
。该温度下,0.1mol/L某一元酸(HA)溶液中 ,该溶液中由水电离的c平(H+)为
,该溶液中由水电离的c平(H+)为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】ⅰ.(1)氨气极易溶于水,氨气与水反应的化学方程式为_____________________ ;
氨水显碱性的原因是_____________________________ (用离子方程式表示)。
(2)在6份0.01 mol·L-1的氨水中分别加入下列物质:
A.浓氨水 B.纯水 C.少量浓硫酸 D.少量NaOH固体 E.少量Al2(SO4)3固体
①能使c(OH-)减少、c(NH4+)增大的是____ (填字母,下同)。
②能使c(OH-)增大、c(NH4+)减少的是____ 。
③能使c(OH-)和c(NH4+)都增大的是____ 。
④能使c(OH-)和c(NH4+)都减少的是____ 。
ⅱ.某温度下纯水中c(H+)=2×10-7 mol·L-1,则此时c(OH-)=________ ;该温度下向纯水中加盐酸使c(H+)=5×10-6 mol·L-1,则此时c(OH-)=______________________________ 。
氨水显碱性的原因是
(2)在6份0.01 mol·L-1的氨水中分别加入下列物质:
A.浓氨水 B.纯水 C.少量浓硫酸 D.少量NaOH固体 E.少量Al2(SO4)3固体
①能使c(OH-)减少、c(NH4+)增大的是
②能使c(OH-)增大、c(NH4+)减少的是
③能使c(OH-)和c(NH4+)都增大的是
④能使c(OH-)和c(NH4+)都减少的是
ⅱ.某温度下纯水中c(H+)=2×10-7 mol·L-1,则此时c(OH-)=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】常温下,有 0.1 mol/L 的四种溶液:①HCl ②CH3COOH ③NaOH ④Na2CO3
(1)用化学用语解释溶液①呈酸性的原因:_________ 。
(2)溶液③的 pH=_________ 。
(3)溶液①、②分别与等量的溶液③恰好完全反应,消耗的体积:①_________ ②(填“>”、“<”或“=”)。
(4)溶液④加热后碱性增强,结合化学用语解释原因:_________ 。
(5)常温下,下列关于溶液②的判断正确的是_________ 。
a.c(CH3COO−) = 0.1 mol/L
b.溶液中c(H+) > c(CH3COO−) > c(OH −)
c.加入CH3COONa(s),c(H+)不变
d.滴入 NaOH 浓溶液,溶液导电性增强
(1)用化学用语解释溶液①呈酸性的原因:
(2)溶液③的 pH=
(3)溶液①、②分别与等量的溶液③恰好完全反应,消耗的体积:①
(4)溶液④加热后碱性增强,结合化学用语解释原因:
(5)常温下,下列关于溶液②的判断正确的是
a.c(CH3COO−) = 0.1 mol/L
b.溶液中c(H+) > c(CH3COO−) > c(OH −)
c.加入CH3COONa(s),c(H+)不变
d.滴入 NaOH 浓溶液,溶液导电性增强
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请按照下列要求回答问题:
(1)电解氯化钠溶液的化学方程式:__________________________________ 。
(2)硫化钠水解的离子方程式:________________________________ 。
(3)0.1 mol/L 的碳酸钠溶液中离子浓度由大到小顺序为:__________________________ 。
(4)浓的 Al2(SO4)3 溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理__________________________ 。
(5)将25℃下 pH=12 的 Ba(OH)2 溶液aL与 pH=1的HCl溶液bL 混合,若所得混合液为中性,则 a:b=__________________________ 。(溶液体积变化忽略不计)。
(6)pH=3 的 NH4Cl 溶液,由水电离出的 c(H+)=__________________________ 。
(7)常温时,Fe(OH)3 的溶度积常数 Ksp=1×10-38,要使溶液中的 Fe3+沉淀完全(残留的 c(Fe3+)<10-5 mol·L-1),则 溶液的 pH 应大于____________________________ 。
(1)电解氯化钠溶液的化学方程式:
(2)硫化钠水解的离子方程式:
(3)0.1 mol/L 的碳酸钠溶液中离子浓度由大到小顺序为:
(4)浓的 Al2(SO4)3 溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理
(5)将25℃下 pH=12 的 Ba(OH)2 溶液aL与 pH=1的HCl溶液bL 混合,若所得混合液为中性,则 a:b=
(6)pH=3 的 NH4Cl 溶液,由水电离出的 c(H+)=
(7)常温时,Fe(OH)3 的溶度积常数 Ksp=1×10-38,要使溶液中的 Fe3+沉淀完全(残留的 c(Fe3+)<10-5 mol·L-1),则 溶液的 pH 应大于
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】盐酸、醋酸和氨水是中学化学中常见的三种物质,某校实验小组利用浓盐酸、冰醋酸和浓氨水分别配制了浓度均为0.1mol•L-1的三种溶液各100mL并进行相关实验,据此回答下列问题:
(1)配制上述三种溶液的过程中会用到的玻璃仪器有量筒、烧杯、玻璃棒,以及___________ 。
(2)将浓度均为0.1mol•L-1的盐酸和氨水等体积混合,则
①所得混合溶液显___________ 性(填“酸性”、“碱性”或“中性”),原因是___________ (用离子方程式表示)
②所得混合溶液中所有离子的物质的量浓度由大到小的顺序为:___________ ;
③25℃时,使用pH计测得此混合溶液的pH为a,则混合溶液中c(NH )=
)=___________ mol•L-1(用含a的代数式表示,混合过程中溶液体积的微小变化忽略不计)。
(1)配制上述三种溶液的过程中会用到的玻璃仪器有量筒、烧杯、玻璃棒,以及
(2)将浓度均为0.1mol•L-1的盐酸和氨水等体积混合,则
①所得混合溶液显
②所得混合溶液中所有离子的物质的量浓度由大到小的顺序为:
③25℃时,使用pH计测得此混合溶液的pH为a,则混合溶液中c(NH
 )=
)=
您最近一年使用:0次

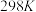 时,酸HA的电离平衡常数
时,酸HA的电离平衡常数 ,水的离子积
,水的离子积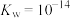 .试计算,在该温度下:
.试计算,在该温度下: 的HA溶液中,由水电离产生的
的HA溶液中,由水电离产生的