密闭容器中,分别加入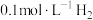 和
和 ,发生反应
,发生反应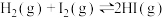 ,记录数据如下表所示。
,记录数据如下表所示。
(1)在0~30s内,用 表示的化学反应速率
表示的化学反应速率
_______ 。
(2)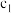
_______ 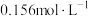 、
、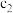
_______ 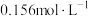 (均填“≥”“≤”或“=”)。
(均填“≥”“≤”或“=”)。
(3)求0~60s以不同物质表示的化学反应速率之比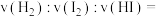
_______ 。
(4)一定温度下的密闭容器中,判断该可逆反应达到平衡状态的标志是_______。
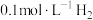 和
和 ,发生反应
,发生反应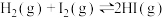 ,记录数据如下表所示。
,记录数据如下表所示。| 时间/s | 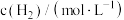 |  | 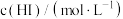 |
| 0 | 0.100 | 0.100 | 0 |
| 30 | 0.040 | 0.040 | 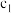 |
| 60 | 0.022 | 0.022 | 0.156 |
| 80 | 0.022 | 0.022 | 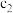 |
 表示的化学反应速率
表示的化学反应速率
(2)
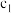
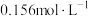 、
、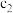
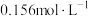 (均填“≥”“≤”或“=”)。
(均填“≥”“≤”或“=”)。(3)求0~60s以不同物质表示的化学反应速率之比
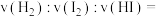
(4)一定温度下的密闭容器中,判断该可逆反应达到平衡状态的标志是_______。
A. 和 和 浓度相等 浓度相等 | B.反应容器内总质量不随时间变化 |
C. 百分含量保持不变 百分含量保持不变 | D.单位时间内生成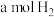 同时生成 同时生成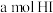 |
2023高一·全国·专题练习 查看更多[1]
(已下线)第6章 化学反应速率和化学平衡 6.2 化学平衡
更新时间:2023-03-13 16:06:21
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示 已知A、B、C均为气体
已知A、B、C均为气体 。
。
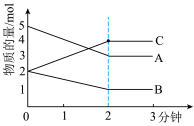
(1)该反应的化学方程式为_______________ 。
(2)反应开始至2分钟时,B的平均反应速率为_______________ 。
(3)能说明该反应已达到平衡状态的是_______________ 。
A.v(A)=2v(B)
B.容器内气体密度不变
C.v逆(A)=v正(C)
D.各组分的物质的量相等
E. 混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为_______________ 。
(5)下表是该小组研究影响过氧化氢H2O2分解速率的因素时采集的一组数据:用 制取
制取 所需的时间
所需的时间 秒
秒
①该研究小组在设计方案时。考虑了浓度、_______________ 、_______________ 等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?_______________ 。
(6)将质量相同但聚集状态不同的 分别加入到5mL5%的双氧水中,并用带火星的木条测试。测定结果如下:
分别加入到5mL5%的双氧水中,并用带火星的木条测试。测定结果如下:
①写出 发生分解的化学反应方程式
发生分解的化学反应方程式_______________ 。
②实验结果说明催化剂作用的大小与_______________ 有关。
 已知A、B、C均为气体
已知A、B、C均为气体 。
。 
(1)该反应的化学方程式为
(2)反应开始至2分钟时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是
A.v(A)=2v(B)
B.容器内气体密度不变
C.v逆(A)=v正(C)
D.各组分的物质的量相等
E. 混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为
(5)下表是该小组研究影响过氧化氢H2O2分解速率的因素时采集的一组数据:用
 制取
制取 所需的时间
所需的时间 秒
秒
| 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 | |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360s | 480s | 540s | 720s |
| MnO2催化剂、加热 | 10s | 25s | 60s | 120s |
①该研究小组在设计方案时。考虑了浓度、
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?
(6)将质量相同但聚集状态不同的
 分别加入到5mL5%的双氧水中,并用带火星的木条测试。测定结果如下:
分别加入到5mL5%的双氧水中,并用带火星的木条测试。测定结果如下:催化剂 | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3.5分钟 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
①写出
 发生分解的化学反应方程式
发生分解的化学反应方程式②实验结果说明催化剂作用的大小与
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反应速率并探究其影响因素的实验。(已知:在酸性条件下 会分解产生刺激性气味气体和淡黄色沉淀。)
会分解产生刺激性气味气体和淡黄色沉淀。)
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。
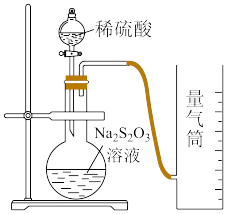
(1)除如图装置所示的实验用品外,还需要的一件实验用品是_______ 。
(2) 中的两个硫的化合价并不相同,假如其中一个硫的化合价为+4,则另一个硫的化合价为
中的两个硫的化合价并不相同,假如其中一个硫的化合价为+4,则另一个硫的化合价为_______ ;圆底烧瓶中所发生反应的离子方程式为_______ 。
(3)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内 的反应速率为
的反应速率为_______ (设圆底烧瓶内混合溶液的总体积为100ml,且反应过程中体积不变),而该测定值比实际值偏小,其原因可能是:_______ 。
(4)利用该化学反应,试简述测定反应速率的其他方法:_______ (写一种)。
Ⅱ.探究化学反应速率的影响因素
为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。(已知 ,
, 与
与 均为无色)
均为无色)
(5)表中Vx= _______ mL,t1、t2、t3的大小关系是_______ 。
 会分解产生刺激性气味气体和淡黄色沉淀。)
会分解产生刺激性气味气体和淡黄色沉淀。)Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。

(1)除如图装置所示的实验用品外,还需要的一件实验用品是
(2)
 中的两个硫的化合价并不相同,假如其中一个硫的化合价为+4,则另一个硫的化合价为
中的两个硫的化合价并不相同,假如其中一个硫的化合价为+4,则另一个硫的化合价为(3)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内
 的反应速率为
的反应速率为(4)利用该化学反应,试简述测定反应速率的其他方法:
Ⅱ.探究化学反应速率的影响因素
为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。(已知
 ,
, 与
与 均为无色)
均为无色)| 实验序号 | 体积V/mL | 蓝色褪去时间/s | |||
0.02mol/L 溶液 溶液 | 淀粉溶液 | 0.01mol/L碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大_______ ,原因是_______ 。
(2)哪一段时段的反应速率最小_______ ,原因是_______ 。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,直接写计算结果)_______ 。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)_______ 。
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)哪一段时段的反应速率最小
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,直接写计算结果)
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)
您最近一年使用:0次
【推荐1】某温度时,在一个2L恒容密闭容器中,X、Y、Z三种气体其物质的量随时间的变化曲线如图所示。

(1)该反应的化学方程式为___________
(2)将等物质的最的A和B,混合于2L的恒容密闭容器中,发生如下反应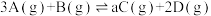 ,5min末,测得D的物质的量为1mol,
,5min末,测得D的物质的量为1mol,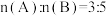 ,C的化学反应速率是
,C的化学反应速率是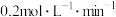 ,A的转化率是
,A的转化率是___________ ,a的值是___________ 。
(3)该条件下,能说明(2)中的可逆反应达到化学平衡状态的是___________ (填标号)
A.混合气体的平均相对分子质量不再改变
B.容器内压强不再改变
C.A、B、C、D四种气体的物质的量浓度相等
D.混合气体的密度不再改变
E.单位时间内消耗2molD,同时消耗1molB
F.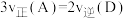

(1)该反应的化学方程式为
(2)将等物质的最的A和B,混合于2L的恒容密闭容器中,发生如下反应
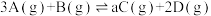 ,5min末,测得D的物质的量为1mol,
,5min末,测得D的物质的量为1mol,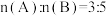 ,C的化学反应速率是
,C的化学反应速率是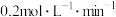 ,A的转化率是
,A的转化率是(3)该条件下,能说明(2)中的可逆反应达到化学平衡状态的是
A.混合气体的平均相对分子质量不再改变
B.容器内压强不再改变
C.A、B、C、D四种气体的物质的量浓度相等
D.混合气体的密度不再改变
E.单位时间内消耗2molD,同时消耗1molB
F.
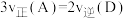
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】I.如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图像回答问题:
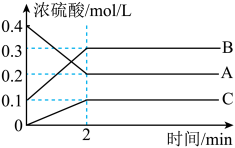
(1)2min内,用C表示的反应速率为______________ 。
(2)该反应的方程式为______________ 。
(3)在其他条件下,测得A的反应速率为0.05 mol/(L·s),此时的反应与800℃时相比,________ 。
A.比800℃ 时快 B.比800℃ 时慢 C.和800℃ 时速率一样
Ⅱ.学习小组甲利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如表实验:
(4)通过实验A、B,可探究出___________ (填外部因素)的改变对化学反应速率的影响,其中V1=_____ 、T1=_____ ;通过实验________ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=_______ ,t2_______ 8 (填写“=”、“>”或“<”)。
(5)若t1<8,则由此实验可以得出的结论是_______ 。

(1)2min内,用C表示的反应速率为
(2)该反应的方程式为
(3)在其他条件下,测得A的反应速率为0.05 mol/(L·s),此时的反应与800℃时相比,
A.比800℃ 时快 B.比800℃ 时慢 C.和800℃ 时速率一样
Ⅱ.学习小组甲利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如表实验:
实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(5)若t1<8,则由此实验可以得出的结论是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】甲醇(CH3OH)是一种无色液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
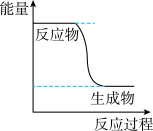
(1)已知:2CH3OH(g)+O2(g)⇌2CO2(g)+4H2(g)的能量变化如图所示,下列说法正确的是_____ 。(填字母)
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学反应不仅有新物质生成,同时也一定伴随能量变化
d.2mol甲醇和1mol氧气的总键能大于2mol二氧化碳和4mol氢气的总键能
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.4mol/L。则4min内平均反应速率v(H2)=_____ ,CH3OH的转化率为______ 。(转化率=某反应物转化浓度与该反应物起始浓度的百分比)
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、氧气和KOH溶液构成。该燃料电池的总反应为CH3OH+O2+KOH=K2CO3+H2O(未配平)。回答下列问题:
①该电池的正极反应物为______ 。
②负极的电极反应式为_____ 。
(1)已知:2CH3OH(g)+O2(g)⇌2CO2(g)+4H2(g)的能量变化如图所示,下列说法正确的是

a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学反应不仅有新物质生成,同时也一定伴随能量变化
d.2mol甲醇和1mol氧气的总键能大于2mol二氧化碳和4mol氢气的总键能
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.4mol/L。则4min内平均反应速率v(H2)=
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、氧气和KOH溶液构成。该燃料电池的总反应为CH3OH+O2+KOH=K2CO3+H2O(未配平)。回答下列问题:
①该电池的正极反应物为
②负极的电极反应式为
您最近一年使用:0次
【推荐1】二氧化碳、甲烷是地球大气中的主要温室气体,它们能吸收地面反射的太阳辐射,使地球表面变暖,因此,对二氧化碳、甲烷的高效利用有着举足轻重的作用。回答下列问题:
(1)已知下列反应
①CH4(g)+H2O(g) CO(g)+3H2(g) △H1
CO(g)+3H2(g) △H1
②CO(g)+H2O(g) CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2
则二氧化碳重整甲烷反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)△H3=
2CO(g)+2H2(g)△H3=_______ 。
(2)恒温恒容密闭容器中,反应CH4(g)+CO2(g) 2CO(g)+2H2(g)达到平衡状态的标志是
2CO(g)+2H2(g)达到平衡状态的标志是_________ 。
A.容器内的压强保持不变
B.c(CH4):c(CO2):c(CO):c(H2)=1:1:2:2
C.混合气体的平均分子量保持不变
D.混合气体的颜色保持不变
E.单位时间内断裂C-H键和形成H-H键的数目之比为2:1
(3)反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的平衡常数的表达式为
2CO(g)+2H2(g)的平衡常数的表达式为__________ 。
(4)T℃时,向恒容密闭容器中投入CH4和CO2各1mol,发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):
2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):
①在0~20min内,平均反应速率v(CO)=_________ kPa/min。
②若在恒温恒压密闭容器中进行上述反应,CH4的转化率将_________ (填增大、减小、不变)。
(1)已知下列反应
①CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1
CO(g)+3H2(g) △H1②CO(g)+H2O(g)
 CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2则二氧化碳重整甲烷反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g)△H3=
2CO(g)+2H2(g)△H3=(2)恒温恒容密闭容器中,反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)达到平衡状态的标志是
2CO(g)+2H2(g)达到平衡状态的标志是A.容器内的压强保持不变
B.c(CH4):c(CO2):c(CO):c(H2)=1:1:2:2
C.混合气体的平均分子量保持不变
D.混合气体的颜色保持不变
E.单位时间内断裂C-H键和形成H-H键的数目之比为2:1
(3)反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的平衡常数的表达式为
2CO(g)+2H2(g)的平衡常数的表达式为(4)T℃时,向恒容密闭容器中投入CH4和CO2各1mol,发生反应CH4(g)+CO2(g)
 2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):
2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):| 时间/min | 0 | 10 | 20 | 30 | 50 | 60 |
| 总压/kPa | 100 | 118 | 132 | 141 | 148 | 148 |
②若在恒温恒压密闭容器中进行上述反应,CH4的转化率将
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】化学链燃烧是利用载氧体将空气中的氧传输至燃料的新技术,基于CuO/ 载氧体的丙烷化学链燃烧技术原理如图所示。
载氧体的丙烷化学链燃烧技术原理如图所示。
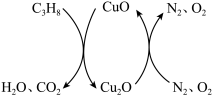
空气反应器与燃料反应器中发生的反应分别如下:
反应1: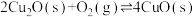
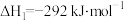
反应2: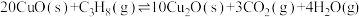
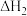
反应3: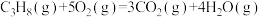
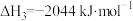
请回答下列问题:
(1)反应1在_______ (填“高温”、“低温”或“任意温度”)下能自发。
(2)一定温度下,在容积可变的密闭容器中加入足量 (s)和适量的
(s)和适量的 发生反应1。
发生反应1。
①当 的质量不变时,
的质量不变时,_______ (填“能”或“不能”)说明该反应达到平衡状态。
②若达到平衡之后,保持恒温恒容条件下再充入少量 ,达到新平衡之后
,达到新平衡之后 的平衡转化率
的平衡转化率_______ (填“增大”、“减小”或“不变”)。
(3)在一定温度下,总压强恒定为68kPa,在密闭容器中加入丙烷和氮气的混合气体以及足量CuO(s),只发生上述反应2(氮气不参与反应),测得丙烷的平衡转化率与投料比[ ]的关系如图所示:
]的关系如图所示:
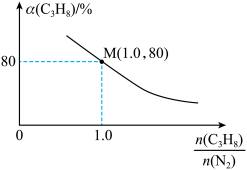
在上述温度下,平衡常数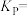
_______  (以分压表示,列出计算式即可,分压=总压×物质的量分数)。
(以分压表示,列出计算式即可,分压=总压×物质的量分数)。
 载氧体的丙烷化学链燃烧技术原理如图所示。
载氧体的丙烷化学链燃烧技术原理如图所示。
空气反应器与燃料反应器中发生的反应分别如下:
反应1:
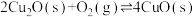
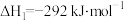
反应2:
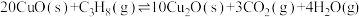
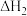
反应3:
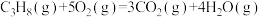
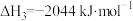
请回答下列问题:
(1)反应1在
(2)一定温度下,在容积可变的密闭容器中加入足量
 (s)和适量的
(s)和适量的 发生反应1。
发生反应1。①当
 的质量不变时,
的质量不变时,②若达到平衡之后,保持恒温恒容条件下再充入少量
 ,达到新平衡之后
,达到新平衡之后 的平衡转化率
的平衡转化率(3)在一定温度下,总压强恒定为68kPa,在密闭容器中加入丙烷和氮气的混合气体以及足量CuO(s),只发生上述反应2(氮气不参与反应),测得丙烷的平衡转化率与投料比[
 ]的关系如图所示:
]的关系如图所示:
在上述温度下,平衡常数
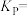
 (以分压表示,列出计算式即可,分压=总压×物质的量分数)。
(以分压表示,列出计算式即可,分压=总压×物质的量分数)。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】在化学研究和工业生产中,我们不仅关注化学反应中的物质变化和能量变化,还需要关注化学反应的快慢和进行的程度等。
(1)断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表:
进行反应 ,当生成
,当生成 时,将
时,将___________ (填“吸收”或“放出”)___________ kJ的能量。
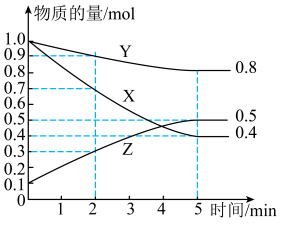
(2)在体积为5L的恒温密闭容器中,气体X、Y、Z物质的量随时间变化关系曲线如下图所示。
①该反应的化学方程式为:___________ 。
②0-2min内Z的化学反应速率为:___________ 。
③2min时的 与5min时的
与5min时的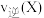 的大小关系为:
的大小关系为:
___________ 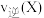 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
④下列描述能表示该反应达平衡状态的是___________ 。
A.Z的体积分数不再改变
B.容器内气体压强不再发生变化
C.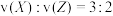
D.容器内混合气体的密度不再发生变化
E.容器内混合气体的平均相对分子质量不再发生变化
(1)断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表:
| 共价键 |  |  |  |
能量变化/( ) ) | 436.0 | 390.8 | 946.0 |
进行反应
 ,当生成
,当生成 时,将
时,将(2)在体积为5L的恒温密闭容器中,气体X、Y、Z物质的量随时间变化关系曲线如下图所示。

①该反应的化学方程式为:
②0-2min内Z的化学反应速率为:
③2min时的
 与5min时的
与5min时的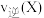 的大小关系为:
的大小关系为:
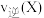 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。④下列描述能表示该反应达平衡状态的是
A.Z的体积分数不再改变
B.容器内气体压强不再发生变化
C.
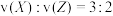
D.容器内混合气体的密度不再发生变化
E.容器内混合气体的平均相对分子质量不再发生变化
您最近一年使用:0次



