周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,其次外层所有轨道均是全满状态。回答下列问题:
(1)b、c、d的简单离子半径最大的是___________ (填离子符号),e的晶胞结构中e配位数为___________ 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的电子式为___________ ;分子中既含有极性共价键、又含有非极性共价键的化合物是___________ (填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是___________ (任写一种);酸根呈三角锥结构的酸是___________ (填化学式)。
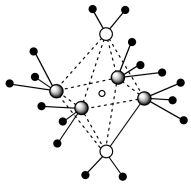
(4)e和c形成的一种离子化合物的晶体结构如图所示,则e离子的电荷为___________ 。

(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构。该化合物中,阴离子为___________ ,阳离子中存在的化学键类型有___________ 。
(1)b、c、d的简单离子半径最大的是
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的电子式为
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是
(4)e和c形成的一种离子化合物的晶体结构如图所示,则e离子的电荷为

(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构。该化合物中,阴离子为

更新时间:2023-03-22 11:06:56
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】甲、乙、丙、丁四种短周期元素的位置如图所示(其中乙、丙、丁的位置未标出)。

已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等。
(1)甲元素在周期表中的位置为______________ 。
(2)丙、丁可形成AB2型化合物,其结构式为________ 。
(3)丙是自然界中形成化合物种类最多的元素,其单质与甲元素的最高价氧化物对应水化物的浓溶液共热时反应的化学方程式是______________________ 。
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,写出这些化合物中任意两种符合以下条件的化学式_______________ ,________________________ 。(①原子个数比为1∶2;②分子中价电子总数为偶数)。

已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等。
(1)甲元素在周期表中的位置为
(2)丙、丁可形成AB2型化合物,其结构式为
(3)丙是自然界中形成化合物种类最多的元素,其单质与甲元素的最高价氧化物对应水化物的浓溶液共热时反应的化学方程式是
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,写出这些化合物中任意两种符合以下条件的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E为原子序数依次增大的5种短周期主族元素,其中仅含有一种金属元素,A单质是自然界中密度最小的气体,A和D最外层电子数相同;B原子的最外层电子数是次外层电子数的两倍; C和E在周期表中相邻,且E的质子数是C的2倍。请回答下列问题:
(1)B在元素周期表中的位置是_____________________ ;
(2)E的离子结构示意图是_____ ;DA中含有_______ ;(填化学键类型)
(3)BC2的电子式为________ ;(用具体元素表示,下同)
(4)C、D、E三种元素简单离子的离子半径由大到小的顺序是______________________ ;
(5)C和E形成氢化物的稳定性关系是__________________ ;为证明E最高价氧化物对应水化物酸性强于B时发生的化学反应方程式为______________________________________ 。
(1)B在元素周期表中的位置是
(2)E的离子结构示意图是
(3)BC2的电子式为
(4)C、D、E三种元素简单离子的离子半径由大到小的顺序是
(5)C和E形成氢化物的稳定性关系是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z是同周期的短周期元素,原子序数依次增大。Y为地壳中含量最高的金属元素,Z是所在周期中非金属最强的元素,X、Y的最高价氧化物对应的水化物可以相互反应。
(1)Y元素的原子结构示意图是_________________ 。
(2)X、Z最高价氧化物对应的水化物之间发生反应的离子方程式为______________ 。
(3)Z、碳和氟三种元素可组成氟利昂(CZ3F),它在紫外线作用下破坏臭氧层的反应过程部如下:
①CZ3F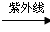 CZ2F·+Z·
CZ2F·+Z·
②Z·+O3 O2+ZO·
O2+ZO·
③ ZO·+O· Z·+O2
Z·+O2
反应①中破坏的化学键属于________ (填“极性”或“非极性”)共价键。
(4)下列说法正确的是___________ (填字母)。
a.X与氧元素可形成碱性氧化物
b.常温下与水反应的难易程度可证明金属性:X>Y
c.X、Y、Z形成的简单离子的核外电子排布均相同
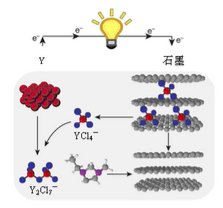
(5)Y、石墨与含YCl4-的离子液体可构成原电池,其工作原理如图所示。若电路中转移电子的物质的量为4. 5 mol,则消耗Y单质的质量是________ 。
(1)Y元素的原子结构示意图是
(2)X、Z最高价氧化物对应的水化物之间发生反应的离子方程式为
(3)Z、碳和氟三种元素可组成氟利昂(CZ3F),它在紫外线作用下破坏臭氧层的反应过程部如下:
①CZ3F
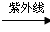 CZ2F·+Z·
CZ2F·+Z·②Z·+O3
 O2+ZO·
O2+ZO·③ ZO·+O·
 Z·+O2
Z·+O2反应①中破坏的化学键属于
(4)下列说法正确的是
a.X与氧元素可形成碱性氧化物
b.常温下与水反应的难易程度可证明金属性:X>Y
c.X、Y、Z形成的简单离子的核外电子排布均相同
(5)Y、石墨与含YCl4-的离子液体可构成原电池,其工作原理如图所示。若电路中转移电子的物质的量为4. 5 mol,则消耗Y单质的质量是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】元素周期表的一部分如图, 代表对应的元素,回答下列问题:
代表对应的元素,回答下列问题:_____ ,元素I在周期表中的位置为_____ 。
(2)D、E和J三种元素的离子半径由大到小的顺序是_____ (用离子符号表示)。
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是_____ (填物质名称)。
(4)A、C和J三种元素能形成多种化合物,其中酸性最强的化合物的化学式是_____ 。
(5)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为_____ 。
(6)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_____(填字母)。
 代表对应的元素,回答下列问题:
代表对应的元素,回答下列问题:
(2)D、E和J三种元素的离子半径由大到小的顺序是
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是
(4)A、C和J三种元素能形成多种化合物,其中酸性最强的化合物的化学式是
(5)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为
(6)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_____(填字母)。

| A.若a、b、c表示第ⅦA族元素,则X表示对应气态氢化物的沸点 |
| B.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| C.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
| D.若a、b、c表示第ⅦA族元素,则X表示对应简单离子的还原性 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】部分中学化学常见元素原子结构及性质如下表所示。
(1)这五种元素的原子半径由大到小的顺序为_______________ (用元素符号表示)。
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方案为________ 。E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,M中共用电子对对数为_______________ ,N的结构式为_______________ 。
(3)A与C可以形成一种新型陶瓷材料,机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是_______________ 。
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发此种陶瓷的全陶发动机替代同类型金属发动机
D.此种陶瓷的开发受到资源的限制,没有发展前途
| 序号 | 元素 | 结构及性质 |
| ① | A | A为地壳中含量仅次于氧的非金属元素,其单质晶体结构与金刚石相似 |
| ② | B | B原子最外层电子数是内层电子总数的1/5 |
| ③ | C | C是常用化肥的主要元素,单质常温下呈气态 |
| ④ | D | 通常情况下,D在化合物中显负价,A、B、C都能与D形成中学常见化合物 |
| ⑤ | E | E是宇宙中最丰富的元素 |
(1)这五种元素的原子半径由大到小的顺序为
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方案为
(3)A与C可以形成一种新型陶瓷材料,机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发此种陶瓷的全陶发动机替代同类型金属发动机
D.此种陶瓷的开发受到资源的限制,没有发展前途
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期律和周期表有力地论证了事物变化中量变引起质变的规律性,以及结构决定性质的化学观念.随着原子序数的递增,七种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示,请回答下列问题:

(1)元素B位于周期表中的第________ 周期第_______ 族.
(2)D、E、F三种元素对应的简单离子半径由大到小的顺序为________ (用元素的离子符号表示).
(3)用电子式表示G的氢化物的形成过程_______________________ .
(4)元素A与C形成的电子总数为22的分子的结构式为_____________ .
(5)D的最高价氧化物的水化物与E的最高价氧化物反应的离子方程式为___________ .
(6)元素C与D按原子个数比1∶1形成的化合物所含的所有化学类型为___________ .
(7)下列有关物质性质的推断,正确的是__________ (填标号).
a.单质的氧化性: b.金属性:
b.金属性:
c.气态氢化物的稳定性: d.最高价氧化物的水化物酸性:
d.最高价氧化物的水化物酸性:

(1)元素B位于周期表中的第
(2)D、E、F三种元素对应的简单离子半径由大到小的顺序为
(3)用电子式表示G的氢化物的形成过程
(4)元素A与C形成的电子总数为22的分子的结构式为
(5)D的最高价氧化物的水化物与E的最高价氧化物反应的离子方程式为
(6)元素C与D按原子个数比1∶1形成的化合物所含的所有化学类型为
(7)下列有关物质性质的推断,正确的是
a.单质的氧化性:
 b.金属性:
b.金属性:
c.气态氢化物的稳定性:
 d.最高价氧化物的水化物酸性:
d.最高价氧化物的水化物酸性:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知X、Y、Z、R、W、Q六种元素中,X的原子序数为1;Y元素原子最外层电子数是内层电子总数的2倍;Z元素原子次外层电子数比其最外层电子数少4个;R元素原子最外层有1个电子,其阳离子与Z的阴离子原子核外电子总数相同;W元素原子K层和M层电子总数等于其L层电子数。请要求填空:
(1)Z元素形成的原子的结构示意图为___________ ;
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是___________ (填化学式);属于非电解质的是___________ (填一种物质的名称即可);
(3)现有标准状况下YZ和 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为___________ ;
(4)55.0g化合物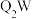 中含有
中含有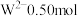 ,则Q的相对原子质量为
,则Q的相对原子质量为___________ ;
(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中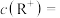
___________ ;
(6)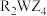 溶于水的电离方程式
溶于水的电离方程式___________ ;
(7)化合物 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(1)Z元素形成的原子的结构示意图为
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是
(3)现有标准状况下YZ和
 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为(4)55.0g化合物
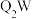 中含有
中含有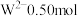 ,则Q的相对原子质量为
,则Q的相对原子质量为(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中
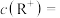
(6)
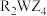 溶于水的电离方程式
溶于水的电离方程式(7)化合物
 与
与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知X、Y、Z、W、Q、R、E七种元素中,原子序数X<Y<Z<W<Q<R<E,其结构或性质信息如下表。
请根据信息回答有关问题:
(1)元素X的原子核外共有_______ 种不同运动状态的电子,有_______ 种不同能级的电子。
(2)Q的基态原子电子排布式为_______ ,R的元素符号为_______ ,E元素基态原子的价电子排布式为_______ 。
(3)含有元素W的盐的焰色试验为_______ 色,许多金属元素形成的盐都可以发生焰色试验,其原因是_______ 。
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数 |
| Y | 元素原子最外层电子排布式为nsnnpn+1 |
| Z | 单质在常温、常压下是气体,原子的M层上有1个未成对的p电子 |
| W | 元素的正一价离子的电子层结构与氩相同 |
| Q | 元素的核电荷数为Y和Z之和 |
| R | 元素的正三价离子的3d能级为半充满 |
| E | 元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
(1)元素X的原子核外共有
(2)Q的基态原子电子排布式为
(3)含有元素W的盐的焰色试验为
您最近一年使用:0次
【推荐3】现有A、B、C、D、E、F、G、H8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为
的电子式为________ 。(A、C为字母代号,请将字母代号用元素符号表示,下同)。
(2)B元素基态原子中能量最高的电子所占据的原子轨道呈________ 形。
(3)E元素基态原子的核外价电子轨道表示式为________ ,该元素的 远远大于
远远大于 ,其原因是
,其原因是________ 。
(4)D、E、F三种元素的简单离子半径由大到小的顺序是________________ 。
(5)G的最高价氧化物对应的水化物与E的氧化物反应的离子方程式________________________ 。
(6)H位于元素周期表中________ 区(按电子排布分区)。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素是形成化合物种类最多的元素 |
| C元素基态原子的核外p能级电子数比s能级电子数少1 |
| D元素基态原子的核外p轨道中有两个未成对电子 |
E元素的气态基态原子的第一至第四电离能分别是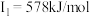 , ,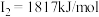 , ,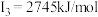 , ,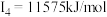 |
| F元素的主族序数与周期数的差为4 |
| G元素是前四周期中电负性最小的元素 |
| H元素位于元素周期表中的第8列 |
 的电子式为
的电子式为(2)B元素基态原子中能量最高的电子所占据的原子轨道呈
(3)E元素基态原子的核外价电子轨道表示式为
 远远大于
远远大于 ,其原因是
,其原因是(4)D、E、F三种元素的简单离子半径由大到小的顺序是
(5)G的最高价氧化物对应的水化物与E的氧化物反应的离子方程式
(6)H位于元素周期表中
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】地壳中含量排在前五位的元素分别是O、Si、Al、Fe、Ca,占到地壳总质量的90.83%。回答下列问题:
(1)Ca元素的基态原子价电子排布式为_______ 。
(2)“棕色环”现象是检验溶液中 的一种方法。向含有
的一种方法。向含有 溶液的试管中加入
溶液的试管中加入 ,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[
,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[ 。
。
① 中N元素采取
中N元素采取_______ 杂化,其立体构型为_______ (填名称)。
② 中含有的作用力类型有
中含有的作用力类型有_______ (填字母序号)。
a.离子键 b.金属键 c.非极性键 d.极性键 e.配位键
③ 中一种配体实际上是
中一种配体实际上是 ,则其中Fe元素的化合价为
,则其中Fe元素的化合价为_______ ;写出 的一种等电子体的化学式
的一种等电子体的化学式_______ 。
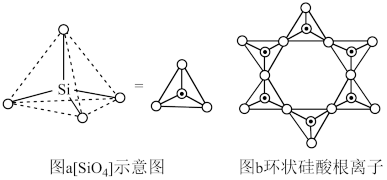
(3)硅酸盐中的硅酸根通常以[SiO4]四面体(如图a)的方式形成链状、环状或网络状复杂阴离子。图b为一种环状硅酸根离子,写出其化学式_______ 。
(1)Ca元素的基态原子价电子排布式为
(2)“棕色环”现象是检验溶液中
 的一种方法。向含有
的一种方法。向含有 溶液的试管中加入
溶液的试管中加入 ,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[
,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[ 。
。①
 中N元素采取
中N元素采取②
 中含有的作用力类型有
中含有的作用力类型有a.离子键 b.金属键 c.非极性键 d.极性键 e.配位键
③
 中一种配体实际上是
中一种配体实际上是 ,则其中Fe元素的化合价为
,则其中Fe元素的化合价为 的一种等电子体的化学式
的一种等电子体的化学式(3)硅酸盐中的硅酸根通常以[SiO4]四面体(如图a)的方式形成链状、环状或网络状复杂阴离子。图b为一种环状硅酸根离子,写出其化学式

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】化学在治理空气污染方面发挥着重要的作用,将污染气体吸收或转化为对环境友好的气体是环境科学研究的热点。
Ⅰ、工业制硫酸中尾气SO2的处理。
1.SO2分子的空间结构为_____ ;SO2的键角_____ H2O(选填“>”或“<”)
2.下图是工业制硫酸中的转化器,有关说法正确的是_____。(不定项)
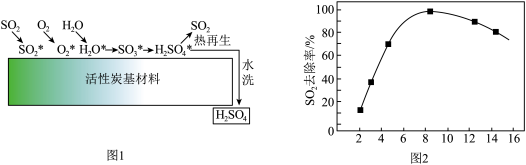
利用活性炭催化可去除尾气中SO2,并使其“热再生”,机理如下图1(*代表吸附态)。_____ 。
Ⅱ、N2O的转化
在Fe+催化作用下与CO发生反应:N2O(g)+CO(g) N2(g)+CO2(g)
N2(g)+CO2(g)
4.该反应分两步进行,第一步:Fe++N2O FeO++N2,则第二步反应为
FeO++N2,则第二步反应为_____ 。已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能_____ (选填“>”“<”或“=”)第二步反应的活化能。
Ⅰ、工业制硫酸中尾气SO2的处理。
1.SO2分子的空间结构为
2.下图是工业制硫酸中的转化器,有关说法正确的是_____。(不定项)
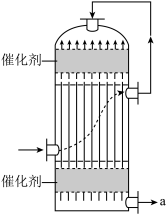
| A.该装置能充分利用热能 |
| B.进入转化器气体要净化操作 |
| C.温度475℃,此时SO2转化率最大 |
| D.该装置a端出来的气体只有SO3 |
利用活性炭催化可去除尾气中SO2,并使其“热再生”,机理如下图1(*代表吸附态)。
Ⅱ、N2O的转化
在Fe+催化作用下与CO发生反应:N2O(g)+CO(g)
 N2(g)+CO2(g)
N2(g)+CO2(g)4.该反应分两步进行,第一步:Fe++N2O
 FeO++N2,则第二步反应为
FeO++N2,则第二步反应为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】钛酸钡具有优良的介电、压电特性,主要用于电容器、自动温控等领域。
(1)钛元素在周期表中的位置______ ;基态钛原子的电子排布式为______ 。
(2)钡元素在自然界中主要以重晶石形式存在,其成分为BaSO4,其中所含三种元素的电负性从大到小的顺序为______ (用元素符号表示);SO 的空间构型为
的空间构型为______ ,其中S原子的杂化方式为______ 。
(3)卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示,已知TiF4的晶体类型与TiCl4、TiBr4、TiI4不同,下列判断不正确的是______ (选填字母序号)。

a.NaX均为离子晶体
b.随X半径的增大,NaX的离子键减弱,熔点逐渐降低
c.TiF4的熔点反常升高是由于氢键的作用
d.TiCl4、TiBr4、TiI4的相对分子质量依次增大,分子间作用力增大,熔点逐渐升高
(4)钛酸钡的晶胞结构如图所示,在该晶胞结构中,钛离子、钡离子、氧离子的个数比为______ ;该物质的化学式为______ ;晶体中每个钡离子周围与其距离最近且相等的氧离子的数量是______ ;其晶胞参数约为apm,钛酸钡晶体的密度ρ=______ g·cm-3(设阿伏加德罗常数的值为NA,用含a、NA的代数式表示)。

(1)钛元素在周期表中的位置
(2)钡元素在自然界中主要以重晶石形式存在,其成分为BaSO4,其中所含三种元素的电负性从大到小的顺序为
 的空间构型为
的空间构型为(3)卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示,已知TiF4的晶体类型与TiCl4、TiBr4、TiI4不同,下列判断不正确的是

a.NaX均为离子晶体
b.随X半径的增大,NaX的离子键减弱,熔点逐渐降低
c.TiF4的熔点反常升高是由于氢键的作用
d.TiCl4、TiBr4、TiI4的相对分子质量依次增大,分子间作用力增大,熔点逐渐升高
(4)钛酸钡的晶胞结构如图所示,在该晶胞结构中,钛离子、钡离子、氧离子的个数比为

您最近一年使用:0次



