现有A、B、C、D、E、F、G、H8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为
的电子式为________ 。(A、C为字母代号,请将字母代号用元素符号表示,下同)。
(2)B元素基态原子中能量最高的电子所占据的原子轨道呈________ 形。
(3)E元素基态原子的核外价电子轨道表示式为________ ,该元素的 远远大于
远远大于 ,其原因是
,其原因是________ 。
(4)D、E、F三种元素的简单离子半径由大到小的顺序是________________ 。
(5)G的最高价氧化物对应的水化物与E的氧化物反应的离子方程式________________________ 。
(6)H位于元素周期表中________ 区(按电子排布分区)。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素是形成化合物种类最多的元素 |
| C元素基态原子的核外p能级电子数比s能级电子数少1 |
| D元素基态原子的核外p轨道中有两个未成对电子 |
E元素的气态基态原子的第一至第四电离能分别是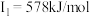 , ,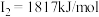 , ,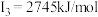 , ,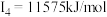 |
| F元素的主族序数与周期数的差为4 |
| G元素是前四周期中电负性最小的元素 |
| H元素位于元素周期表中的第8列 |
 的电子式为
的电子式为(2)B元素基态原子中能量最高的电子所占据的原子轨道呈
(3)E元素基态原子的核外价电子轨道表示式为
 远远大于
远远大于 ,其原因是
,其原因是(4)D、E、F三种元素的简单离子半径由大到小的顺序是
(5)G的最高价氧化物对应的水化物与E的氧化物反应的离子方程式
(6)H位于元素周期表中
更新时间:2024-04-04 02:41:45
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分,表中列出12种元素在周期表中的位置,按要求回答下列问题。
(1)在这12种元素中,化学性质最不活泼的元素名称是______ ,得电子能力最强的原子是_____ (用元素符号表示);元素⑦的最高价氧化物对应的水化物是_____ (写化学式)。
(2)元素④的离子结构示意图为__________ 。③与⑧形成的化合物的电子式:_______ 。
(3)①⑧⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示)______ 。
(4)请写出:
(ⅰ) ③的单质置换出⑥的单质的化学方程式:_________________________ 。
(ⅱ) ⑤和(11)两种元素最高价氧化物对应的水化物相互反应的离子方程式为___________ 。
(ⅲ)元素⑨的单质和元素①的最高价氧化物对应的水化物常温下反应的化学方程式为__ 。
| 周期\族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | (11) | ⑧ | ⑩ | ||||
| 三 | ① | ③ | ⑤ | ⑦ | (12) | ⑨ | ||
| 四 | ② | ④ |
(2)元素④的离子结构示意图为
(3)①⑧⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示)
(4)请写出:
(ⅰ) ③的单质置换出⑥的单质的化学方程式:
(ⅱ) ⑤和(11)两种元素最高价氧化物对应的水化物相互反应的离子方程式为
(ⅲ)元素⑨的单质和元素①的最高价氧化物对应的水化物常温下反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】a、b、c、d、e为五种短周期主族元素,原子序数依次递增。下图是a~e五种元素的单质及其化合物(或其溶液)的转化关系。已知A为金属单质,B、C、D是非金属单质,且在常温常压下都是气体,D常用于自来水的杀菌、消毒;化合物G的焰色试验呈黄色,化合物F通常状况下呈气态。请回答下列问题
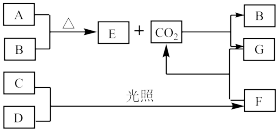
(1)d在元素周期表中的位置位于___________ ,CO2的电子式为___________ 。
(2)e的单质与d的最高价氧化物对应的水化物反应的化学方程式是___________ 。
(3)Na2O2可在呼吸面具中作为氧气来源,假设每人每分钟消耗0.448LO2(标准状况),且所需的O2全部由Na2O2来提供,则某消防员工作1小时所需Na2O2的质量为___________ g
(4)b、c、d元素中,原子半径由小到大的顺序是___________ (填元素符号);c、d、e元素分别形成的简单离子中离子半径最小的是___________ (填离子符号)。
(5)b和e两元素相比较,非金属性较强是___________ (填元素符号),可以证明该结论的是___________ 。
A.e的气态氢化物比b的气态氢化物稳定
B.b氧化物对应的水化物的酸性弱于e氧化物对应的水化物的酸性
C.b的简单氢化物的沸点比e的氢化物沸点低
D.b和e形成的化合物中的化合价b为正价,e为负价

(1)d在元素周期表中的位置位于
(2)e的单质与d的最高价氧化物对应的水化物反应的化学方程式是
(3)Na2O2可在呼吸面具中作为氧气来源,假设每人每分钟消耗0.448LO2(标准状况),且所需的O2全部由Na2O2来提供,则某消防员工作1小时所需Na2O2的质量为
(4)b、c、d元素中,原子半径由小到大的顺序是
(5)b和e两元素相比较,非金属性较强是
A.e的气态氢化物比b的气态氢化物稳定
B.b氧化物对应的水化物的酸性弱于e氧化物对应的水化物的酸性
C.b的简单氢化物的沸点比e的氢化物沸点低
D.b和e形成的化合物中的化合价b为正价,e为负价
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下图为元素周期表。

试完成下列问题:
(1)图中阴影部分所示区域的元素称为___________ 元素,下列元素属于该区域的是___________ (填字母)。
A.Ba B.Fe C.Br D.Rb
(2)已知A、B、C、D、E、F六种短周期元素的原子半径和某些化合价如下表:
试将D、F两种元素的元素符号填入上图所示元素周期表中的相应位置____ 。
(3)C的最高价氧化物与E的单质在点燃条件下发生反应的化学方程式为___________ ;由F的化合物生成A的单质的化学方程式为___________ 。
(4)C与氢元素可组成一种气体,该气体在标准状况下的密度为1.25 g·L-1,该气体的摩尔质量为___________ 。

试完成下列问题:
(1)图中阴影部分所示区域的元素称为
A.Ba B.Fe C.Br D.Rb
(2)已知A、B、C、D、E、F六种短周期元素的原子半径和某些化合价如下表:
| 元素 | A | B | C | D | E | F |
| 化合价 | -2 | +5、-3 | +4、-4 | +6、-2 | +2 | +1 |
| 原子半径/nm | 0.074 | 0.075 | 0.077 | 0.102 | 0.160 | 0.186 |
(3)C的最高价氧化物与E的单质在点燃条件下发生反应的化学方程式为
(4)C与氢元素可组成一种气体,该气体在标准状况下的密度为1.25 g·L-1,该气体的摩尔质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)________________ 。
(2)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有________________ 。
(3)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:_____________________ 。若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:_________________________ 。
(1)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(2)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有
(3)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为________ ;元素Y、Z、W的原子半径由大到小顺序为________ 。
(2)单质铜和元素Y的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为____________ 。
(3)元素W位于周期表的第_____ 周期第________ 族,其非金属性比R弱,用原子结构的知识解释原因:__________ 。元素W和R的气态氢化物的稳定性关系为:________ (写出化学式)。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的化学方程式:____________ 。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为____________ 。
(1)元素X的最高价氧化物的电子式为
(2)单质铜和元素Y的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为
(3)元素W位于周期表的第
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的化学方程式:
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同族,它们原子的最外层电子排布式为ns1。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。请回答下列问题:
(1)A是________ ,B是________ ,E是________ 。
(2)写出C元素基态原子的电子排布式:________________________ 。
(3)元素B与D的电负性的大小关系是B____________ (填“>”“<”或“=”,下同)D,E与C的第一电离能大小关系是E________ C。
(4)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式:_____________ 。
(1)A是
(2)写出C元素基态原子的电子排布式:
(3)元素B与D的电负性的大小关系是B
(4)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钛(Ti)被称为“未来金属”,其化合物广泛用于国防、电讯器材、医疗器械和化工设备等领域。回答下列问题:
(1)基态钛原子的价电子排布式为___________ ,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有___________ 种。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其它三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___________ 。
(3)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示:___________ 。
②请在图中标出配位键___________ (用“→”表示);
③配合物中非金属元素的含氧酸根的中心原子杂化轨道类型是sp2的是___________ 。
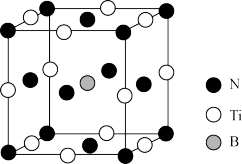
(4)用B掺杂TiN后(晶胞结构中只是B原子部分代替钛原子),其晶胞结构如图所示,距离Ti最近的B有___________ 个,Ti与B的最近距离为___________ nm;掺杂B后的晶体密度是TiN晶体的___________ 倍。(已知掺杂B后的晶体密度为ρg/cm3,阿伏加德罗常数的值为NA)
(1)基态钛原子的价电子排布式为
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其它三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示:

②请在图中标出配位键
③配合物中非金属元素的含氧酸根的中心原子杂化轨道类型是sp2的是
(4)用B掺杂TiN后(晶胞结构中只是B原子部分代替钛原子),其晶胞结构如图所示,距离Ti最近的B有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】废旧锡铬合金(含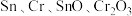 和少量Pb)。采用如下工艺流程回收锡并制备重铬酸钾
和少量Pb)。采用如下工艺流程回收锡并制备重铬酸钾 。
。

已知:①“熔融氧化”中,氧化产物为 ,还原产物为
,还原产物为 ;
;
② 。
。
回答下列问题:
(1)基态 原子核外有
原子核外有___________ 个未成对电子。
(2)“热溶”时发生的非氧化还原反应的离子方程式为___________ ;加快“热溶”速率的措施有___________ (任写2条)。
(3)“溶渣”的主要成分为___________ (填化学式)。
(4)“调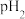 ”的作用是
”的作用是___________
(5)“熔融氧化”反应的化学方程式为___________ ,该操作可在___________ (填字母)中进行。
A.蒸发皿 B.铁坩埚 C.石英坩埚 D.烧杯
(6)“转化、分离”中,需要通过蒸发浓缩、降温至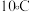 、结晶的方法分离得到
、结晶的方法分离得到 晶体的原因为
晶体的原因为___________ 。
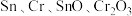 和少量Pb)。采用如下工艺流程回收锡并制备重铬酸钾
和少量Pb)。采用如下工艺流程回收锡并制备重铬酸钾 。
。
已知:①“熔融氧化”中,氧化产物为
 ,还原产物为
,还原产物为 ;
;②
 。
。回答下列问题:
(1)基态
 原子核外有
原子核外有(2)“热溶”时发生的非氧化还原反应的离子方程式为
(3)“溶渣”的主要成分为
(4)“调
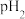 ”的作用是
”的作用是(5)“熔融氧化”反应的化学方程式为
A.蒸发皿 B.铁坩埚 C.石英坩埚 D.烧杯
(6)“转化、分离”中,需要通过蒸发浓缩、降温至
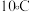 、结晶的方法分离得到
、结晶的方法分离得到 晶体的原因为
晶体的原因为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】a、b、c、d、e均为短周期主族元素,其中a与c的原子序数之和等于e的原子序数,上述五种元素的最外层电子数与原子半径的大小关系如图所示。请按要求回答下列问题:_______ (填元素符号),这些元素形成的酸性最强的最高价含氧酸和碱性最强的碱形成的盐是_______ (填化学式)。
(2)c、d、e三种元素可形成一种有毒气体 ,该气体分子的结构式为
,该气体分子的结构式为________ 。
(3)上述五种元素的基态原子中,未成对电子数为2的元素有________ (填元素符号)。
(4)基态b原子中有____ 种不同能量的电子;其基态 的核外电子占据的最高能级的电子云轮廓图呈
的核外电子占据的最高能级的电子云轮廓图呈_______ 形,该能级的轨道有_____ 个伸展方向。
(5)a元素的第二电离能____ (填“大于”或“小于”)b元素的第二电离能,原因是_____ 。
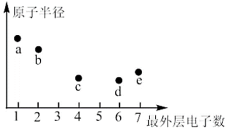
(2)c、d、e三种元素可形成一种有毒气体
 ,该气体分子的结构式为
,该气体分子的结构式为(3)上述五种元素的基态原子中,未成对电子数为2的元素有
(4)基态b原子中有
 的核外电子占据的最高能级的电子云轮廓图呈
的核外电子占据的最高能级的电子云轮廓图呈(5)a元素的第二电离能
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】第二代半导体材料——(Ⅲ−V)A族化合物的特殊性能使之成为科学家的研究热点之一。
(1)基态镓原子的价电子排布式为__ ,基态P原子的价电子排布图为___ 。
(2)NH4NO3中N的杂化方式为__ ;NH4NO3呈__ 性,原因是__ 。
(3)N、P、As位于同一主族,已知NH3的沸点比PH3的沸点高,AsH3的沸点比PH3的沸点高。产生的原因是__ 。
(4)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有__ 。
(5)磷化铝晶胞如图,若晶胞参数为dpm,NA代表阿伏加德罗常数的值,则磷化铝晶体的密度ρ=__ g/cm3。(用含d的表达式填空)

(1)基态镓原子的价电子排布式为
(2)NH4NO3中N的杂化方式为
(3)N、P、As位于同一主族,已知NH3的沸点比PH3的沸点高,AsH3的沸点比PH3的沸点高。产生的原因是
(4)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有
(5)磷化铝晶胞如图,若晶胞参数为dpm,NA代表阿伏加德罗常数的值,则磷化铝晶体的密度ρ=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】砷(As)及其化合物被广泛用在农药、除草剂、杀虫剂及合金中。请回答下列问题:
(1)基态砷原子核外电子的电子云有____ 种不同的伸展方向;下列关于基态砷原子的价电子排布图中表示正确的是_____ 。
A.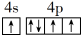 B.
B. C.
C.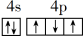 D.
D.
(2)锗(Ge)、砷(As)、硒(Se)三种元素的第一电离能从大到小的顺序为____ (用元素符号表示)。
(3)在相同条件下,AsH3的沸点高于PH3但低于NH3的原因为___________ 。
(4)砷的含氧酸有H3AsO3、H3AsO4、HAsO3等。
①HAsO3电离出的 的空间构型为
的空间构型为_____ ;写出两种与 互为等电子体的分子的化学式
互为等电子体的分子的化学式________ 。
②H3AsO3和H3AsO4中酸性较强的是______ ,原因是________________ 。
(5)砷和铟组成的一种化合物属于半导体材料,其晶胞结构如下图所示,则该化合物的化学式为_____ ;已知晶胞的参数为a pm,阿伏伽德罗常数的值为NA,则该晶体的密度为______ g·cm−3(用含a和NA的代数式表示)。

(1)基态砷原子核外电子的电子云有
A.
 B.
B. C.
C. D.
D.
(2)锗(Ge)、砷(As)、硒(Se)三种元素的第一电离能从大到小的顺序为
(3)在相同条件下,AsH3的沸点高于PH3但低于NH3的原因为
(4)砷的含氧酸有H3AsO3、H3AsO4、HAsO3等。
①HAsO3电离出的
 的空间构型为
的空间构型为 互为等电子体的分子的化学式
互为等电子体的分子的化学式②H3AsO3和H3AsO4中酸性较强的是
(5)砷和铟组成的一种化合物属于半导体材料,其晶胞结构如下图所示,则该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氯化钠是一种典型且极具魅力的晶体,我们通过学习氯化钠可以更好地了解其他类似物质的结构。已知氯化钠的晶胞如下图1所示。

图1
(1)下列关于氯化钠的说法正确的是_______。
(2)已知 的密度为
的密度为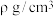 ,
, 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则在
,则在 晶体里
晶体里 和
和 的最短距离为
的最短距离为_______  。
。
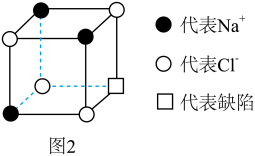
(3)温度升高时, 晶体出现缺陷,如图2所示,当图中方格内填入
晶体出现缺陷,如图2所示,当图中方格内填入 时,恰好构成氯化钠晶胞的1/8。
时,恰好构成氯化钠晶胞的1/8。 晶体出现缺陷时,其导电性大大增强,原因是
晶体出现缺陷时,其导电性大大增强,原因是_______ 。
(4) 、
、 的晶体类型与氯化钠相同,
的晶体类型与氯化钠相同, 和
和 的离子半径分别为
的离子半径分别为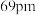 和
和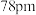 ,则熔点:
,则熔点:
_______  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(5)钡在氧气中燃烧时得到一种钡的氧化物 晶体,其阴阳离子的排布与氯化钠相同,其中存在的化学键的类型为
晶体,其阴阳离子的排布与氯化钠相同,其中存在的化学键的类型为_______ 。

图1
(1)下列关于氯化钠的说法正确的是_______。
A.基态 的电子有5种空间运动状态 的电子有5种空间运动状态 |
| B.钠是第一电离能最大的碱金属元素 |
C.氯原子的价电子排布式可写成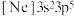 |
| D.每个氯离子周围与它最近且等距的氯离子有12个 |
 的密度为
的密度为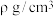 ,
, 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则在
,则在 晶体里
晶体里 和
和 的最短距离为
的最短距离为 。
。(3)温度升高时,
 晶体出现缺陷,如图2所示,当图中方格内填入
晶体出现缺陷,如图2所示,当图中方格内填入 时,恰好构成氯化钠晶胞的1/8。
时,恰好构成氯化钠晶胞的1/8。 晶体出现缺陷时,其导电性大大增强,原因是
晶体出现缺陷时,其导电性大大增强,原因是
(4)
 、
、 的晶体类型与氯化钠相同,
的晶体类型与氯化钠相同, 和
和 的离子半径分别为
的离子半径分别为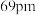 和
和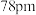 ,则熔点:
,则熔点:
 (填“>”“<”或“=”)
(填“>”“<”或“=”)(5)钡在氧气中燃烧时得到一种钡的氧化物
 晶体,其阴阳离子的排布与氯化钠相同,其中存在的化学键的类型为
晶体,其阴阳离子的排布与氯化钠相同,其中存在的化学键的类型为
您最近一年使用:0次



