铁元素是最重要的金属元素之一,很多含铁化合物具有重要作用。
(1)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。
①与N同周期的主族元素中,第一电离能比N大的元素是_______ 。
②[Fe(SCN)(H2O)5]2+中该配离子中配位体是_______ ,Fe3+的配位数为_______ 。
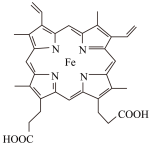
(2)血红素结构如图所示,在图中画出Fe2+与N原子间的化学键_______ (若是配位键,需要用箭头加以表示),血红素中C原子的杂化方式是_______ 。
(3)FeCO3可作补血剂,CoCO3可用于陶瓷工业的着色剂。已知:①r(Fe2+)为61pm,r(Co2+)为65pm。②隔绝空气加热:FeCO3 FeO+CO2↑,CoCO3
FeO+CO2↑,CoCO3 CoO+CO2↑分别加热FeCO3和CoCO3时,FeCO3的分解温度低于CoCO3,其原因是
CoO+CO2↑分别加热FeCO3和CoCO3时,FeCO3的分解温度低于CoCO3,其原因是_______ 。
(1)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。
①与N同周期的主族元素中,第一电离能比N大的元素是
②[Fe(SCN)(H2O)5]2+中该配离子中配位体是
(2)血红素结构如图所示,在图中画出Fe2+与N原子间的化学键

(3)FeCO3可作补血剂,CoCO3可用于陶瓷工业的着色剂。已知:①r(Fe2+)为61pm,r(Co2+)为65pm。②隔绝空气加热:FeCO3
 FeO+CO2↑,CoCO3
FeO+CO2↑,CoCO3 CoO+CO2↑分别加热FeCO3和CoCO3时,FeCO3的分解温度低于CoCO3,其原因是
CoO+CO2↑分别加热FeCO3和CoCO3时,FeCO3的分解温度低于CoCO3,其原因是
更新时间:2023-03-27 18:38:48
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氮族元素是指元素周期表中VA族的所有元素,包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)等元素,在农药、化肥等领域有广泛应用。回答下列问题:
(1)基态Bi的价电子排布图为_______ 。
(2)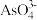 中和
中和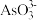 中
中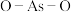 键角较大的是
键角较大的是_______ 。
(3)氮元素的常见含氧酸根为 ,其空间构型为
,其空间构型为_______ 。
(4) 和
和 可形成配离子
可形成配离子 ,该配离子中各元素的第一电离能由小到大的顺序为
,该配离子中各元素的第一电离能由小到大的顺序为_______ (用元素符号表示)。
(1)基态Bi的价电子排布图为
(2)
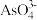 中和
中和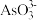 中
中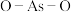 键角较大的是
键角较大的是(3)氮元素的常见含氧酸根为
 ,其空间构型为
,其空间构型为(4)
 和
和 可形成配离子
可形成配离子 ,该配离子中各元素的第一电离能由小到大的顺序为
,该配离子中各元素的第一电离能由小到大的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ti、Na、Mg、C、N、O、Fe等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ ,能量最低的是_______ (填序号)
a.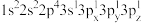 b.
b. c.
c. d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子核外共有_______ 种运动状态不同的电子,最高能层电子的电子云轮廓形状为_______ 。与Ti同周期的所有过渡元素的基态原子中,写出任意一种最外层电子数与钛不同的元素外围电子排布式_______ 。
(4)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是_______ ,判断理由是_______ 。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是_______ 。Fe3+与Fe2+的离子半径大小关系为:Fe3+_______ Fe2+(填“大于”或“小于”),原因为:_______ 。
(1)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
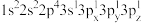 b.
b. c.
c. d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子核外共有
(4)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是
| 元素 | I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 |
| X | 737.7 | 1 450.7 | 7 732.7 |
| Y | 1 313.9 | 3 388.3 | 5 300.5 |
| Z | 1 402.3 | 2 856.0 | 4 578.1 |
您最近一年使用:0次
【推荐3】回答下列问题
(1)F元素的基态原子最外层电子排布式为nsnnpn+3,则n=___________ ;基态原子中能量最高的是___________ 电子,核外电子的轨道表示式为___________ 。
(2)硝酸和尿素( )的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原因:
)的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原因:___________ 。
(3)N、O、S的第一电离能(I1)由大到小的顺序为___________ ,原因是______________________ 。
(1)F元素的基态原子最外层电子排布式为nsnnpn+3,则n=
(2)硝酸和尿素(
 )的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原因:
)的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原因:(3)N、O、S的第一电离能(I1)由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】《上海市排水“十四五”规划》提出到“十四五”末期,新增污水处理规模约280万立方米/日。聚合氯化铝(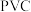 )是一种高效絮凝剂,广泛用于城市给排水净化。工业上制备
)是一种高效絮凝剂,广泛用于城市给排水净化。工业上制备 的一种方法:
的一种方法: 。
。
(1)上述反应所涉及的第二周期元素中,未成对电子数相等的元素有___________ ,能说明两者非金属性强弱的事实是___________ 。
(2)常压、180℃时, 升华形成的二聚体(
升华形成的二聚体( )的结构如图所示,试用“→”标出其中的配位键
)的结构如图所示,试用“→”标出其中的配位键___________ ,其杂化方式为___________ 。

(3)美国科学家宣布发现了铝的某种超原子结构( )具有40个价电子时处于相对稳定状态。请预测稳定的
)具有40个价电子时处于相对稳定状态。请预测稳定的 所带的电荷数为__________。
所带的电荷数为__________。
(4)铝的“超级原子”结构有 、
、 等。这类超级原子和
等。这类超级原子和 类似,最外层电子数为40时处于相对稳定状态,下列说法正确的是__________。
类似,最外层电子数为40时处于相对稳定状态,下列说法正确的是__________。
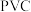 )是一种高效絮凝剂,广泛用于城市给排水净化。工业上制备
)是一种高效絮凝剂,广泛用于城市给排水净化。工业上制备 的一种方法:
的一种方法: 。
。(1)上述反应所涉及的第二周期元素中,未成对电子数相等的元素有
(2)常压、180℃时,
 升华形成的二聚体(
升华形成的二聚体( )的结构如图所示,试用“→”标出其中的配位键
)的结构如图所示,试用“→”标出其中的配位键
(3)美国科学家宣布发现了铝的某种超原子结构(
 )具有40个价电子时处于相对稳定状态。请预测稳定的
)具有40个价电子时处于相对稳定状态。请预测稳定的 所带的电荷数为__________。
所带的电荷数为__________。| A.-1 | B.+2 | C.0 | D.+3 |
(4)铝的“超级原子”结构有
 、
、 等。这类超级原子和
等。这类超级原子和 类似,最外层电子数为40时处于相对稳定状态,下列说法正确的是__________。
类似,最外层电子数为40时处于相对稳定状态,下列说法正确的是__________。A. 与盐酸反应的化学方程式可表示为: 与盐酸反应的化学方程式可表示为: |
B. 和 和 互为同位素 互为同位素 |
C. 和 和 都具有较强的还原性,容易失去电子生成阳离子 都具有较强的还原性,容易失去电子生成阳离子 |
D. 超原子中 超原子中 原子间通过离子键结合 原子间通过离子键结合 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】填空。
(1)工业上电解 制取单质铝,常利用冰晶石
制取单质铝,常利用冰晶石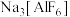 降低
降低 的熔点。冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在
的熔点。冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在_______ (填字母)。
a.离子键 b.极性键 c.配位键 d.范德华力
(2) 的晶体结构如下图所示,其中原子坐标参数A为
的晶体结构如下图所示,其中原子坐标参数A为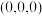 ,B为
,B为 ,则C原子坐标参数为
,则C原子坐标参数为_______ 。

(1)工业上电解
 制取单质铝,常利用冰晶石
制取单质铝,常利用冰晶石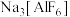 降低
降低 的熔点。冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在
的熔点。冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在a.离子键 b.极性键 c.配位键 d.范德华力
(2)
 的晶体结构如下图所示,其中原子坐标参数A为
的晶体结构如下图所示,其中原子坐标参数A为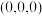 ,B为
,B为 ,则C原子坐标参数为
,则C原子坐标参数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的原子是________________ 。
(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内存在________ (填序号,下同)。
a.离子键 b.配位键 c.共价键
(3)向盛有硫酸铜溶液的试管中滴加氨水,先生成难溶物,继续滴加氨水,难溶物溶解,得到深蓝色透明溶液。下列对此现象的说法正确的是________ 。
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后,生成深蓝色的配离子[Cu(NH3)4]2+
C.[Cu(NH3)4]2+的立体结构为正四面体形
D.在[Cu(NH3)4]2+配离子中,Cu2+给出孤电子对,NH3提供空轨道
(4)向氯化铜溶液中加入过量浓氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]Cl2晶体,深蓝色晶体中含有的化学键除普通的共价键外,还有________ 和________ 。
(1)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的原子是
(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内存在
a.离子键 b.配位键 c.共价键
(3)向盛有硫酸铜溶液的试管中滴加氨水,先生成难溶物,继续滴加氨水,难溶物溶解,得到深蓝色透明溶液。下列对此现象的说法正确的是
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后,生成深蓝色的配离子[Cu(NH3)4]2+
C.[Cu(NH3)4]2+的立体结构为正四面体形
D.在[Cu(NH3)4]2+配离子中,Cu2+给出孤电子对,NH3提供空轨道
(4)向氯化铜溶液中加入过量浓氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]Cl2晶体,深蓝色晶体中含有的化学键除普通的共价键外,还有
您最近一年使用:0次



