在HF、H2O、NH3、CS2、CH4、H2O2、N2分子中:
(1)以非极性键结合的非极性分子是___________ (填化学式,下同)。
(2)以极性键结合,具有直线形结构的非极性分子是___________ 。
(3)以极性键结合,具有正四面体结构的非极性分子是___________ 。
(4)以极性键结合,具有三角锥形结构的极性分子是___________ 。
(5)含有非极性键的极性分子是___________ 。
(1)以非极性键结合的非极性分子是
(2)以极性键结合,具有直线形结构的非极性分子是
(3)以极性键结合,具有正四面体结构的非极性分子是
(4)以极性键结合,具有三角锥形结构的极性分子是
(5)含有非极性键的极性分子是
22-23高二下·贵州贵阳·阶段练习 查看更多[3]
更新时间:2023-03-27 21:24:25
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】现有下列物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)只由离子键构成的物质是__________________ (填序号,下同)。
(2)只由极性键构成的物质是__________________ 。
(3)由极性键和非极性键构成的物质是__________________ 。
(4)由离子键和极性键构成的物质是__________________ 。
(5)由离子键和非极性键构成的物质是__________________ 。
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)只由离子键构成的物质是
(2)只由极性键构成的物质是
(3)由极性键和非极性键构成的物质是
(4)由离子键和极性键构成的物质是
(5)由离子键和非极性键构成的物质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为____ 。元素Mn与O中,电负性较大的是___ ,基态原子核外未成对电子数较多的是____ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为____ 和____ 。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____ 。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在____ 。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】研究表明,利用FeCl2、NH4H2PO4、Li2CO3和苯胺( )制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
)制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
(1)Fe2+基态核外电子排布式为___________ 。
(2)N、P、O三种元素的电负性由大到小的顺序为___________ 。
(3)CO 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ 。
(4)1mol苯胺分子中含有σ键的数目为___________ ;苯胺与甲苯的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是___________ 。
 )制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
)制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。(1)Fe2+基态核外电子排布式为
(2)N、P、O三种元素的电负性由大到小的顺序为
(3)CO
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(4)1mol苯胺分子中含有σ键的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】按下列要求填空
(1)基态某原子的最外层电子排布式是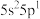 ,推断该元素位于第五周期第
,推断该元素位于第五周期第_______ 族,该元素的最高正化合价为_______ ,在元素周期表中属于_______ 区。
(2)基态某原子的价层电子排布式为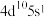 ,推断该元素位于第五周期第
,推断该元素位于第五周期第_______ 族,在元素周期表中属于_______ 区。
(3)比较大小(写>或<)
①键长:
________  ②键能:
②键能:
________ 
③键角:
________  ④键的极性:
④键的极性:
_______ 
⑤沸点:
________  ⑥熔点:
⑥熔点:
_______ 
(4)① 杂化类型为
杂化类型为_______ ,VSEPR模型为_______ ,分子空间构型为_______ 。
② 杂化类型为
杂化类型为_______ ,VSEPR模型为_______ ,离子空间构型为_______ 。
③ 杂化类型为
杂化类型为_______ ,VSEPR模型为_______ ,离子空间构型为_______ 。
(5)电子式:碳化钙( )
)_______ 。
(6)在空气中 稳定性小于
稳定性小于 ,从电子排布的角度分析,其主要原因
,从电子排布的角度分析,其主要原因_______ 。
(1)基态某原子的最外层电子排布式是
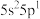 ,推断该元素位于第五周期第
,推断该元素位于第五周期第(2)基态某原子的价层电子排布式为
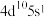 ,推断该元素位于第五周期第
,推断该元素位于第五周期第(3)比较大小(写>或<)
①键长:

 ②键能:
②键能:

③键角:

 ④键的极性:
④键的极性:

⑤沸点:

 ⑥熔点:
⑥熔点:

(4)①
 杂化类型为
杂化类型为②
 杂化类型为
杂化类型为③
 杂化类型为
杂化类型为(5)电子式:碳化钙(
 )
)(6)在空气中
 稳定性小于
稳定性小于 ,从电子排布的角度分析,其主要原因
,从电子排布的角度分析,其主要原因
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】元素化学是化学的基石,不同的元素往往呈现不同的特性。回答下列问题:
(1)Sn为第五周期元素,与C同主族,基态Sn的价电子排布式为_______ 。
(2)已知 的熔点为1040℃,
的熔点为1040℃, 的熔点为194℃,分析其差异的原因:
的熔点为194℃,分析其差异的原因:_______ 。
(3)基态碳原子的核外电子有_______ 种不同的运动状态。
(4)检验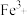 时,
时, 以S原子配位而不以N原子配位的原因是
以S原子配位而不以N原子配位的原因是_______ 。
(5)碳酰肼的结构为 ,是一种新型的环保锅炉水除氧剂。
,是一种新型的环保锅炉水除氧剂。
①碳酰肼中氮原子的杂化轨道类型为_______ 。
② 碳酰肼中含有的
碳酰肼中含有的 键数目为
键数目为_______  (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(6)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图所示,该化合物中的化学键有_______ (填字母)。 键 C.
键 C. 键 D.氢键 E.配位键
键 D.氢键 E.配位键
(1)Sn为第五周期元素,与C同主族,基态Sn的价电子排布式为
(2)已知
 的熔点为1040℃,
的熔点为1040℃, 的熔点为194℃,分析其差异的原因:
的熔点为194℃,分析其差异的原因:(3)基态碳原子的核外电子有
(4)检验
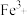 时,
时, 以S原子配位而不以N原子配位的原因是
以S原子配位而不以N原子配位的原因是(5)碳酰肼的结构为
 ,是一种新型的环保锅炉水除氧剂。
,是一种新型的环保锅炉水除氧剂。①碳酰肼中氮原子的杂化轨道类型为
②
 碳酰肼中含有的
碳酰肼中含有的 键数目为
键数目为 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(6)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图所示,该化合物中的化学键有

 键 C.
键 C. 键 D.氢键 E.配位键
键 D.氢键 E.配位键
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】溶质在溶剂中的溶解度取决于多种因素,请回答下列问题:
(1)实验发现:CH4极难溶于水,而HF极易溶于水,其原因是_______ 。
(2)通常条件下,1体积的水可溶解700体积的NH3,请说明三点理由:_______ 。
(1)实验发现:CH4极难溶于水,而HF极易溶于水,其原因是
(2)通常条件下,1体积的水可溶解700体积的NH3,请说明三点理由:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】表数据是对应物质的熔点
(1)AlCl3属于_______ (选填“强”、“弱”)电解质,它的晶体类型为__________ 。
(2)BCl3分子构型为平面正三角形,则BCl3分子为_________ 分子,其分子中的共价键类型为__________ 键。(均选填“极性”、“非极性”)
(3)BF3的熔点与BCl3相比______ (选填“高”、“低”、“无法确定”)。下列化学用语中,能正确表示BF3分子的是_______ (选填编号)。
a.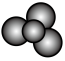
b.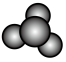
c.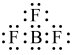
d.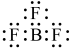
(4)NCl3在湿气中易水解生成两种物质,其中一种具有漂白性,写出水解的化学方程式_____ 。
| 物质 | 熔点(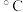 ) ) |
| AlF3 | 1291 |
| AlCl3 | 190 |
| BCl3 | -107 |
| NCl3 | -40 |
(1)AlCl3属于
(2)BCl3分子构型为平面正三角形,则BCl3分子为
(3)BF3的熔点与BCl3相比
a.

b.

c.

d.
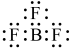
(4)NCl3在湿气中易水解生成两种物质,其中一种具有漂白性,写出水解的化学方程式
您最近一年使用:0次

 中的溶解度比在水中的溶解度大:
中的溶解度比在水中的溶解度大: 和
和 的混合溶液中加入过量的
的混合溶液中加入过量的 ,能生成
,能生成 沉淀,而不能生成
沉淀,而不能生成 沉淀:
沉淀: 存在两种对映异构体,而
存在两种对映异构体,而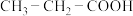 不存在对映异构体:
不存在对映异构体:

