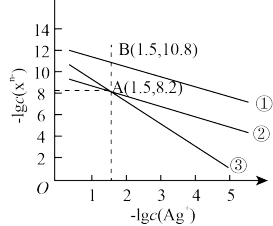
常温下,用AgNO3溶液分别滴定浓度均为0.01mol•L-1的KCl、K2C2O4溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O 的水解)。Xn-表示Cl-或C2O
的水解)。Xn-表示Cl-或C2O 。下列叙述正确的是
。下列叙述正确的是

 的水解)。Xn-表示Cl-或C2O
的水解)。Xn-表示Cl-或C2O 。下列叙述正确的是
。下列叙述正确的是
| A.Ksp(Ag2C2O4)的数量级为10-7 |
| B.N点表示AgCl的不饱和溶液 |
C.常温下,Ag2C2O4(s)+2Cl-(aq) AgCl(s)+C2O AgCl(s)+C2O (aq)的平衡常数为109.04 (aq)的平衡常数为109.04 |
D.向c(Cl-)=c(C2O )的混合溶液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 )的混合溶液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 |
更新时间:2023-04-08 15:09:50
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,几种铜盐的溶度积常数如表所示。下列说法正确的是
| 化合物 | CuCl | CuBr | Cu2S | Cu(OH)2 | Fe(OH)2 | CuS |
| Ksp | 3×10﹣7 | 2×10﹣9 | 2.5×10﹣50 | 2.6×10﹣19 | 8×10﹣16 | 1.3×10﹣36 |
| A.常温下,溶解度:CuCl<CuBr |
| B.向含同浓度的CuCl2和FeCl2的溶液中滴加稀NaOH溶液,Fe2+先沉淀 |
| C.向Cu(OH)2悬浊液中加入Na2S溶液,会形成CuS黑色沉淀 |
| D.反应2CuCl+S2﹣⇌Cu2S+2Cl﹣的平衡常数很小,反应几乎不进行 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列实验方案中,不能达到实验目的是
| 选项 | 实验目的 | 实验方案 |
| A | 验证Ksp(BaSO4) <Ksp(BaCO3) | 室温下,将BaSO4投入饱和Na2CO3溶液中充分反应,向过滤后所得固体中加入足量盐酸,固体部分溶解且有无色无味气体产生 |
| B | 验证氧化性:Br2>I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静止,可观察到下层液体呈紫色 |
| C | 验证酸性:HCN<CH3COOH | 室温下,用pH试纸测得0.100 mol·L-1 CH3COOH溶液的pH值约为3,0.100 mol·L-1 HCN溶液的pH值约为5 |
| D | 验证Fe3+能催化H2O2分解,且该分解反应为放热反应 | 向FeCl3溶液中滴入几滴30%的H2O2溶液,有气体产生,一段时间后,FeCl3溶液颜色加深 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温时,若Ca(OH)2和CaWO4(钨酸钙)的沉淀溶解平衡曲线如图所示(已知 =0.58)。下列分析不正确的是
=0.58)。下列分析不正确的是

 =0.58)。下列分析不正确的是
=0.58)。下列分析不正确的是
| A.a点表示Ca(OH)2与CaWO4均未达到溶解平衡状态 |
| B.饱和Ca(OH)2溶液和饱和CaWO4溶液等体积混合: c(OH-)>c(H+)>c(Ca2+)>c(WO42-) |
| C.饱和Ca(OH)2溶液中加入少量Na2O,溶液变浑浊 |
| D.石灰乳与0.1mol/LNa2WO4溶液混合后发生反应:Ca(OH)2+WO42-=CaWO4 +2OH- |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 将气体X分别通入溴水和酸性高锰酸钾溶液中,两溶液均褪色 | 气体X一定是SO2 |
| B | 向NaAlO2溶液中滴入NaHCO3溶液,产生白色沉淀 | AlO2-结合H+的能力比CO32-强 |
| C | 向某溶液中先滴加少量氯水,再滴加2滴KSCN溶液,溶液变成血红色 | 原溶液中一定含有Fe2+ |
| D | 在2mL0.01mol/L的Na2S溶液中先滴入几滴0.01mol/L ZnSO4溶液有白色沉淀,再滴入CuSO4溶液,又出现黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】测定溶液中Cl-的浓度时,常用标准AgNO3溶液滴定,K2CrO4作指示剂。根据如下关于AgCl、Ag2CrO4的溶度积图,判断下列说法正确 的是
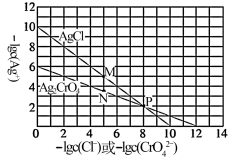

| A.P点时,二者的溶度积常数相同 |
| B.M点时,对AgCl溶液而言为饱和状态,对Ag2CrO4溶液而言为过饱和状态 |
C.向c(Cl-)=c( )=1×10-2mol·L-1的混合溶液中逐滴滴加1×10-3mol·L-1AgNO3溶液,振荡,先产生AgCl沉淀,当溶液中c(Cl-)降至1×10-5mol·L-1时,c( )=1×10-2mol·L-1的混合溶液中逐滴滴加1×10-3mol·L-1AgNO3溶液,振荡,先产生AgCl沉淀,当溶液中c(Cl-)降至1×10-5mol·L-1时,c( )=1×10-3.5mol·L-1 )=1×10-3.5mol·L-1 |
| D.当Cl-按化学计量比完全反应后,过量的一滴AgNO3溶液与K2CrO4反应沉淀颜色有明显变化。 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】还原沉淀法是处理含铬(含Cr2O 和CrO
和CrO )工业废水的常用方法,过程如下:
)工业废水的常用方法,过程如下:
CrO
 Cr2O
Cr2O
 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
已知转换过程中的反应为:2CrO (aq)+2H+(aq)
(aq)+2H+(aq)  Cr2O
Cr2O (aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO
(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO 有10/11转化为Cr2O
有10/11转化为Cr2O ,下列说法不正确的是
,下列说法不正确的是
 和CrO
和CrO )工业废水的常用方法,过程如下:
)工业废水的常用方法,过程如下:CrO

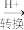 Cr2O
Cr2O
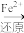 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓已知转换过程中的反应为:2CrO
 (aq)+2H+(aq)
(aq)+2H+(aq)  Cr2O
Cr2O (aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO
(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO 有10/11转化为Cr2O
有10/11转化为Cr2O ,下列说法不正确的是
,下列说法不正确的是| A.溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B.若用绿矾(FeSO4·7H2O)作还原剂,处理1 L废水,至少需要458.7 g |
| C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5 |
| D.常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5 mol·L-1,应调溶液的pH=5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向10mL浓度均为0.1mol·L-1的FeSO4和ZnSO4的混合溶液中加入0.1mol·L-1氨水,溶液中金属元素有不同的存在形式,它们的物质的量浓度与氨水(Kb=1.8×10-5)体积关系如下图所示。测得M、N点溶液pH分别为8.04、8.95。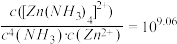
ii.Ksp[Zn(OH)2]<Ksp[Fe(OH)2]
下列说法正确的是
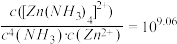
ii.Ksp[Zn(OH)2]<Ksp[Fe(OH)2]
下列说法正确的是
| A.曲线Y表示Zn2+ |
| B.Ksp[Fe(OH)2]=10-16.92 |
| C.N点以后,锌元素主要以Zn2+形式存在 |
| D.Zn(OH)2+4NH3⇌[Zn(NH3)4]2++2OH- K=10-7.86 |
您最近一年使用:0次

 是常见的二元弱酸(电离常数
是常见的二元弱酸(电离常数 ,
,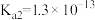 )。氢氧化铁[
)。氢氧化铁[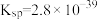 ]、氢氧化锌[
]、氢氧化锌[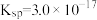 ]均为难溶多元弱碱,硫化锌[
]均为难溶多元弱碱,硫化锌[ ]为难溶盐。所有数据均为25℃的值。下列有关说法不正确的是
]为难溶盐。所有数据均为25℃的值。下列有关说法不正确的是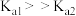 ,所以
,所以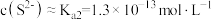
 饱和溶液中的
饱和溶液中的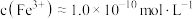
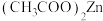 、
、 溶液中通入等物质的量的
溶液中通入等物质的量的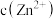 更小
更小 的
的 溶液与相同物质的量的
溶液与相同物质的量的 )的关系如图所示。下列说法正确的是
)的关系如图所示。下列说法正确的是