下列说法不正确的是
| A.键角是两个相邻共价键之间的夹角,说明共价键有方向性 |
| B.硫原子有两个未成对电子,因而只能形成2个共价键 |
| C.杂化轨道用于形成共价键和孤电子对 |
D.粒子ClO 的VSEPR模型与离子的空间结构不一致 的VSEPR模型与离子的空间结构不一致 |
更新时间:2023-04-11 15:23:21
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】氨硼烷(NH3BH3)和乙烷的结构相似,含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。下列说法正确的是
| A.H、B、N三种元素中,电负性最大的是B |
| B.根据对角线规则,B、Si最高价氧化物对应的水化物均为二元酸 |
| C.氨硼烷N采取sp3杂化,B采取sp3杂化 |
| D.NH3BH3属于分子晶体,晶体中存在的化学键只有极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列分子结构图中的“●”表示中心原子,“○”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。

下列说法错误的是

下列说法错误的是
A.只有分子①和③的中心原子采用 杂化 杂化 |
| B.分子②中含有三条σ键 |
| C.键角大小:③>①>④ |
| D.分子④是极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】氰分子式为 ,结构可表示为
,结构可表示为 ,性质与卤素相似,下列叙述中正确的是
,性质与卤素相似,下列叙述中正确的是
 ,结构可表示为
,结构可表示为 ,性质与卤素相似,下列叙述中正确的是
,性质与卤素相似,下列叙述中正确的是| A.NaCN与AgCN都易溶于水 |
B. 不能与NaOH溶液反应 不能与NaOH溶液反应 |
| C.四个原子在一条直线上,为非极性分子 |
D. 的键长大于 的键长大于 键 键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
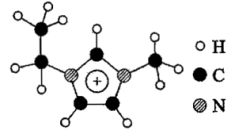
【推荐2】化合物(如图所示)由原子序数依次增大且分布在前三周期的元素X、Y、Z、M组成。其中Y和M同主族,下列说法正确的是
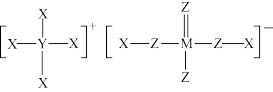
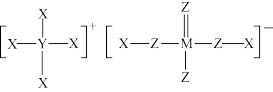
| A.简单氢化物的键角:Y<Z |
B.该化合物中M的杂化方式为 |
C.该化合物的阳离子与 是等电子体 是等电子体 |
D.除X原子外该化合物中其他原子均满足 结构 结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】为了降低能耗,选择硝酸根作为电催法合成氨的原料,离子方程式为: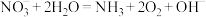 。下列说法正确的是
。下列说法正确的是
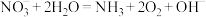 。下列说法正确的是
。下列说法正确的是A. 的VSEPR模型和空间结构一致 的VSEPR模型和空间结构一致 |
B. 分子之间氢键 分子之间氢键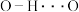 的键角约为109° 的键角约为109° |
C. 和 和 分子均含有非极性共价键 分子均含有非极性共价键 |
D. 的电子式为 的电子式为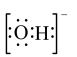 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列推论错误的是
| A.NaCl为离子晶体,可推测CsCl也为离子晶体 |
| B.CO2晶体是分子晶体,可推测CS2晶体也是分子晶体 |
| C.NH4+为正四面体结构,可推测PH4+也为正四面体结构 |
| D.NCl3中N原子是sp3杂化,可推测BCl3中B原子也是sp3杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某种合成医药、农药的中间体W结构如图所示,其中X、Y、Z、M、R均为短周期元素,原子序数依次增大。下列说法正确的是


| A.Z2和YM为等电子体 | B.RM3的空间构型为三角锥形 |
| C.W分子中R的杂化方式为sp2 | D.W分子中只存在极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.电负性越大,元素的非金属性越强,第一电离能也越大 |
| B.键长越短,共价键的稳定性越强 |
| C.共价键的成键原子只能是非金属原子 |
| D.SCl2属于AB2型共价化合物,中心原子S采用sp杂化轨道成键 |
您最近一年使用:0次

 的分子结构与
的分子结构与 相似,如图所示。下列有关说法错误的是
相似,如图所示。下列有关说法错误的是

 大π键
大π键

 ,下列有关叙述正确的是
,下列有关叙述正确的是
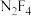 的电子式为
的电子式为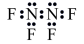
 强
强 中N原子的杂化方式不相同
中N原子的杂化方式不相同

