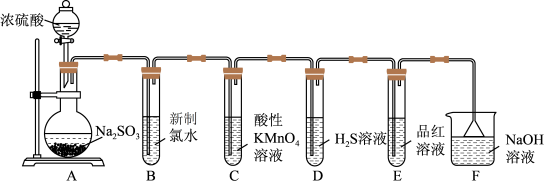
某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
已知: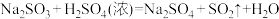 ;请回答下列问题:
;请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是___________ 。
(2)反应后,装置B中产生的现象是___________ ,发生反应的离子方程式为___________ 。
(3)装置C中的现象是___________ ,表现了SO2的___________ (填选项字母);装置D中的现象是___________ ,表现了SO2的___________ 。(同上)
A、漂白性 B、氧化性 C、还原性 D、酸性
(4)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:___________ 。

已知:
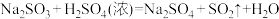 ;请回答下列问题:
;请回答下列问题:(1)装置A中盛放浓硫酸的仪器名称是
(2)反应后,装置B中产生的现象是
(3)装置C中的现象是
A、漂白性 B、氧化性 C、还原性 D、酸性
(4)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:
更新时间:2023-04-14 11:28:13
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某小组同学验证 的性质。装置如下图所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向
的性质。装置如下图所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向 固体上滴加70%的硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
固体上滴加70%的硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
已知:
(1)瓶盖___________ (填字母)中的实验现象能证明 具有还原性。
具有还原性。
(2)根据瓶盖A中现象,推断无色溶液中所含的离子是 和
和___________ 。
(3)瓶盖C中发生反应的化学方程式为___________ 。
(4)瓶盖C中无明显变化,若要证明C中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是___________ (填字母)。
a.石蕊溶液 b. 溶液
溶液
(5)上述实验可证明 具有还原性、
具有还原性、___________ 等性质。
 的性质。装置如下图所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向
的性质。装置如下图所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向 固体上滴加70%的硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
固体上滴加70%的硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。| 实验装置 | 瓶盖 | 物质 | 实验现象 |
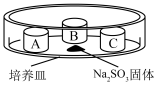 | A |  酸性溶液 酸性溶液 | 溶液褪色 |
| B | 蘸有品红溶液的棉花 | 品红溶液褪色 | |
| C | 蒸馏水 | 无明显变化 |

(1)瓶盖
 具有还原性。
具有还原性。(2)根据瓶盖A中现象,推断无色溶液中所含的离子是
 和
和(3)瓶盖C中发生反应的化学方程式为
(4)瓶盖C中无明显变化,若要证明C中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是
a.石蕊溶液 b.
 溶液
溶液(5)上述实验可证明
 具有还原性、
具有还原性、
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】用如图所示装置进行 与
与 反应的实验(夹持装置已略去):
反应的实验(夹持装置已略去):
(1)仪器a的名称为_______ 。
(2)装置Ⅳ中浓硫酸的作用为_______ 。
(3)装置Ⅲ中发生反应的化学方程式为_______ ,石棉绒的作用为_______ 。
(4)常温下,若将气体b缓慢通入盛有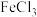 溶液的敞开试管中,一段时间后,观察到试管中颜色发生变化:
溶液的敞开试管中,一段时间后,观察到试管中颜色发生变化:
①写出上述溶液颜色发生变化时的离子方程式:_______ 。
②该反应中还原剂的总物质的量与氧化剂的总物质的量之比为_______ 。
 与
与 反应的实验(夹持装置已略去):
反应的实验(夹持装置已略去):
(1)仪器a的名称为
(2)装置Ⅳ中浓硫酸的作用为
(3)装置Ⅲ中发生反应的化学方程式为
(4)常温下,若将气体b缓慢通入盛有
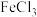 溶液的敞开试管中,一段时间后,观察到试管中颜色发生变化:
溶液的敞开试管中,一段时间后,观察到试管中颜色发生变化:①写出上述溶液颜色发生变化时的离子方程式:
②该反应中还原剂的总物质的量与氧化剂的总物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】如图所示是制取SO2并验证SO2某些性质的装置图。
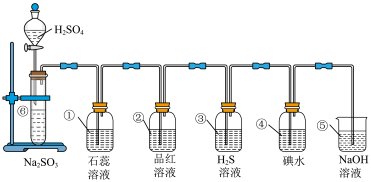
试回答:
(1)⑥中发生反应的化学方程式为___ 。
(2)①中的实验现象为___ ,此实验证明SO2是___ 氧化物。
(3)②中的品红溶液___ ,证明SO2有___ 。
(4)③中的H2S溶液____ ,证明SO2有___ 。
(5)④中的碘水___ ,证明SO2有____ 。
(6)⑤中NaOH溶液的作用是___ ,有关反应的化学方程式为____ 。

试回答:
(1)⑥中发生反应的化学方程式为
(2)①中的实验现象为
(3)②中的品红溶液
(4)③中的H2S溶液
(5)④中的碘水
(6)⑤中NaOH溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
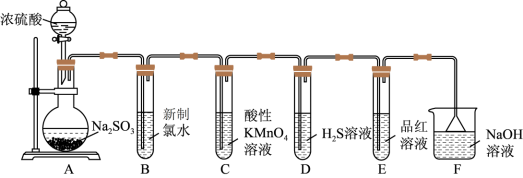
已知: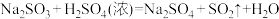 ;请回答下列问题:
;请回答下列问题:
(1)装置A中盛放亚硫酸钠溶液的仪器名称是_______ 。
(2)装置B中发生的离子方程式为_______ 。
(3)以上装置中表现了SO2氧化性的是_______ (填装置字母);
(4)装置F中倒扣漏斗的作用是_______ 。
(5)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:_______ 。

已知:
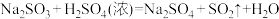 ;请回答下列问题:
;请回答下列问题:(1)装置A中盛放亚硫酸钠溶液的仪器名称是
(2)装置B中发生的离子方程式为
(3)以上装置中表现了SO2氧化性的是
(4)装置F中倒扣漏斗的作用是
(5)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】利用下图所示装置制取SO2并验证其部分性质(夹持装置已省略)。
已知: Na2SO3+ H2SO4(浓)=Na2SO4+ SO2↑+H2O
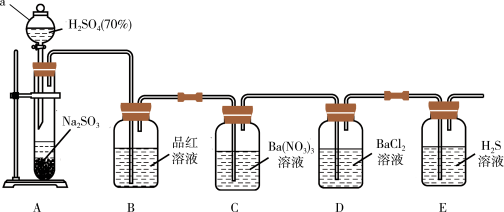
回答下列问题:
(1)仪器a的名称为______ ;装置B中品红溶液褪色,说明SO2具有______ 性。
(2)装置C中有白色沉淀生成,则该白色沉淀为_________ (填化学式) 。
(3)装置D中无白色沉淀产生,再向其中通入______ (填标号) 气体仍不会产生沉淀。
a.Cl2 b.NH3 c.O2 d.CO2
(4)装置E中有淡黄色沉淀生成,则该反应的化学方程式为_____________ 。
(5)该实验装置的缺陷是________________ 。
已知: Na2SO3+ H2SO4(浓)=Na2SO4+ SO2↑+H2O

回答下列问题:
(1)仪器a的名称为
(2)装置C中有白色沉淀生成,则该白色沉淀为
(3)装置D中无白色沉淀产生,再向其中通入
a.Cl2 b.NH3 c.O2 d.CO2
(4)装置E中有淡黄色沉淀生成,则该反应的化学方程式为
(5)该实验装置的缺陷是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】随着网络信息时代不断的发展,人和事件在网络上曝光的几率更大了,所以网络红人也逐渐的增加起来。2018年8月9日,美国男子为了变成网络红人,居然用漂白粉洗澡,结果差点被送进医院。太和一中为塑造中学生正确的价值观,结合此事发出“好学的中学生是最红的”倡议,我校理化创新社的同学发现教材在提到某些物质的用途时,仅指出该物质常用做漂白剂,并没有对其漂白原理及应用范围进行介绍,为响应学校的倡议,决定邀请你一起在全校普及漂白剂知识。查阅资料可知常见的六种漂白剂有:活性炭、氯水、过氧化氢、过氧化钠、臭氧、二氧化硫。请你帮助理化创新社的同学解决以下问题:
I.为探究和比较SO2和氯水的漂白性,理化创新社的同学设计了如的实验装置。

⑴实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:________________ ;
⑵实验室用装置E制备Cl2,其反应的化学化学方程式为:________________ ;
⑶①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:________________ ,D:________________ ;
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为:B:________________ ,D:________________ ;
⑷一位同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)________________ ;
II.很多同学认为往过氧化钠固体完全溶解反应后的溶液中滴加酚酞只会变红而不会褪色,而理化创新社的同学在实验中发现酚酞变红后又褪色。请帮助他们探究过氧化钠与水反应后的溶液滴加酚酞试液先变红后褪色的原因:
⑸过氧化钠与水反应的化学方程式为:________________ ;
⑹经查阅文献发现过氧化钠与水反应过程中,钠元素形成了稳定的化合物,溶液中还生成了一种不是很稳定且具有漂白性的物质X,X的化学式是________________ ;
⑺查阅资料发现过氧化钠与水的反应可以认为存在2步反应。请你尝试写出这2步化学反应的化学方程式:①________________ ;
②________________ ;
⑻下列说法正确的是________________ 。
A.利用SO2的漂白性可使酸性高锰酸钾溶液褪色
B.漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂
C.为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质
D.制造白糖工业中可用活性炭做脱色剂,是利用了活性炭的物理吸附能力
E.臭氧的漂白原理和双氧水不相同
I.为探究和比较SO2和氯水的漂白性,理化创新社的同学设计了如的实验装置。

⑴实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:
⑵实验室用装置E制备Cl2,其反应的化学化学方程式为:
⑶①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为:B:
⑷一位同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)
II.很多同学认为往过氧化钠固体完全溶解反应后的溶液中滴加酚酞只会变红而不会褪色,而理化创新社的同学在实验中发现酚酞变红后又褪色。请帮助他们探究过氧化钠与水反应后的溶液滴加酚酞试液先变红后褪色的原因:
⑸过氧化钠与水反应的化学方程式为:
⑹经查阅文献发现过氧化钠与水反应过程中,钠元素形成了稳定的化合物,溶液中还生成了一种不是很稳定且具有漂白性的物质X,X的化学式是
⑺查阅资料发现过氧化钠与水的反应可以认为存在2步反应。请你尝试写出这2步化学反应的化学方程式:①
②
⑻下列说法正确的是
A.利用SO2的漂白性可使酸性高锰酸钾溶液褪色
B.漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂
C.为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质
D.制造白糖工业中可用活性炭做脱色剂,是利用了活性炭的物理吸附能力
E.臭氧的漂白原理和双氧水不相同
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】如图所示是制取SO2并验证SO2某些性质的装置图。

试回答:
(1)⑥中发生反应的化学方程式为___ 。
(2)①中的实验现象为___ ,此实验证明SO2是___ 氧化物。
(3)②中的品红溶液___ ,证明SO2有___ 。
(4)③中的H2S溶液____ ,证明SO2有___ 。
(5)④中的碘水___ ,证明SO2有____ 。
(6)⑤中NaOH溶液的作用是___ ,有关反应的化学方程式为____ 。

试回答:
(1)⑥中发生反应的化学方程式为
(2)①中的实验现象为
(3)②中的品红溶液
(4)③中的H2S溶液
(5)④中的碘水
(6)⑤中NaOH溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。____ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择______ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案____ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为_____ 。
(5)装置E的作用是______ 。装置F中为_____ 溶液。
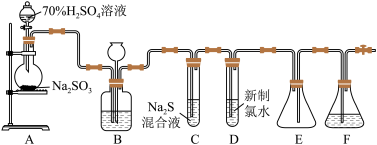
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某化学学习小组为探究NO2和SO2的反应,进行如下实验(如图所示)。

(1)图甲两集气瓶中___________ (填“上”或“下”)瓶颜色深。
(2)图乙中反应的现象是___________ 。
(3)图丙中“有红棕色气体产生”说明SO2和NO2反应的产物中有___________ ,说明NO2在该反应中表现___________ 性。
(4)由图乙和图丙中的现象写出NO2和SO2反应的化学方程式:___________ 。

(1)图甲两集气瓶中
(2)图乙中反应的现象是
(3)图丙中“有红棕色气体产生”说明SO2和NO2反应的产物中有
(4)由图乙和图丙中的现象写出NO2和SO2反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】二氧化硫具有漂白性,工业上常用二氧化硫来漂白纸浆、毛、丝、草帽等。此外二氧化硫还能够抑制霉菌和细菌的滋生,可用作防腐剂。
Ⅰ.甲组同学拟利用 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与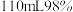 的浓硫酸(含
的浓硫酸(含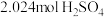 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。
(1)写出 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:__________________ 。
(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为_________ (填化学式)。
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)
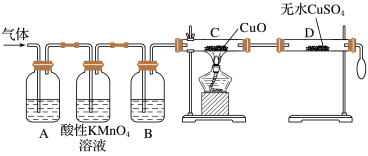
①A中试剂是品红溶液,作用是____________ 。
②B中所装试剂为____________ 。
③证明气体中混有杂质气体的实验现象是:________ 。
Ⅱ. 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。
(4)工业上有多种方法可以减少 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是___________ 。
(5)丙组同学认为 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
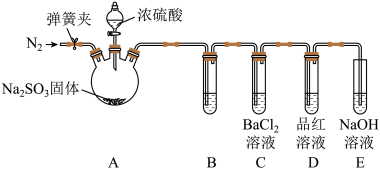
已知: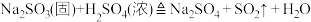
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是___________ 。
Ⅰ.甲组同学拟利用
 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与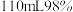 的浓硫酸(含
的浓硫酸(含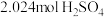 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。(1)写出
 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)

①A中试剂是品红溶液,作用是
②B中所装试剂为
③证明气体中混有杂质气体的实验现象是:
Ⅱ.
 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。(4)工业上有多种方法可以减少
 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是(5)丙组同学认为
 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
已知:
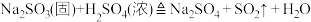
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是
您最近一年使用:0次

 为组成元素相同的无色液体,
为组成元素相同的无色液体, 是单质,I的溶液呈蓝色,反应①是工业上冶炼金属的一种方法。请回答下列问题:
是单质,I的溶液呈蓝色,反应①是工业上冶炼金属的一种方法。请回答下列问题: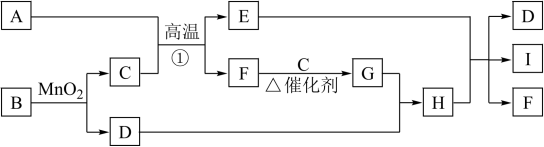
 的水溶液)化学方程式
的水溶液)化学方程式


