硅材料在生活中占有重要地位。请回答:
(1)Si原子结构示意图为___________ , 受热分解生成
受热分解生成 和
和 ,
, 空间结构名称为
空间结构名称为___________ , 受热不稳定的原因是
受热不稳定的原因是___________ 。
(2)在硅酸盐中, 四面体(如下图(a))中Si原子的杂化形式为
四面体(如下图(a))中Si原子的杂化形式为___________ 。
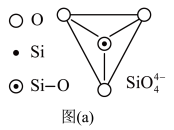
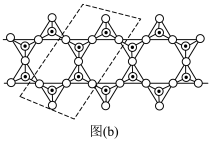
(3) 通过共用顶角氧离子可形成链状结构型式。图(b)为一种无限长双链结构的多硅酸根,Si与O的原子数之比为
通过共用顶角氧离子可形成链状结构型式。图(b)为一种无限长双链结构的多硅酸根,Si与O的原子数之比为______ ,化学式为______ 。
(1)Si原子结构示意图为
 受热分解生成
受热分解生成 和
和 ,
, 空间结构名称为
空间结构名称为 受热不稳定的原因是
受热不稳定的原因是(2)在硅酸盐中,
 四面体(如下图(a))中Si原子的杂化形式为
四面体(如下图(a))中Si原子的杂化形式为
(3)
 通过共用顶角氧离子可形成链状结构型式。图(b)为一种无限长双链结构的多硅酸根,Si与O的原子数之比为
通过共用顶角氧离子可形成链状结构型式。图(b)为一种无限长双链结构的多硅酸根,Si与O的原子数之比为
更新时间:2023/04/15 18:58:37
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】某盐A由三种元素组成,其相关的转化关系如下图(所有产物均已标在框图上),其中C为红棕色液体,其化学性质与其组成元素的单质相似。
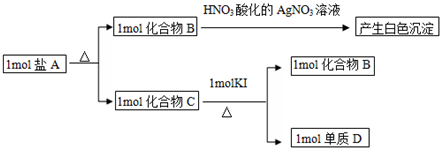
(1)A的化学式为________________ ,画出B中阴离子的结构示意图:___________ ;
(2)写出C的电子式:________________ ;化合物C中显正价的是____________ 元素;
(3)写出化合物C与KI反应的化学方程式:_____________________ ;
(4)下列物质能与C发生反应的有_______________ 。
A.SO2 B.H2O C.乙烯 D.Na2SO4

(1)A的化学式为
(2)写出C的电子式:
(3)写出化合物C与KI反应的化学方程式:
(4)下列物质能与C发生反应的有
A.SO2 B.H2O C.乙烯 D.Na2SO4
您最近一年使用:0次
【推荐2】某研究小组为探究不溶性固体X的组成和性质,进行了如下实验。已知X是一种仅含有四种元素的具有固定成的盐类物质,H由碘元素和另外一种元素组成,图中所有气体体积均在标准状况下测定。
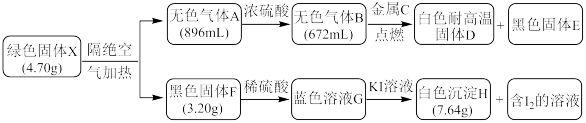
请回答下列问题:
(1)写出X的化学式__________ ;
(2)写出C的原子结构示意图___________ ;组成E元素的某种核素常用于考古断代,该原子核内中子数为8,写出该校素的原子符号___________ 。
(3)C在装有B的集气瓶中燃烧,其实验现象为___________ ;并写出相应的化学方程式___________ 。
(4)已知H能与含NaClO的碱性溶液反应生成NaIO3和蓝色絮状沉淀,试写出该反应的离子方程式____________________________ 。

请回答下列问题:
(1)写出X的化学式
(2)写出C的原子结构示意图
(3)C在装有B的集气瓶中燃烧,其实验现象为
(4)已知H能与含NaClO的碱性溶液反应生成NaIO3和蓝色絮状沉淀,试写出该反应的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态K原子中,核外电子占据最高能层的符号是___________ 。占据该能层电子的电子云轮廓图形状为___________ 。
(2)元素K的焰色为___________ 色。单质K的密度比Na___________ (填“大”或“小”)。
(3)I的原子结构示意图为___________ 。
(4)X射线衍射测定发现,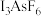 中存在
中存在 离子。
离子。 离子的空间结构为
离子的空间结构为___________ 。
(5) 晶体是一种性能良好的非线性光学材料,其晶胞结构如图所示,晶胞中K、I、O分别处于顶角、体心、面心位置,棱长为anm。K与O间的最短距离为
晶体是一种性能良好的非线性光学材料,其晶胞结构如图所示,晶胞中K、I、O分别处于顶角、体心、面心位置,棱长为anm。K与O间的最短距离为___________ nm,与K紧邻的O个数为___________ 。
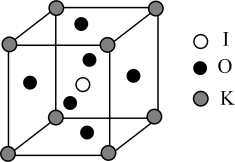
(6)在 晶胞结构的另一种表示中,I处于各顶角位置,则K处于
晶胞结构的另一种表示中,I处于各顶角位置,则K处于___________ 位置,O处于___________ 位置。
(1)基态K原子中,核外电子占据最高能层的符号是
(2)元素K的焰色为
(3)I的原子结构示意图为
(4)X射线衍射测定发现,
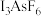 中存在
中存在 离子。
离子。 离子的空间结构为
离子的空间结构为(5)
 晶体是一种性能良好的非线性光学材料,其晶胞结构如图所示,晶胞中K、I、O分别处于顶角、体心、面心位置,棱长为anm。K与O间的最短距离为
晶体是一种性能良好的非线性光学材料,其晶胞结构如图所示,晶胞中K、I、O分别处于顶角、体心、面心位置,棱长为anm。K与O间的最短距离为
(6)在
 晶胞结构的另一种表示中,I处于各顶角位置,则K处于
晶胞结构的另一种表示中,I处于各顶角位置,则K处于
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】铁橄榄石是天然的铁矿石,由实验测得铁橄榄石的摩尔质量为204 g·mol-1,其中铁元素的质量分数为54.9%,可以通过如下反应和相应的数据推知它的化学式。其中A ~ J是中学化学中的常见物质,G是一种红褐色固体,D是一种难溶于水的含氧酸,J是一种主要的温室气体,A为强碱,其焰色反应呈黄色,E和B分别与酸化的硝酸银溶液反应时的实验现象相同,均有白色沉淀产生,流程中的部分生成物已略去。
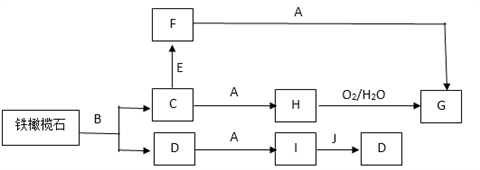
回答下列问题:
(1)A的电子式:__________________ 。
(2)铁橄榄石的化学式:__________________ 。
(3)写出H → G的化学方程式:__________________ 。

回答下列问题:
(1)A的电子式:
(2)铁橄榄石的化学式:
(3)写出H → G的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】设计如下实验探究某矿石(仅含四种短周期元素)的组成和性质,无色液体1为最常见的液体纯净物:

(1)白色胶状沉淀2的化学式___________ ,无色液体1的电子式___________ 。
(2)矿石的化学式为___________ 。
(3)白色粉末3溶于过量NaOH溶液的离子方程式是___________ 。
(4)无色溶液3与过量NaOH溶液反应的离子方程式___________ 。
(5)白色粉末3与能与同主族短周期元素的单质反应,检验其反应产物的方法是___________ 。

(1)白色胶状沉淀2的化学式
(2)矿石的化学式为
(3)白色粉末3溶于过量NaOH溶液的离子方程式是
(4)无色溶液3与过量NaOH溶液反应的离子方程式
(5)白色粉末3与能与同主族短周期元素的单质反应,检验其反应产物的方法是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】我国某企业冶炼锌的过程采用萃取法回收镣锗铜,但萃余液中仍有大量硫酸、 以及少量
以及少量 、
、 、
、 、
、 、
、 、
、 等,现利用该萃余液生产ZnO的工业流程如图所示。
等,现利用该萃余液生产ZnO的工业流程如图所示。 )中硫元素为
)中硫元素为 价,具有强氧化性。回答下列问题:
价,具有强氧化性。回答下列问题:
(1) 中O的化合价为
中O的化合价为___ ,过硫酸钠氧化了萃余液中的___ (填离子符号)。
(2)下列仪器中,操作Ⅰ需要用到,且主要成分为无机非金属材料的是___ (填标号)。____ 。
(4)加入 目的是将滤液中
目的是将滤液中 沉淀,检验
沉淀,检验 完全沉淀的操作为
完全沉淀的操作为____ 。
(5)操作Ⅱ名称为____ 。
(6)萃余液中锌含量为39g/L,现用1 萃余液生产ZnO,得到ZnO32.4kg,则ZnO的产率为
萃余液生产ZnO,得到ZnO32.4kg,则ZnO的产率为___ 。
 以及少量
以及少量 、
、 、
、 、
、 、
、 、
、 等,现利用该萃余液生产ZnO的工业流程如图所示。
等,现利用该萃余液生产ZnO的工业流程如图所示。
 )中硫元素为
)中硫元素为 价,具有强氧化性。回答下列问题:
价,具有强氧化性。回答下列问题:(1)
 中O的化合价为
中O的化合价为(2)下列仪器中,操作Ⅰ需要用到,且主要成分为无机非金属材料的是
A.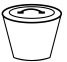 B.
B.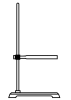 C.
C.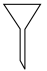 D.
D.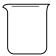 E.
E.
(4)加入
 目的是将滤液中
目的是将滤液中 沉淀,检验
沉淀,检验 完全沉淀的操作为
完全沉淀的操作为(5)操作Ⅱ名称为
(6)萃余液中锌含量为39g/L,现用1
 萃余液生产ZnO,得到ZnO32.4kg,则ZnO的产率为
萃余液生产ZnO,得到ZnO32.4kg,则ZnO的产率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】铁氨化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy,的制备需铁、氨气丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为_______ 。
(2)丙酮(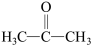 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是_______ ,三种元素电负性由小到大的顺序为_______ ,1mol丙酮分子中含有σ键的数目为_______ 。
(3)N、P、S三种元素的第一电离能由小到大的顺序为_______ 。
(4)乙醇(CH3CH2OH)的沸点高于丙酮,这是因为_______ 。
(5)磷酸根离子的空间构型为_______ 。
(1)Fe3+基态核外电子排布式为
(2)丙酮(
 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是(3)N、P、S三种元素的第一电离能由小到大的顺序为
(4)乙醇(CH3CH2OH)的沸点高于丙酮,这是因为
(5)磷酸根离子的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】新型节能材料高温超导体的最先突破是从1987年新的钇钡铜氧材料的研究开始的。对钇钡铜氧材料的分析表明,其组成为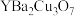 ;其中39号元素金属钇化合价为+3价,铜以常见的
;其中39号元素金属钇化合价为+3价,铜以常见的 和罕见的高价态形式存在。
和罕见的高价态形式存在。
(1)写出该物质中高价铜离子的核外价电子排布图___________ 。
(2)将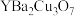 试样溶于稀酸,高价铜离子全部被还原为
试样溶于稀酸,高价铜离子全部被还原为 。写出试样在稀酸中溶解的离子反应方程式
。写出试样在稀酸中溶解的离子反应方程式___________ 。
(3) 能与
能与 形成具有对称空间结构的
形成具有对称空间结构的 。若
。若 中两个
中两个 ,分别被
,分别被 取代,能得到(m)、(n)两种不同结构的
取代,能得到(m)、(n)两种不同结构的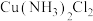 :
: 的空间构型是
的空间构型是___________ ;在水中的溶解度:(m)___________ (n)(填“>”、“=”或“<”)。
(4)锌、钴、镍可形成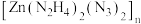 、
、 、
、 等配合物。
等配合物。
①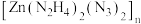 中
中 的配体是
的配体是___________ 。
②氯化钴(Ⅲ)的氨合物钴离子配位数为6,制备条件不同,所得晶体结构不同。有活性炭催化时,主要生成橙黄色晶体 ,已知
,已知 是以
是以 为中心的正八面体结构(如图所示),若其中2个
为中心的正八面体结构(如图所示),若其中2个 被
被 取代,则所形成的
取代,则所形成的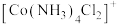 的空间结构有
的空间结构有___________ 种;没有活性炭时,所得主要产物是紫红色晶体,化学式为 ,向含0.1mol该晶体的水溶液中滴加
,向含0.1mol该晶体的水溶液中滴加 溶液,可得白色沉淀28.7g,该晶体配离子的化学式为
溶液,可得白色沉淀28.7g,该晶体配离子的化学式为___________ 。___________ 。
②钇钡铜氧晶体属四方晶系,晶胞参数如图所示,晶胞棱长夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。如原子分数坐标A为(0,0,0),B为 ( ,
, ,
, ),C为(
),C为( ,
, ,m),则D的原子分数坐标为
,m),则D的原子分数坐标为___________ 。
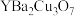 ;其中39号元素金属钇化合价为+3价,铜以常见的
;其中39号元素金属钇化合价为+3价,铜以常见的 和罕见的高价态形式存在。
和罕见的高价态形式存在。(1)写出该物质中高价铜离子的核外价电子排布图
(2)将
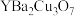 试样溶于稀酸,高价铜离子全部被还原为
试样溶于稀酸,高价铜离子全部被还原为 。写出试样在稀酸中溶解的离子反应方程式
。写出试样在稀酸中溶解的离子反应方程式(3)
 能与
能与 形成具有对称空间结构的
形成具有对称空间结构的 。若
。若 中两个
中两个 ,分别被
,分别被 取代,能得到(m)、(n)两种不同结构的
取代,能得到(m)、(n)两种不同结构的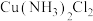 :
:
 的空间构型是
的空间构型是(4)锌、钴、镍可形成
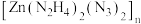 、
、 、
、 等配合物。
等配合物。①
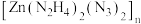 中
中 的配体是
的配体是②氯化钴(Ⅲ)的氨合物钴离子配位数为6,制备条件不同,所得晶体结构不同。有活性炭催化时,主要生成橙黄色晶体
 ,已知
,已知 是以
是以 为中心的正八面体结构(如图所示),若其中2个
为中心的正八面体结构(如图所示),若其中2个 被
被 取代,则所形成的
取代,则所形成的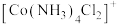 的空间结构有
的空间结构有 ,向含0.1mol该晶体的水溶液中滴加
,向含0.1mol该晶体的水溶液中滴加 溶液,可得白色沉淀28.7g,该晶体配离子的化学式为
溶液,可得白色沉淀28.7g,该晶体配离子的化学式为
②钇钡铜氧晶体属四方晶系,晶胞参数如图所示,晶胞棱长夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。如原子分数坐标A为(0,0,0),B为 (
 ,
, ,
, ),C为(
),C为( ,
, ,m),则D的原子分数坐标为
,m),则D的原子分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】富氮含能化合物具有高密度、高生成焓、高能量及清洁无污染(爆炸产物主要是 )等优点。回答下列问题:
)等优点。回答下列问题:
(1)固态 的晶体类型为
的晶体类型为___________ , 在常温下显示出惰性,但在高温下化学性质非常活泼,可与
在常温下显示出惰性,但在高温下化学性质非常活泼,可与 、
、 、
、 和
和 等直接化合,其原因是
等直接化合,其原因是___________ 。
(2) 的空间构型为
的空间构型为___________ ,N原子的杂化方式是___________ 。 与
与 具有相同的空间构型,
具有相同的空间构型, 可聚合为
可聚合为 ,原因是
,原因是___________ 。
(3)由于氮的孤对电子之间的相互排斥,使得全氮类物质,如 (
(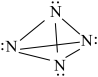 )、
)、 (
(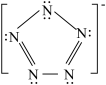 )非常不稳定,存在时间极短。
)非常不稳定,存在时间极短。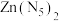 可以稳定存在,原因是
可以稳定存在,原因是___________ 。
(4)叠氮化钠( )的晶体结构如图所示。阿伏加德罗常数的值为
)的晶体结构如图所示。阿伏加德罗常数的值为 ,叠氮化钠的晶胞参数为
,叠氮化钠的晶胞参数为 、
、 、
、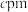 ,
, ,密度
,密度 ,则
,则
___________ (用含a、b、c和 的代数式表示)。
的代数式表示)。
 )等优点。回答下列问题:
)等优点。回答下列问题:(1)固态
 的晶体类型为
的晶体类型为 在常温下显示出惰性,但在高温下化学性质非常活泼,可与
在常温下显示出惰性,但在高温下化学性质非常活泼,可与 、
、 、
、 和
和 等直接化合,其原因是
等直接化合,其原因是(2)
 的空间构型为
的空间构型为 与
与 具有相同的空间构型,
具有相同的空间构型, 可聚合为
可聚合为 ,原因是
,原因是(3)由于氮的孤对电子之间的相互排斥,使得全氮类物质,如
 (
( )、
)、 (
( )非常不稳定,存在时间极短。
)非常不稳定,存在时间极短。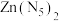 可以稳定存在,原因是
可以稳定存在,原因是(4)叠氮化钠(
 )的晶体结构如图所示。阿伏加德罗常数的值为
)的晶体结构如图所示。阿伏加德罗常数的值为 ,叠氮化钠的晶胞参数为
,叠氮化钠的晶胞参数为 、
、 、
、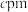 ,
, ,密度
,密度 ,则
,则
 的代数式表示)。
的代数式表示)。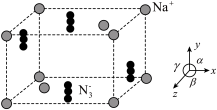
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】铼(Re)用于制造高效能火箭引擎。从辉钼矿氧化焙烧后的烟道灰(主要成分有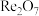 、
、 、
、 、CuO、
、CuO、 )中提取铼粉的一种工艺流程如图所示。
)中提取铼粉的一种工艺流程如图所示。
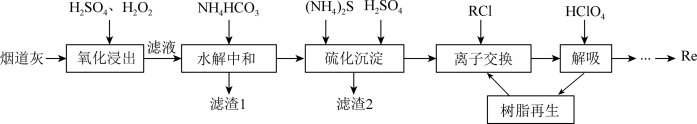
已知:
回答下列问题:
(1)“氧化浸出”时, 被氧化为
被氧化为 ,
, 被氧化的离子方程式为
被氧化的离子方程式为___________ 。
(2)“水解中和”时,加 调节溶液pH=6。
调节溶液pH=6。
① 溶液中
溶液中
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②除钼的化合物外,滤渣1中还有___________ (填化学式)。
③计算此时溶液中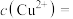
___________  。
。
(3)“硫化沉淀”时,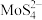 与
与 反应生成难溶的
反应生成难溶的 ,离子方程式为
,离子方程式为___________ 。
(4)“离子交换”“解吸”“树脂再生”一系列步骤中物质转化关系如图所示。
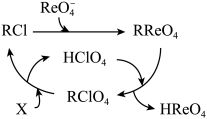
①树脂再生时需加入的试剂X为___________ (填化学式)。
②“解吸”所用 中的阴离子的空间构型为
中的阴离子的空间构型为___________ 。
(5)铼的某种氧化物的晶胞如图所示,该物质的化学式为___________ 。铼原子填在氧原子围成的___________ (填“四面体”、“立方体”或“八面体”)空隙中。

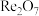 、
、 、
、 、CuO、
、CuO、 )中提取铼粉的一种工艺流程如图所示。
)中提取铼粉的一种工艺流程如图所示。
已知:
 |  |  | |
| 开始沉淀pH | 2.5 | 7.0 | 5.7 |
| 完全沉淀pH | 3.2 | 9.0 | 6.7 |
(1)“氧化浸出”时,
 被氧化为
被氧化为 ,
, 被氧化的离子方程式为
被氧化的离子方程式为(2)“水解中和”时,加
 调节溶液pH=6。
调节溶液pH=6。①
 溶液中
溶液中
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②除钼的化合物外,滤渣1中还有
③计算此时溶液中
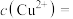
 。
。(3)“硫化沉淀”时,
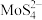 与
与 反应生成难溶的
反应生成难溶的 ,离子方程式为
,离子方程式为(4)“离子交换”“解吸”“树脂再生”一系列步骤中物质转化关系如图所示。

①树脂再生时需加入的试剂X为
②“解吸”所用
 中的阴离子的空间构型为
中的阴离子的空间构型为(5)铼的某种氧化物的晶胞如图所示,该物质的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】过渡金属及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布图为___________ ,与钛同周期的过渡元素中,基态原子的成对电子数与钛相同的还有___________ 种。
(2)在浓的 的盐酸溶液中加入乙醚,并通入
的盐酸溶液中加入乙醚,并通入 至饱和,可得到配位数为6、组成为
至饱和,可得到配位数为6、组成为 的晶体,该晶体中两种配体的物质的量之比为
的晶体,该晶体中两种配体的物质的量之比为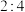 ,则由该配合离子组成的晶体化学式还可以写为
,则由该配合离子组成的晶体化学式还可以写为___________ 。
(3)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂 ,通过如图反应实现铜离子的富集,进行回收。
,通过如图反应实现铜离子的富集,进行回收。 所含元素的第一电离能最大的是
所含元素的第一电离能最大的是___________ (用元素符号表示)。
② 化合物中中心原子铜的配位数是
化合物中中心原子铜的配位数是___________ 。
(4)氮化镓( )已成为固态射频功率应用领域无可争议的冠军,它在雷达,
)已成为固态射频功率应用领域无可争议的冠军,它在雷达, 无线领域等方面应用广泛。
无线领域等方面应用广泛。 是坚硬的高熔点材料,熔点约为
是坚硬的高熔点材料,熔点约为 ,晶体
,晶体 的熔点高于晶体
的熔点高于晶体 (熔点
(熔点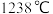 )熔点的原因是
)熔点的原因是___________ 。
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。 ,
, 原子半径为
原子半径为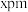 ,
, 原子半径为
原子半径为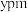 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞中原子的空间利用率为
,则该晶胞中原子的空间利用率为___________ (列出计算式即可,不用化简)。
(1)基态钛原子的价电子排布图为
(2)在浓的
 的盐酸溶液中加入乙醚,并通入
的盐酸溶液中加入乙醚,并通入 至饱和,可得到配位数为6、组成为
至饱和,可得到配位数为6、组成为 的晶体,该晶体中两种配体的物质的量之比为
的晶体,该晶体中两种配体的物质的量之比为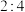 ,则由该配合离子组成的晶体化学式还可以写为
,则由该配合离子组成的晶体化学式还可以写为(3)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂
 ,通过如图反应实现铜离子的富集,进行回收。
,通过如图反应实现铜离子的富集,进行回收。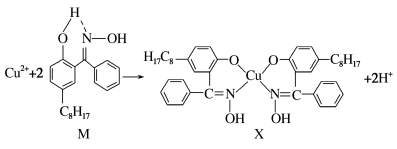
 所含元素的第一电离能最大的是
所含元素的第一电离能最大的是②
 化合物中中心原子铜的配位数是
化合物中中心原子铜的配位数是(4)氮化镓(
 )已成为固态射频功率应用领域无可争议的冠军,它在雷达,
)已成为固态射频功率应用领域无可争议的冠军,它在雷达, 无线领域等方面应用广泛。
无线领域等方面应用广泛。 是坚硬的高熔点材料,熔点约为
是坚硬的高熔点材料,熔点约为 ,晶体
,晶体 的熔点高于晶体
的熔点高于晶体 (熔点
(熔点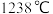 )熔点的原因是
)熔点的原因是(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。
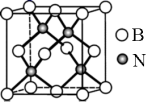
 ,
, 原子半径为
原子半径为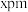 ,
, 原子半径为
原子半径为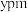 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞中原子的空间利用率为
,则该晶胞中原子的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】我国科学家利用锰簇催化剂( ,x代表氧原子数)解密光合作用。锰簇的可逆结构异构化反应如图。
,x代表氧原子数)解密光合作用。锰簇的可逆结构异构化反应如图。

请回答下列问题:
(1)基态氧原子价层电子轨道表示式为___________ 。基态钙原子中能量最高的电子所占据原子轨道的电子云轮廓图为___________ 形。
(2)金属 、
、 的第二电离能分别为
的第二电离能分别为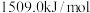 、
、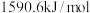 ,
,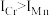 的原因是是
的原因是是___________ 。
(3)在上述异构化反应中, 中由
中由 形成的
形成的 键有
键有___________  。
。
(4) 晶胞与
晶胞与 晶胞属于同种类型,
晶胞属于同种类型, 晶胞结构如图所示。
晶胞结构如图所示。
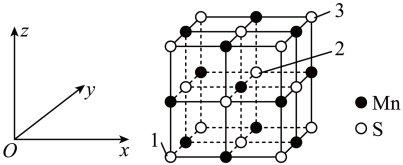
① 原子位于S原子形成的
原子位于S原子形成的___________ (填“正四面体”或“正八面体”)中心。
②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在 晶胞坐标系中,1号S原子坐标为
晶胞坐标系中,1号S原子坐标为 ,3号S原子坐标为
,3号S原子坐标为 ,则2号S原子坐标为
,则2号S原子坐标为___________ 。
③已知: 晶体的密度为
晶体的密度为 ,
, 为阿伏加德罗常数的值。则
为阿伏加德罗常数的值。则 晶胞中阴、阳离子最近距离为
晶胞中阴、阳离子最近距离为___________ pm。
 ,x代表氧原子数)解密光合作用。锰簇的可逆结构异构化反应如图。
,x代表氧原子数)解密光合作用。锰簇的可逆结构异构化反应如图。
请回答下列问题:
(1)基态氧原子价层电子轨道表示式为
(2)金属
 、
、 的第二电离能分别为
的第二电离能分别为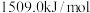 、
、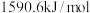 ,
,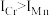 的原因是是
的原因是是(3)在上述异构化反应中,
 中由
中由 形成的
形成的 键有
键有 。
。(4)
 晶胞与
晶胞与 晶胞属于同种类型,
晶胞属于同种类型, 晶胞结构如图所示。
晶胞结构如图所示。
①
 原子位于S原子形成的
原子位于S原子形成的②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在
 晶胞坐标系中,1号S原子坐标为
晶胞坐标系中,1号S原子坐标为 ,3号S原子坐标为
,3号S原子坐标为 ,则2号S原子坐标为
,则2号S原子坐标为③已知:
 晶体的密度为
晶体的密度为 ,
, 为阿伏加德罗常数的值。则
为阿伏加德罗常数的值。则 晶胞中阴、阳离子最近距离为
晶胞中阴、阳离子最近距离为
您最近一年使用:0次



