化学反应中的能量变化通常表现为热量变化,研究热量变化具有重要的意义。化学反应的反应热可通过实验测定,也可通过计算间接获得。
(1)下列变化属于吸热反应的是___________ (填序号)。
①液态水气化 ②胆矾加热变成白色粉末 ③浓硫酸稀释 ④氢气还原氧化铜 ⑤碳酸钙高温分解
⑥氢氧化钾和稀硫酸反应 ⑦灼热的木炭与 的反应 ⑧
的反应 ⑧ 晶体与
晶体与 晶体的反应 ⑨甲烷在空气中燃烧的反应
晶体的反应 ⑨甲烷在空气中燃烧的反应
(2)在25 ℃、101 kPa下,23 g乙醇 完全燃烧生成
完全燃烧生成 和被态水时放热638.4 kJ。则表示乙醇燃烧热的热化学方程式为
和被态水时放热638.4 kJ。则表示乙醇燃烧热的热化学方程式为___________ 。
Ⅰ.中和反应反应热的实验测定
(3)某化学兴趣小组要完成中和反应反应热的测定,实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、量筒2支、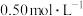 醋酸、
醋酸、 NaOH溶液,实验尚缺少的玻璃用品是
NaOH溶液,实验尚缺少的玻璃用品是___________ 、___________ 。
(4)在量热计中将100 mL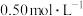 的醋酸溶液与100mL
的醋酸溶液与100mL  的氢氧化钠溶液混合,温度从298.0 K升高到300.7 K,已知量热计的热容常数(各部件温度每升高1 K所需的热量)是
的氢氧化钠溶液混合,温度从298.0 K升高到300.7 K,已知量热计的热容常数(各部件温度每升高1 K所需的热量)是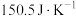 ,溶液密度均近似为
,溶液密度均近似为 ,充分混合后溶液的比热容
,充分混合后溶液的比热容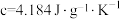 。求醋酸与氢氧化钠发生中和反应的反应热
。求醋酸与氢氧化钠发生中和反应的反应热
___________ 。(小数点后保留1位数字)
(5)若用KOH代替NaOH,对测定结果___________ (填“有”或“无”)影响;若用盐酸代替醋酸做实验,则测定结果
___________ (填“偏大”或“偏小”无影响)。
Ⅱ.通过计算间接获得反应热
(6)利用合成气(主要成分为CO、 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:
①

②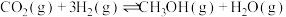

③
 ,已知反应①中相关的化学键键能数据如下:
,已知反应①中相关的化学键键能数据如下:
(已知 结构式为
结构式为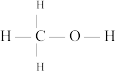 )
)
由此计算
___________ ;已知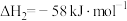 ,则
,则
___________ 。
(1)下列变化属于吸热反应的是
①液态水气化 ②胆矾加热变成白色粉末 ③浓硫酸稀释 ④氢气还原氧化铜 ⑤碳酸钙高温分解
⑥氢氧化钾和稀硫酸反应 ⑦灼热的木炭与
 的反应 ⑧
的反应 ⑧ 晶体与
晶体与 晶体的反应 ⑨甲烷在空气中燃烧的反应
晶体的反应 ⑨甲烷在空气中燃烧的反应(2)在25 ℃、101 kPa下,23 g乙醇
 完全燃烧生成
完全燃烧生成 和被态水时放热638.4 kJ。则表示乙醇燃烧热的热化学方程式为
和被态水时放热638.4 kJ。则表示乙醇燃烧热的热化学方程式为Ⅰ.中和反应反应热的实验测定
(3)某化学兴趣小组要完成中和反应反应热的测定,实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、量筒2支、
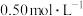 醋酸、
醋酸、 NaOH溶液,实验尚缺少的玻璃用品是
NaOH溶液,实验尚缺少的玻璃用品是(4)在量热计中将100 mL
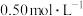 的醋酸溶液与100mL
的醋酸溶液与100mL  的氢氧化钠溶液混合,温度从298.0 K升高到300.7 K,已知量热计的热容常数(各部件温度每升高1 K所需的热量)是
的氢氧化钠溶液混合,温度从298.0 K升高到300.7 K,已知量热计的热容常数(各部件温度每升高1 K所需的热量)是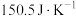 ,溶液密度均近似为
,溶液密度均近似为 ,充分混合后溶液的比热容
,充分混合后溶液的比热容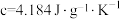 。求醋酸与氢氧化钠发生中和反应的反应热
。求醋酸与氢氧化钠发生中和反应的反应热
(5)若用KOH代替NaOH,对测定结果

Ⅱ.通过计算间接获得反应热
(6)利用合成气(主要成分为CO、
 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:①


②
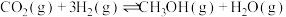

③

 ,已知反应①中相关的化学键键能数据如下:
,已知反应①中相关的化学键键能数据如下:| 化学键 |  |  |  |  |  |
 | 436 | 343 | 1076 | 465 | 413 |
 结构式为
结构式为 )
)由此计算

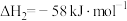 ,则
,则
更新时间:2023-04-21 10:00:26
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】 、
、 、
、 是工业上重要的化工原料,回答下列问题:
是工业上重要的化工原料,回答下列问题:
(1) 的燃烧热为
的燃烧热为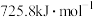 ,写出表示其燃烧热的热化学方程式:
,写出表示其燃烧热的热化学方程式:_______ 。
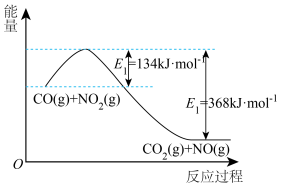
(2)如图表示的是 和
和 反应生成
反应生成 和
和 过程中能量变化示意图,写出
过程中能量变化示意图,写出 和
和 反应的热化学方程式:
反应的热化学方程式:_______ 。
(3)某些常见化学键的键能数据如下表:
则 □
□
_______  。
。
(4)利用 与
与 制备合成气
制备合成气 ,可能的反应历程如图所示:
,可能的反应历程如图所示:
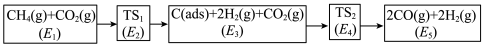
说明: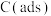 为吸附性活性炭,
为吸附性活性炭, 表示方框中物质总能量(单位:
表示方框中物质总能量(单位: ),
), 表示过渡态。
表示过渡态。
①制备合成气总反应的 可表示为
可表示为_______  。
。
②若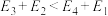 ,则决定速率步骤的化学方程式为
,则决定速率步骤的化学方程式为_______ 。
 、
、 、
、 是工业上重要的化工原料,回答下列问题:
是工业上重要的化工原料,回答下列问题:(1)
 的燃烧热为
的燃烧热为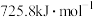 ,写出表示其燃烧热的热化学方程式:
,写出表示其燃烧热的热化学方程式:(2)如图表示的是
 和
和 反应生成
反应生成 和
和 过程中能量变化示意图,写出
过程中能量变化示意图,写出 和
和 反应的热化学方程式:
反应的热化学方程式:
(3)某些常见化学键的键能数据如下表:
| 化学键 |  |  |  |  |  |
键能 | 436 | 415 | 358 | 750 | 463 |
 □
□
 。
。(4)利用
 与
与 制备合成气
制备合成气 ,可能的反应历程如图所示:
,可能的反应历程如图所示: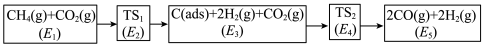
说明:
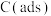 为吸附性活性炭,
为吸附性活性炭, 表示方框中物质总能量(单位:
表示方框中物质总能量(单位: ),
), 表示过渡态。
表示过渡态。①制备合成气总反应的
 可表示为
可表示为 。
。②若
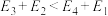 ,则决定速率步骤的化学方程式为
,则决定速率步骤的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高,DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量气压、浓度、pH、温度等而在化学实验研究中应用越来越广泛深入。将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中如图1,通过数字传感器测定实验中密闭容器(气密性良好)内压强与时间的关系如图2所示。
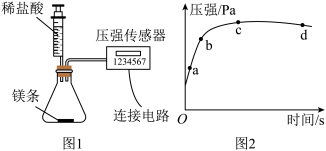
(1)镁条与稀盐酸反应为___________ (填“吸热”或“放热”)反应,图2中a、b、c、d四个点中,产生氢气最快的为___________ 点。
Ⅱ.向恒温恒容的密闭容器中,加入足量的碳和一定量NO,发生反应: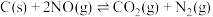 ,数字传感器测得CO2浓度随时间变化如表:
,数字传感器测得CO2浓度随时间变化如表:
(2)下列措施能加快反应速率的是___________。
(3)0~90s用NO来表示反应的平均速率为___________ 。
(4)下列能说明反应达到平衡状态的是___________。
(5)已知合成氨反应中,随温度升高氨的产率会下降。在实际生产中,选定的温度为400℃~500℃,为避免产率太低反应的温度不宜过高,但温度也不宜过低,原因是___________ 。除传统方法外,近几年科学家在研究利用原电池原理进行常温常压下合成氨。一种通过原电池进行合成氨的装置如图,在该装置中,电极a为___________ 极(填“正”或“负”),该电极的电极反应式为___________ 。

(6)合成氨反应可能的微观历程如图所示:
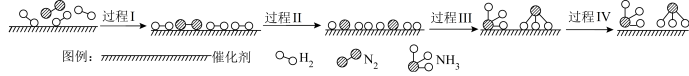
吸附在催化剂表面的物质用*标注。已知过程Ⅲ可以表示为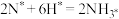 ,则过程Ⅱ可以表示为
,则过程Ⅱ可以表示为___________ 。

(1)镁条与稀盐酸反应为
Ⅱ.向恒温恒容的密闭容器中,加入足量的碳和一定量NO,发生反应:
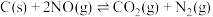 ,数字传感器测得CO2浓度随时间变化如表:
,数字传感器测得CO2浓度随时间变化如表:反应时间/ | 0 | 80 | 90 | 100 | 110 |
 浓度/( 浓度/( ) ) | 0.00 | 0.30 | 0.36 | 0.39 | 0.39 |
| A.及时分离出氮气 | B.升高反应体系温度 |
| C.使用高效催化剂 | D.在体系中通入氦气 |
(4)下列能说明反应达到平衡状态的是___________。
A. |
| B.容器内压强不再改变 |
| C.容器内气体的平均相对分子质量不再改变 |
| D.N2的体积分数不再改变 |

(6)合成氨反应可能的微观历程如图所示:

吸附在催化剂表面的物质用*标注。已知过程Ⅲ可以表示为
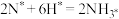 ,则过程Ⅱ可以表示为
,则过程Ⅱ可以表示为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】化学反应的快慢和限度对人类生产生活有重要的影响。
Ⅰ.某反应过程的能量变化如图所示:

(1)由图中曲线变化可知,该反应为___________ (填“放热”或“吸热”)反应,破坏旧键需要吸收的能量为___________ (填“ ”或“
”或“ ”)。
”)。
Ⅱ. 时,A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,该反应的正反应为放热反应。回答下列问题:
时,A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,该反应的正反应为放热反应。回答下列问题:
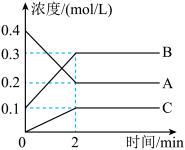
(2)该反应的反应物是___________ 。
(3) 内,C的反应速率为
内,C的反应速率为___________ 。
(4)在其他条件下,测得A的反应速率为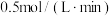 ,此时的反应速率与
,此时的反应速率与 时相比
时相比___________ 。
A.比 时慢 B.比
时慢 B.比 时快 C.和
时快 C.和 时速率一样
时速率一样
(5)能使该反应的反应速率增大的是___________。
Ⅲ.一种用于潜艇的液氨-液氧燃料电池原理示意图如下图所示。已知电池总电极反应为
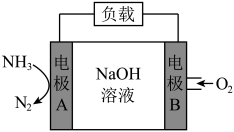
(6)电极B是___________ 极(填“正”或“负”)。
(7)该电池工作时,标况下每消耗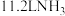 ,转移电子数为
,转移电子数为___________ 。
(8)电极A上发生的电极反应为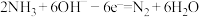 ;则电极B上发生的电极反应式为
;则电极B上发生的电极反应式为___________ 。
Ⅰ.某反应过程的能量变化如图所示:

(1)由图中曲线变化可知,该反应为
 ”或“
”或“ ”)。
”)。Ⅱ.
 时,A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,该反应的正反应为放热反应。回答下列问题:
时,A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,该反应的正反应为放热反应。回答下列问题:
(2)该反应的反应物是
(3)
 内,C的反应速率为
内,C的反应速率为(4)在其他条件下,测得A的反应速率为
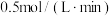 ,此时的反应速率与
,此时的反应速率与 时相比
时相比A.比
 时慢 B.比
时慢 B.比 时快 C.和
时快 C.和 时速率一样
时速率一样(5)能使该反应的反应速率增大的是___________。
| A.适当升高温度 | B.及时分离出 气体 气体 | C.适当降低温度 | D.选择高效的催化剂 |
Ⅲ.一种用于潜艇的液氨-液氧燃料电池原理示意图如下图所示。已知电池总电极反应为


(6)电极B是
(7)该电池工作时,标况下每消耗
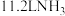 ,转移电子数为
,转移电子数为(8)电极A上发生的电极反应为
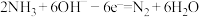 ;则电极B上发生的电极反应式为
;则电极B上发生的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室利用如图装置进行中和热的测定,请回答下列问题:
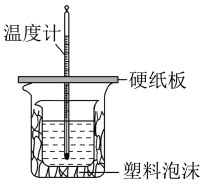
(1)从实验装置上看,图中尚缺少的玻璃用品是_______ 。
(2)在操作正确的前提下,提高中和热测定准确性的关键是_______ ;
(3)做一次完整的中和热测定实验,温度计需使用_______ 次;
(4)把温度为13℃,浓度为1.0mol/L的酸溶液和1.1mol/L的碱溶液各50mL混合[溶液密度均为1g/mL,生成溶液的比热容c=4.184J/(g·℃)],轻轻搅动,测得酸碱混合液的温度变化数据如表:
①计算上述两组实验测出的中和热:提示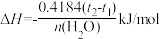 。△H1=
。△H1=_______ kJ/mol;△H2=_______ kJ/mol。
②两组实验结果差异的原因是_______ 。

(1)从实验装置上看,图中尚缺少的玻璃用品是
(2)在操作正确的前提下,提高中和热测定准确性的关键是
(3)做一次完整的中和热测定实验,温度计需使用
(4)把温度为13℃,浓度为1.0mol/L的酸溶液和1.1mol/L的碱溶液各50mL混合[溶液密度均为1g/mL,生成溶液的比热容c=4.184J/(g·℃)],轻轻搅动,测得酸碱混合液的温度变化数据如表:
| 反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热 |
| HCl+NaOH | 13 | 19.8 | △H1 |
| HCl+NH3·H2O | 13 | 19.3 | △H2 |
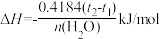 。△H1=
。△H1=②两组实验结果差异的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】反应热的数值可以通过理论计算得出,也可以通过实验测得。某实验探究小组用 的NaOH溶液和
的NaOH溶液和 的硫酸溶液进行中和反应的反应热的测定。
的硫酸溶液进行中和反应的反应热的测定。

(1)若实验中需要使用250 mL NaOH溶液,则在配制时应称量NaOH固体___________ g。
(2)从实验装置上看,还缺少___________ ,装置中隔热层的作用是___________ 。利用上述NaOH溶液和硫酸溶液反应测定中和反应的反应热的实验装置如图所示。
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表:
①近似认为 的NaOH溶液和
的NaOH溶液和 的硫酸溶液的密度都是
的硫酸溶液的密度都是 ,反应后所得溶液的比热容为4.18 J/(g℃)。则该中和反应生成1 mol水时反应热△H=
,反应后所得溶液的比热容为4.18 J/(g℃)。则该中和反应生成1 mol水时反应热△H=___________ (计算结果精确到小数点后一位)。若用30 mL1 mol/L醋酸代替H2SO4溶液进行上述实验,测得反应后的△H___________ (填“偏大”“偏小”或“不受影响”)。
②上述实验结果与理论值(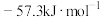 )有偏差,产生偏差的原因不可能是
)有偏差,产生偏差的原因不可能是___________ (填序号)。
A.实验装置保温、隔热效果差
B.用温度计测量最高温度时俯视读数
C.用温度计测定过NaOH溶液的起始温度后,直接测定硫酸溶液的温度
D.把NaOH溶液分多次倒入盛有硫酸溶液的小烧杯中
 的NaOH溶液和
的NaOH溶液和 的硫酸溶液进行中和反应的反应热的测定。
的硫酸溶液进行中和反应的反应热的测定。
(1)若实验中需要使用250 mL NaOH溶液,则在配制时应称量NaOH固体
(2)从实验装置上看,还缺少
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表:
| 实验次数 | 起始温度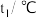 | 最高温度 | ||
| 硫酸溶液 | NaOH溶液 | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.5 |
| 2 | 25.9 | 25.9 | 25.9 | 30.5 |
| 3 | 26.0 | 26.2 | 26.1 | 32 |
 的NaOH溶液和
的NaOH溶液和 的硫酸溶液的密度都是
的硫酸溶液的密度都是 ,反应后所得溶液的比热容为4.18 J/(g℃)。则该中和反应生成1 mol水时反应热△H=
,反应后所得溶液的比热容为4.18 J/(g℃)。则该中和反应生成1 mol水时反应热△H=②上述实验结果与理论值(
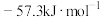 )有偏差,产生偏差的原因不可能是
)有偏差,产生偏差的原因不可能是A.实验装置保温、隔热效果差
B.用温度计测量最高温度时俯视读数
C.用温度计测定过NaOH溶液的起始温度后,直接测定硫酸溶液的温度
D.把NaOH溶液分多次倒入盛有硫酸溶液的小烧杯中
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】用100mL 1.00mol·L-1盐酸与100mL 1.10mol·L-1NaOH溶液在如下图所示的装置中进行中和热测定实验。以下是四次实验所得数据。回答下列问题:
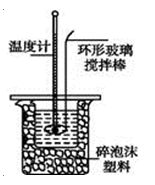
(1)上表中的温度差平均值为__________ ℃
(2)近似认为上述两种溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18J·(g·℃)-1。则计算得到中和热ΔH=_________ (取小数点后一位)。
(3)上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母)___________ 。
a.实验装置保温、隔热效果差
b.用环形铜质搅拌棒代替环形玻璃搅拌棒
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定盐酸溶液起始温度后直接测定NaOH溶液的温度

| 实验数据 | 盐酸起始温度t1/℃ | 氢氧化钠起始温度t2/℃ | 两溶液混合后温度t3/℃ |
| 1 | 21.0 | 21.1 | 26.9 |
| 2 | 21.5 | 21.7 | 28.2 |
| 3 | 21.9 | 22.1 | 28.7 |
| 4 | 22.3 | 22.5 | 29.2 |
(2)近似认为上述两种溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18J·(g·℃)-1。则计算得到中和热ΔH=
(3)上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差
b.用环形铜质搅拌棒代替环形玻璃搅拌棒
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定盐酸溶液起始温度后直接测定NaOH溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
回答下列问题:
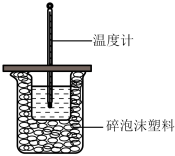
(1)实验中大约要使用230 mL NaOH溶液,配制溶液时至少需要称量NaOH固体____________ g。
(2) 从实验装置上看,图中尚缺少的一种玻璃仪器是__________________ ,烧杯间填满碎泡沫塑料的作用是________________________________ 。
(3)大烧杯上如不盖硬纸板,则求得的中和热数值________ (填“偏大”、“偏小”或“无影响”)。
(4)实验中若改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量________ (填“相等”或“不相等”),所求中和热的数值___________ (填“相等”或“不相等”),理由是_______________________________ 。
(5)三次平行操作测得的数据中,起始时盐酸与烧碱溶液温度相同,而终止温度与起始温度之差(t2-t1)分别为3.3 ℃、3.4 ℃、3.9 ℃,各溶液的密度均为1 g /cm3,生成溶液的比热容C=4.18 J /(g· oC),则最终计算上述实验测出的中和热ΔH1=______________ 。
(6)若用氨水代替NaOH溶液做实验,测定结果ΔH会_____ (填“偏大”“偏小”或“无影响”)
(7)上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是________ (填字母)。
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
c.量取NaOH溶液的体积时仰视读数
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度
回答下列问题:

(1)实验中大约要使用230 mL NaOH溶液,配制溶液时至少需要称量NaOH固体
(2) 从实验装置上看,图中尚缺少的一种玻璃仪器是
(3)大烧杯上如不盖硬纸板,则求得的中和热数值
(4)实验中若改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
(5)三次平行操作测得的数据中,起始时盐酸与烧碱溶液温度相同,而终止温度与起始温度之差(t2-t1)分别为3.3 ℃、3.4 ℃、3.9 ℃,各溶液的密度均为1 g /cm3,生成溶液的比热容C=4.18 J /(g· oC),则最终计算上述实验测出的中和热ΔH1=
(6)若用氨水代替NaOH溶液做实验,测定结果ΔH会
(7)上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
c.量取NaOH溶液的体积时仰视读数
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 H2SO4溶液进行中和热的测定。测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示:
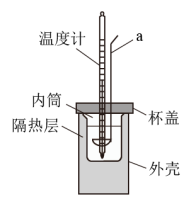
(1)仪器a的名称为___________ 。
(2)写出表示该反应中和热的热化学方程式:___________ 。
(3)步骤三中倒入NaOH溶液的正确操作是___________ 。
A. 沿玻璃棒缓慢倒入 B. 分三次少量倒入 C. 一次迅速倒入
(4)使硫酸与NaOH溶液混合均匀的正确操作是___________(填序号)。
(5)取50 mL NaOH溶液和30 mL H2SO4溶液进行实验,实验数据如下表。
①温度差的平均值为___________ ℃。
②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 H2SO4溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·(g·℃)-1.则测得的中和热ΔH=___________ (取小数点后一位)。
③上述结果与57.3 kJ·mol-1有偏差,产生此偏差的原因可能是___________ (填字母)。
a. 实验装置保温、隔热效果差
b. 量取NaOH溶液的体积时仰视读数
c. 一次性把NaOH溶液倒入盛有H2SO4溶液的小烧杯中
d. 用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度

(1)仪器a的名称为
(2)写出表示该反应中和热的热化学方程式:
(3)步骤三中倒入NaOH溶液的正确操作是
A. 沿玻璃棒缓慢倒入 B. 分三次少量倒入 C. 一次迅速倒入
(4)使硫酸与NaOH溶液混合均匀的正确操作是___________(填序号)。
| A.轻轻地振荡烧杯 | B.揭开硬纸片用玻璃棒搅拌 |
| C.用温度计小心搅拌 | D.用套在温度计上的a轻轻地搅动 |
| 实验 次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.6 | 26.6 | 26.6 | 29.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 H2SO4溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·(g·℃)-1.则测得的中和热ΔH=
③上述结果与57.3 kJ·mol-1有偏差,产生此偏差的原因可能是
a. 实验装置保温、隔热效果差
b. 量取NaOH溶液的体积时仰视读数
c. 一次性把NaOH溶液倒入盛有H2SO4溶液的小烧杯中
d. 用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 硫酸溶液进行中和热的测定。
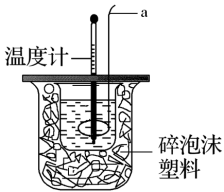
(1)测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示,其中仪器a的名称为_____________ ;
(2)写出该反应中和热的热化学方程式(中和热为57.3 kJ·mol-1)______________ ;
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
① 请填写下表中的空白:
② 近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18kJ·(kg·℃)-1。则中和热ΔH=________________________ (取小数点后一位);
③ 上述实验数据结果与57.3 kJ·mol-1有偏差, 产生偏差的原因不可能是(填字母)________ 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度

(1)测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示,其中仪器a的名称为
(2)写出该反应中和热的热化学方程式(中和热为57.3 kJ·mol-1)
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
① 请填写下表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 26.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
② 近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18kJ·(kg·℃)-1。则中和热ΔH=
③ 上述实验数据结果与57.3 kJ·mol-1有偏差, 产生偏差的原因不可能是(填字母)
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)某同学设计了如下实验流程:在一个小烧杯里,加入20g Ba(OH)2·8H2O晶体和10gNH4Cl晶体,然后将小烧杯放在事先已滴有3滴~4滴水的玻璃片上,并立即用玻璃棒迅速搅拌。实验流程示意图如下,回答下列问题:
①实验中玻璃棒的作用是_______ 。
②浸有稀硫酸的棉花的作用是______ 。
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,可用来点火做饭。在农村推广建造沼气池,不仅能有效地利用____ 能,还能为农业生产提供优良的肥料。已知:标准状况下的112.0LCH4气体完全燃烧,生成CO2和液态水,放出4448kJ的热量。
①写出CH4完全燃烧的热化学方程式为________ 。
②如果上述反应生成的是水蒸气,则反应放出的热量___ 4448kJ。(填“>”或“<”或“=”)
(3)钢铁在潮湿的空气中生锈主要是由电化学腐蚀造成的,发生腐蚀时铁和内部的杂质碳及钢铁表面的电解质溶液形成原电池。钢铁发生吸氧腐蚀时正极的电极反应式________ 。
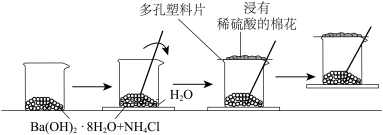
①实验中玻璃棒的作用是
②浸有稀硫酸的棉花的作用是
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,可用来点火做饭。在农村推广建造沼气池,不仅能有效地利用
①写出CH4完全燃烧的热化学方程式为
②如果上述反应生成的是水蒸气,则反应放出的热量
(3)钢铁在潮湿的空气中生锈主要是由电化学腐蚀造成的,发生腐蚀时铁和内部的杂质碳及钢铁表面的电解质溶液形成原电池。钢铁发生吸氧腐蚀时正极的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】二甲醚(CH3OCH3)常用作溶剂、冷冻剂、喷雾剂等,易燃烧。 回答下列问题:
(1)25 ℃、101 kPa时,92g气态二甲醚完全燃烧生成CO2(g)、H2O(l)放出 2912 kJ热量,则表示气态二甲醚燃烧 热的热化学方程式为___________ 。当 CH3OCH3(g)完全燃烧生成 CO2(g)、H2O(l)放出 728 kJ热量时,转移的电子数为___________ (用NA 表示阿伏加德罗常数的值)。
(2)已知 H2(g)和CO(g)的燃烧热 △H 分别是
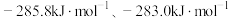
 则反应
则反应
 的反应热△H =
的反应热△H =___________
 。
。
(3)在 2 L 的恒容密闭容器中,充入 6 mol H2 和2 mol CO2合成二甲醚,其反应为
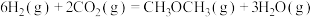 ,在不同温度下,5min时,水蒸气的体积分数如图所示。
,在不同温度下,5min时,水蒸气的体积分数如图所示。
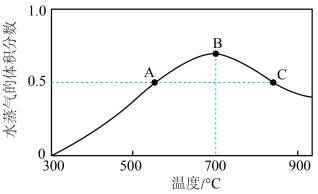
①该反应的 △H=___________ 0(填“>”“<”或“=”)。
②A 点 CO2的逆反应速率___________ (填“>”“<”或“=”)B点 CO2 的逆反应速率;A点对应温度下,0 ~ 5 min 内,平均反应速率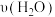 =
=____________ 。
③B点的平衡常数___________ (填“>”“<”或“=”)C点的平衡常数。
(1)25 ℃、101 kPa时,92g气态二甲醚完全燃烧生成CO2(g)、H2O(l)放出 2912 kJ热量,则表示气态二甲醚燃
(2)已知 H2(g)和CO(g)的燃烧热 △H 分别是
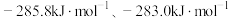
 则反应
则反应 的反应热△H =
的反应热△H = 。
。(3)在 2 L 的恒容密闭容器中,充入 6 mol H2 和2 mol CO2合成二甲醚,其反应为
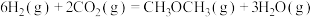 ,在不同温度下,5min时,水蒸气的体积分数如图所示。
,在不同温度下,5min时,水蒸气的体积分数如图所示。
①该反应的 △H=
②A 点 CO2的逆反应速率
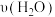 =
=③B点的平衡常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】(1)已知H2S的燃烧热ΔH=-akJ·mol-1,写出表示H2S燃烧反应的热化学方程式__ ,表示H2S燃烧热的热化学方程式__ 。
(2)若将FeCl3溶液蒸干灼烧,最后得到的固体产物主要是__ (填化学式)。FeCl3水溶液呈__ (填“酸”、“中”、“碱”)性,原因为:__ (用离子方程式表示)。
(3)炒过菜的铁锅未及时洗净(残液中有NaCl),第二天便会被腐蚀而出现红褐色铁锈,试回答:铁锅的腐蚀属于电化腐蚀,其原因是__ 。此时铁锅锈蚀主要是吸氧腐蚀,电极反应方程式为:负极:__ ,正极__ 。
(4)估计下列各变化过程是熵增加还是熵减小。(用A、B、C填空)
NH4NO3爆炸:2NH4NO3(s)=2N2(g)+4H2O(g)+O2(g)__
水煤气转化:CO(g)+H2O(g)=CO2(g)+H2(g)__
臭氧的生成:3O2(g)=2O3(g)__
A.熵增大 B.熵减小 C.熵变很小
(2)若将FeCl3溶液蒸干灼烧,最后得到的固体产物主要是
(3)炒过菜的铁锅未及时洗净(残液中有NaCl),第二天便会被腐蚀而出现红褐色铁锈,试回答:铁锅的腐蚀属于电化腐蚀,其原因是
(4)估计下列各变化过程是熵增加还是熵减小。(用A、B、C填空)
NH4NO3爆炸:2NH4NO3(s)=2N2(g)+4H2O(g)+O2(g)
水煤气转化:CO(g)+H2O(g)=CO2(g)+H2(g)
臭氧的生成:3O2(g)=2O3(g)
A.熵增大 B.熵减小 C.熵变很小
您最近一年使用:0次



