在下列探究实验中,探究方案设计有错误的是
| 选项 | 探究方案 | 探究目的 |
| A | 向盛有Fe2+溶液的试管中滴加几滴KSCN溶液,振荡,再滴加几滴新制氯水,观察溶液颜色变化 | Fe2+具有还原性 |
| B | 向铜与浓硫酸反应后的试管加水,观察溶液颜色 | Cu与浓H2SO4反应的氧化产物 |
| C | 向盛有淀粉KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 | Br2的氧化性比I2的强 |
| D | 用pH计测量0.10mol/LH3PO4的pH=3.12 | 磷酸是弱电解质 |
| A.A | B.B | C.C | D.D |
2023·江西景德镇·三模 查看更多[3]
更新时间:2023-05-05 22:11:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意如下。下列说法错误的是
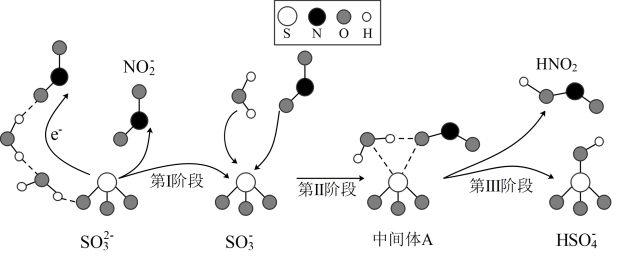

A.第II、III阶段总反应的离子方程式为: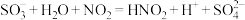 |
B.该过程中 为催化剂 为催化剂 |
C.第I阶段每1mol氧化剂参加反应,转移电子数目为 |
D.还原性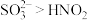 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知还原性:SO32->I->Br-。过量的氯气通入NaBr、NaI、Na2SO3混合液中,将溶液蒸干并充分灼烧后,得到的物质可能是
| A.NaCl、Na2SO4 | B.NaBr、Na2SO4 | C.NaCl、Na2SO3 | D.NaCl、Br2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验事实能证明相应结论的是
| 选项 | 实验事实 | 相应结论 |
| A | 铜分别与浓硝酸、稀硝酸反应时,还原产物NO2比NO中氮元素的价态高 | 浓硝酸得电子能力差,氧化性比稀硝酸弱 |
| B | 磷酸与Na2SO3固体在加热条件下反应生成SO2 | 磷酸的酸性比亚硫酸强 |
| C | 其他条件相同时,1mol/L的醋酸比0.5mol/L的醋酸导电能力弱 | 电解质的电离不需要通电 |
| D | 浓盐酸与MnO2混合加热生成氯气,氯气不再逸出时,固体混合物中仍存在盐酸和MnO2 | 物质浓度影响其氧化性或还原性的强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】宏观辨识与微观探析是化学学科核心素养之一,下列方程式能正确解释相应事实的是
A.用Cu作电极电解饱和食盐水:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
B.向饱和Na2CO3溶液中通入CO2气体:CO2+H2O+  =2 =2 |
C.向碘化亚铁溶液中滴加少量稀硝酸:2 +3Fe2++4H+=3Fe3++2NO↑+2H2O +3Fe2++4H+=3Fe3++2NO↑+2H2O |
| D.用K3[Fe(CN)6]溶液检验亚铁离子: K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】欲除去FeCl3溶液中少量的FeCl2,可行的办法…………………………
| A.滴入KSCN | B.通入氯气 | C.加入铁粉 | D.加入铜粉 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法一定正确的是
A.25℃时,向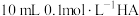 溶液中加入 溶液中加入 的NaOH溶液,当水电离出的 的NaOH溶液,当水电离出的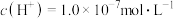 时,滴加氢氧化钠溶液的体积可能出现两种情况,则HA为弱酸 时,滴加氢氧化钠溶液的体积可能出现两种情况,则HA为弱酸 |
| B.常温下,将pH=2的一元酸HA溶液与pH=12的一元碱BOH溶液等体积混合,所得溶液pH=7 |
C.相同温度下, 的NaCl溶液和 的NaCl溶液和 的NaCN溶液中的离子总数相等 的NaCN溶液中的离子总数相等 |
D.将冰醋酸加水稀释,冰醋酸的电离度逐渐增加,但电离常数Ka不变, 逐渐增大,导电性逐渐增强 逐渐增大,导电性逐渐增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.常温下,用湿润的pH试纸测得0.01mol/L的HCl水溶液的pH为2 |
| B.常温下,0.1mol/LCH3COONa溶液的pH>7,说明CH3COOH是弱酸 |
| C.常温下,pH=1的强酸溶液,加水稀释后,溶液中各离子浓度都会降低 |
| D.常温下,pH=3的酸与pH=11的碱等体积混合所得溶液一定显中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验方案能达到实验目的的是
| A.用盐酸酸化的硝酸银溶液鉴别自来水和蒸馏水 |
| B.用分液漏斗分离氯水与酒精的混合物 |
| C.将Cl2分别通入放有干燥和湿润的有色布条的广口瓶探究漂白原理 |
| D.用饱和NaOH溶液除去Cl2气体中混有的少量HCl气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向苯酚钠溶液中通足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
| B | 加热乙醇与浓硫酸的混合溶液,将产生的气体通入少量酸性KMnO4溶液,溶液紫红色褪去 | 有乙烯生成 |
| C | 向2mL0.1mol·L–1NaOH溶液中滴加3滴0.1mol·L–1MgCl2溶液,出现白色沉淀后,再滴加3滴0.1mol·L–1FeCl3溶液,出现红褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 向NaHCO3溶液中滴加紫色石蕊试液,溶液变蓝 | Kw<Ka1(H2CO3)×Ka2(H2CO3) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次






