Ⅰ.按要求回答下列问题:
(1)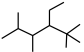 的系统命名为
的系统命名为___________ 。
(2)下列物质的熔沸点由高到低的排序为___________ (填序号)。
① 甲基丁烷②2,
甲基丁烷②2,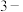 二甲基丁烷③2,
二甲基丁烷③2,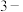 二甲基丙烷④正戊烷⑤
二甲基丙烷④正戊烷⑤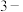 甲基戊烷
甲基戊烷
(3)丙烯使溴的四氯化碳溶液褪色的化学方程式为___________ 。
Ⅱ.氮元素是重要的非金属元素,可形成卤化氮、氮化物、叠氮化物及配合物等多种化合物。
(4)请写出基态氮原子的电子排布图___________ 。
(5) 的沸点由高到低的顺序是
的沸点由高到低的顺序是___________ 。
(6) 与
与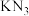 相比,
相比, 的晶格能
的晶格能___________ (填“>”、“=”或“<”)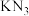 的晶格能。
的晶格能。
(7)某元素X形成的离子 中K、L、M三个电子层均充满了电子。它与
中K、L、M三个电子层均充满了电子。它与 形成晶体的结构如图所示。
形成晶体的结构如图所示。 的符号是
的符号是___________ ,晶体中距离每个 最近的
最近的 有
有___________ 个。

(1)
 的系统命名为
的系统命名为(2)下列物质的熔沸点由高到低的排序为
①
 甲基丁烷②2,
甲基丁烷②2,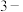 二甲基丁烷③2,
二甲基丁烷③2,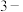 二甲基丙烷④正戊烷⑤
二甲基丙烷④正戊烷⑤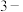 甲基戊烷
甲基戊烷(3)丙烯使溴的四氯化碳溶液褪色的化学方程式为
Ⅱ.氮元素是重要的非金属元素,可形成卤化氮、氮化物、叠氮化物及配合物等多种化合物。
(4)请写出基态氮原子的电子排布图
(5)
 的沸点由高到低的顺序是
的沸点由高到低的顺序是(6)
 与
与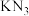 相比,
相比, 的晶格能
的晶格能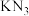 的晶格能。
的晶格能。(7)某元素X形成的离子
 中K、L、M三个电子层均充满了电子。它与
中K、L、M三个电子层均充满了电子。它与 形成晶体的结构如图所示。
形成晶体的结构如图所示。 的符号是
的符号是 最近的
最近的 有
有
更新时间:2023-04-23 14:46:08
|
相似题推荐
【推荐1】用系统命名法命名下列有机物:
(1)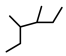
_______
(2)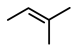
_______
(3)
_______
(1)

(2)

(3)

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识回答下列问题:
(1)碳化钙电子式:_______ 。
(2)用系统命名法命名 为
为_______ 。
(3) 甲基
甲基 乙基
乙基 ,
,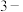 戊二烯的结构简式是
戊二烯的结构简式是_______ 。
(4)分子式为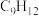 的芳香烃,苯环上的一溴取代物只有一种,该芳香烃的名称为
的芳香烃,苯环上的一溴取代物只有一种,该芳香烃的名称为_______ 。
(1)碳化钙电子式:
(2)用系统命名法命名
 为
为(3)
 甲基
甲基 乙基
乙基 ,
,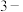 戊二烯的结构简式是
戊二烯的结构简式是(4)分子式为
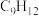 的芳香烃,苯环上的一溴取代物只有一种,该芳香烃的名称为
的芳香烃,苯环上的一溴取代物只有一种,该芳香烃的名称为
您最近半年使用:0次
【推荐3】有机物的结构简式可进一步简化,如:CH3CH2CH2CH3: ;
;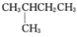 :
: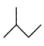 ;CH3CH=CHCH3:
;CH3CH=CHCH3: 。
。
(1)写出下列有机物的结构简式:2,2,3,3-四甲基戊烷:___________ ;3,4-二甲基-4-乙基庚烷:___________ 。
(2)写出下列物质的分子式: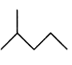 :
:___________ ;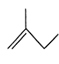 :
:___________ 。
(3)用系统命名法命名下列物质: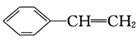
___________ ;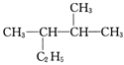
___________ ;
(4)写出新制的银氨溶液与乙醛的化学方程式___________ 。
 ;
;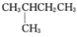 :
: ;CH3CH=CHCH3:
;CH3CH=CHCH3: 。
。(1)写出下列有机物的结构简式:2,2,3,3-四甲基戊烷:
(2)写出下列物质的分子式:
 :
: :
:(3)用系统命名法命名下列物质:
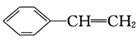

(4)写出新制的银氨溶液与乙醛的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下几种有机物:
① ②
② ③
③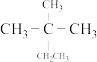 ④
④ ⑤
⑤
⑥ ⑦
⑦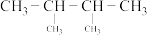 ⑧
⑧ ⑨
⑨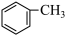
请利用上述给出的物质按要求回答下列问题:
(1)③的系统命名是________ 。
(2)用“>”表示①③④⑧熔沸点高低顺序:________ (填序号)。
(3)与③互为同系物的是________ (填序号)。
(4)⑨的一氯代物同分异构体数目有________ 种。
(5)在120℃, 条件下,某种气态烃与足量的
条件下,某种气态烃与足量的 完全反应后,测得反应前后气体的体积没有发生改变,则该烃是
完全反应后,测得反应前后气体的体积没有发生改变,则该烃是________ (填序号)。
(6)写出⑥在铁作催化剂的条件下与液溴发生取代反应的化学方程式________ 。
①
 ②
② ③
③ ④
④ ⑤
⑤
⑥
 ⑦
⑦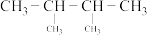 ⑧
⑧ ⑨
⑨
请利用上述给出的物质按要求回答下列问题:
(1)③的系统命名是
(2)用“>”表示①③④⑧熔沸点高低顺序:
(3)与③互为同系物的是
(4)⑨的一氯代物同分异构体数目有
(5)在120℃,
 条件下,某种气态烃与足量的
条件下,某种气态烃与足量的 完全反应后,测得反应前后气体的体积没有发生改变,则该烃是
完全反应后,测得反应前后气体的体积没有发生改变,则该烃是(6)写出⑥在铁作催化剂的条件下与液溴发生取代反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列七种有机物:① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦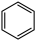 请回答:
请回答:
(1)写出⑤的官能团的名称_______ 。
(2)与①互为同系物的是_______ (填序号)。
(3)与④互为同分异构体的是_______ (填序号)。
(4)①④⑥熔沸点由高到低的顺序为:_______ 。
(5)写出③与⑤发生反应的化学方程式_______ 。
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 请回答:
请回答:(1)写出⑤的官能团的名称
(2)与①互为同系物的是
(3)与④互为同分异构体的是
(4)①④⑥熔沸点由高到低的顺序为:
(5)写出③与⑤发生反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】习惯命名法:用“正”“异”“新”来区分烷烃
(1)丁烷有两种即___________ 和___________ ,结构简式分别为___________ 和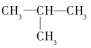 。
。
(2)戊烷有三种,即___________ 、___________ 、___________ ,其结构简式分别为___________ 、___________ 、_______________ 。
(3)正戊烷、异戊烷、新戊烷的沸点逐渐___________ ,原因是同种烷烃的不同异构体中,支链___________ 其沸点___________ 。
(1)丁烷有两种即
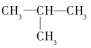 。
。(2)戊烷有三种,即
(3)正戊烷、异戊烷、新戊烷的沸点逐渐
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求完成:
(1)基态O2-离子核外电子排布式___________
(2)基态P原子核外电子排布式___________
(3)基态Al原子核外电子排布式___________
(4)基态As原子核外电子排布图___________
(5)基态Fe3+核外电子排布图___________
(6)基态V原子价电子排布图___________
(7)基态Se原子价电子排布图___________
(1)基态O2-离子核外电子排布式
(2)基态P原子核外电子排布式
(3)基态Al原子核外电子排布式
(4)基态As原子核外电子排布图
(5)基态Fe3+核外电子排布图
(6)基态V原子价电子排布图
(7)基态Se原子价电子排布图
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】短周期元素A、B、C、D、E在元素周期表位置如下图所示,其中B元素最外层有两个未成对电子。回答下列问题:
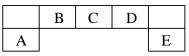
(1)E元素原子的价电子轨道表示式为_____
(2)比较A、D元素简单离子半径的大小:_____ (用微粒符号表示)。
(3)F与D同主族且相邻,比较D的氢化物和F的氢化物稳定性大小:_____ (用化学式表示)。

(1)E元素原子的价电子轨道表示式为
(2)比较A、D元素简单离子半径的大小:
(3)F与D同主族且相邻,比较D的氢化物和F的氢化物稳定性大小:
您最近半年使用:0次
填空题
|
适中
(0.65)
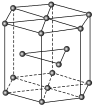
【推荐1】金属Zn晶体中的原子堆积方式如图所示,六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为___ g·cm-3(列出计算式)。

您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大 晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、·表示
晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、·表示 和
和 ,
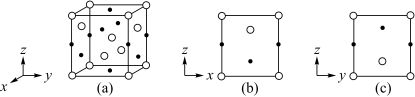
, 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是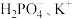 在晶胞
在晶胞 面、
面、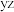 面上的位置。
面上的位置。
(1)若晶胞底边的边长均为 、高为
、高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶体的密度为
,晶体的密度为_______  (写出含
(写出含 、a、c的表达式)。
、a、c的表达式)。
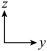
(2)晶胞在x轴方向的投影图为_______(填标号)。
 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大 晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、·表示
晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、·表示 和
和 ,
, 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是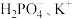 在晶胞
在晶胞 面、
面、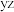 面上的位置。
面上的位置。
(1)若晶胞底边的边长均为
 、高为
、高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶体的密度为
,晶体的密度为 (写出含
(写出含 、a、c的表达式)。
、a、c的表达式)。(2)晶胞在x轴方向的投影图为_______(填标号)。

A.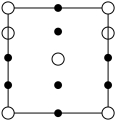 | B. |
C.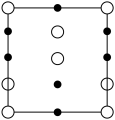 | D. |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】随着科学的发展,氟及其化合物的用途日益广泛。
Ⅰ.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如下图。
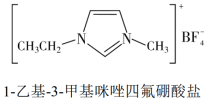
(1)写出基态铜原子的价电子排布式___________ 。H、O、C电负性由大到小的顺序___________ 。
(2)NaBF4是制备此离子液体的原料。
①微粒中F—B—F键角:BF3___________ BF (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②BF3可以与NaF反应生成NaBF4的原因是_________ 。
(3)以Cu(BF4)2和[Emim]BF4的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为___________ ,电解质溶液中Cu2+向___________ (填“阴”或“阳”)极移动。
(4)铜—镍镀层能增强材料的耐蚀性,镍在周期表中的位置为:___________ 。按照核外电子排布,把元素周期表划分为5个区,Ni位于___________ 区。从价电子排布的角度解释Ni位于元素周期表该区的原因:___________ 。
Ⅱ.NaF等氟化物可以做光导纤维材料,一定条件下,某NaF的晶胞结构如下图。
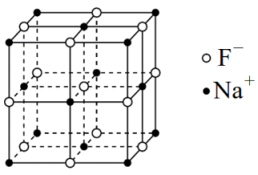
(5)与F-距离最近且相等的Na+有___________ 个。
(6)NA表示阿伏加德罗常数的值。NaF晶胞为正方体,边长为anm,则晶体的摩尔体积Vm=___________ m3·mol-1。(nm=10-9m)
(7)下图所示结构单元不能作为NaF晶胞的原因是___________ 。

Ⅰ.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如下图。

(1)写出基态铜原子的价电子排布式
(2)NaBF4是制备此离子液体的原料。
①微粒中F—B—F键角:BF3
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②BF3可以与NaF反应生成NaBF4的原因是
(3)以Cu(BF4)2和[Emim]BF4的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为
(4)铜—镍镀层能增强材料的耐蚀性,镍在周期表中的位置为:
Ⅱ.NaF等氟化物可以做光导纤维材料,一定条件下,某NaF的晶胞结构如下图。

(5)与F-距离最近且相等的Na+有
(6)NA表示阿伏加德罗常数的值。NaF晶胞为正方体,边长为anm,则晶体的摩尔体积Vm=
(7)下图所示结构单元不能作为NaF晶胞的原因是

您最近半年使用:0次



