按要求完成:
(1)基态O2-离子核外电子排布式___________
(2)基态P原子核外电子排布式___________
(3)基态Al原子核外电子排布式___________
(4)基态As原子核外电子排布图___________
(5)基态Fe3+核外电子排布图___________
(6)基态V原子价电子排布图___________
(7)基态Se原子价电子排布图___________
(1)基态O2-离子核外电子排布式
(2)基态P原子核外电子排布式
(3)基态Al原子核外电子排布式
(4)基态As原子核外电子排布图
(5)基态Fe3+核外电子排布图
(6)基态V原子价电子排布图
(7)基态Se原子价电子排布图
21-22高二上·宁夏石嘴山·期中 查看更多[2]
(已下线)第1.1.3讲 泡利原理、洪特规则、能量最低原理 -2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)宁夏石嘴山市第三中学2021-2022学年高二上学期期中考试化学试题
更新时间:2021-12-03 12:27:12
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】金属钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,主要步骤如下:
Ⅰ.即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C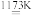 2TiCl4+2FeCl3+6CO
2TiCl4+2FeCl3+6CO
TiO2+2Cl2+2C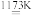 TiCl4+2CO
TiCl4+2CO
Ⅱ.将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg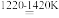 Ti+2MgCl2
Ti+2MgCl2
Ⅲ.用稀盐酸溶解MgCl2和过量Mg后得海绵状钛,再在真空熔化铸成钛锭。
请回答下列问题:
(1)基态钛原子的价电子排布式为___ 。
(2)与CO互为等电子体的离子为___ (填化学式)。
(3)在CH2Cl2、HCHO、CO2、C2H4中,碳原子采取sp2杂化的分子有___ 。
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于___ (填“原子”“分子”或“离子”)晶体。
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是___ ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为___ 。
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为___ 。

Ⅰ.即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C
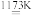 2TiCl4+2FeCl3+6CO
2TiCl4+2FeCl3+6COTiO2+2Cl2+2C
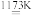 TiCl4+2CO
TiCl4+2COⅡ.将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg
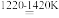 Ti+2MgCl2
Ti+2MgCl2Ⅲ.用稀盐酸溶解MgCl2和过量Mg后得海绵状钛,再在真空熔化铸成钛锭。
请回答下列问题:
(1)基态钛原子的价电子排布式为
(2)与CO互为等电子体的离子为
(3)在CH2Cl2、HCHO、CO2、C2H4中,碳原子采取sp2杂化的分子有
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请完成下列各题的填空:
(1)氢化钠(NaH)电子式为___________ ,氢负离子的离子结构示意图为___________ 。
(2)基态砷原子价层电子的电子排布式为___________ ,基态砷原子的核外有___________ 个未成对电子,基态砷原子电子占据最高能级的电子云轮廓图为___________ 形;
(3)第一电离能As___________ Se 填“
填“ ”或“
”或“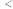 ”
” ,原因是
,原因是___________ 。
(4)亚硒酸根离子 的VSEPR模型为
的VSEPR模型为___________ ,其中心原子的轨道杂化方式为___________ 。
(5)向硫酸铜溶液中逐滴加入氨水至得到蓝色透明溶液后,再加入极性较小的溶剂乙醇,析出深蓝色晶体 ,该晶体中中心离子为
,该晶体中中心离子为___________ ,配离子中的配位体为___________ ,配位数为___________ 。
(6)有机砷 是治疗昏睡病不可缺少的药物,该有机砷中存在的化学键的种类为
是治疗昏睡病不可缺少的药物,该有机砷中存在的化学键的种类为___________  填字母编号
填字母编号 。
。
a.离子键 b. 键 c.
键 c. 键 d.碳碳双键
键 d.碳碳双键
(1)氢化钠(NaH)电子式为
(2)基态砷原子价层电子的电子排布式为
(3)第一电离能As
 填“
填“ ”或“
”或“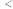 ”
” ,原因是
,原因是(4)亚硒酸根离子
 的VSEPR模型为
的VSEPR模型为(5)向硫酸铜溶液中逐滴加入氨水至得到蓝色透明溶液后,再加入极性较小的溶剂乙醇,析出深蓝色晶体
 ,该晶体中中心离子为
,该晶体中中心离子为(6)有机砷
 是治疗昏睡病不可缺少的药物,该有机砷中存在的化学键的种类为
是治疗昏睡病不可缺少的药物,该有机砷中存在的化学键的种类为 填字母编号
填字母编号 。
。a.离子键 b.
 键 c.
键 c. 键 d.碳碳双键
键 d.碳碳双键
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色。
(1)Cu的价电子轨道表达式为____ ;在周期表中,Cu元素属于___________ 区。
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解,写出沉淀溶解的离子方程式:___________ 。
(3)向深蓝色溶液继续加入___________ ,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。[Cu(NH3)4]SO4·H2O中,1mol[Cu(NH3)4] 2+含有σ键的数目为___________ 。
(4)___________ (填“H2O”或“NH3”)与Cu2+形成的配位键更稳定。
(5)SO 的VSEPR模型名称为
的VSEPR模型名称为___________ ,H3O+空间构型为___________ 。
(6)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如下图所示。
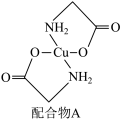
该结构中,除共价键外还存在配位键,请在图中用“→”表示出配位键___________ 。
(1)Cu的价电子轨道表达式为
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解,写出沉淀溶解的离子方程式:
(3)向深蓝色溶液继续加入
(4)
(5)SO
 的VSEPR模型名称为
的VSEPR模型名称为(6)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如下图所示。

该结构中,除共价键外还存在配位键,请在图中用“→”表示出配位键
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题。
(1)Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ 、___________ (填标号)。
A. B.
B.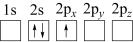
C. D.
D.
(3)基态Fe原子价层电子的电子排布图(轨道表达式)为___________ ,基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(1)Fe成为阳离子时首先失去
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(3)基态Fe原子价层电子的电子排布图(轨道表达式)为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】微量元素硼对植物生长及人体健康有着十分重要的作用,也广泛应用于新型材料的制备。
(1)基态硼原子的价电子轨道表达式是___________ 。
(2)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为___________ 。
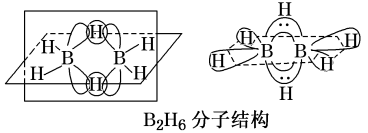
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是___________ ,写出一种与氨硼烷互为等电子体的分子:___________ (填化学式)。
(3)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。 的键角是
的键角是___________ ,立体构型为___________ 。
(1)基态硼原子的价电子轨道表达式是
(2)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为

②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是
(3)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。
 的键角是
的键角是
您最近一年使用:0次

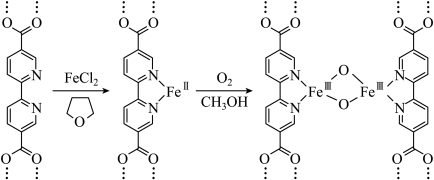
 与CH3OH的式量相差较大,但二者的沸点却极为接近,原因有:i.CH3OH的极性强于
与CH3OH的式量相差较大,但二者的沸点却极为接近,原因有:i.CH3OH的极性强于 ;ii.
;ii.

