回答下列问题。
(1)Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ 、___________ (填标号)。
A. B.
B.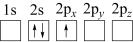
C. D.
D.
(3)基态Fe原子价层电子的电子排布图(轨道表达式)为___________ ,基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(1)Fe成为阳离子时首先失去
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(3)基态Fe原子价层电子的电子排布图(轨道表达式)为
2023高三·全国·专题练习 查看更多[2]
更新时间:2023-08-21 20:01:50
|
相似题推荐
【推荐1】洪特规则
(1)内容:基态原子中,填入_______ 的电子总是先单独分占,且自旋平行。
(2)特例:在简并轨道上的电子排布处于全充满、半充满和全空状态时,具有_______ 的能量和_______ 的稳定性。

如:24Cr的电子排布式为_______ ,为半充满状态,易错写为1s22s22p63s23p63d44s2。
(1)内容:基态原子中,填入
(2)特例:在简并轨道上的电子排布处于全充满、半充满和全空状态时,具有

如:24Cr的电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】今年是诺贝尔奖颁发120周年,其中很多获得诺贝尔化学奖的研究成果都极大的影响着我们的生活。请回答与诺贝尔化学奖获奖成果相关的下列问题:
(1)1995年,诺贝尔化学奖授予Paul Crutzen、Mario Molina 和F.S Rowland 三位科学家,以表彰他们在平流层臭氧化学研究领域所做出的贡献。氟利昂(CCl2F2等)及氮的氧化物在O3分解中起重要作用,N、O、F的第一电离能由大到小的顺序为___________ 。
(2)2019年,诺贝尔化学奖授予John B Goodenough,M.stanley Whittlingham 和 Akira Yoshino,以表彰他们在锂离子电池的发展方面作出的卓越贡献。
①从原子结构理论角度解释,Fe3+比Fe2+稳定的原因为___________ 。
②早在1973年,Whittingham 发现一种极强富能材料TiS2,以此作为锂电池的全新阴极。Ti的基态原子核外电子排布式为___________ 。下列硫的各种微粒中,电离最外层一个电子所需能量最大的是___________ 。(填字母)。
A.[Ne]3s23p3 B.[Ne]3s23p4 C.[Ne]3s23p33d1 D.[Ne]3s23p5
(1)1995年,诺贝尔化学奖授予Paul Crutzen、Mario Molina 和F.S Rowland 三位科学家,以表彰他们在平流层臭氧化学研究领域所做出的贡献。氟利昂(CCl2F2等)及氮的氧化物在O3分解中起重要作用,N、O、F的第一电离能由大到小的顺序为
(2)2019年,诺贝尔化学奖授予John B Goodenough,M.stanley Whittlingham 和 Akira Yoshino,以表彰他们在锂离子电池的发展方面作出的卓越贡献。
①从原子结构理论角度解释,Fe3+比Fe2+稳定的原因为
②早在1973年,Whittingham 发现一种极强富能材料TiS2,以此作为锂电池的全新阴极。Ti的基态原子核外电子排布式为
A.[Ne]3s23p3 B.[Ne]3s23p4 C.[Ne]3s23p33d1 D.[Ne]3s23p5
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题。
(1)A是在地壳中含量最多的元素,该元素原子的电子排布图是_______ ,其原子核外有_______ 个未成对电子,能量最高的电子所在的轨道呈_______ 形。B为周期表中第29号元素,B的电子排布式为_______ 。
(2)汽车尾气含有CO和NO等有毒气体,净化有毒气体的反应方程式为: ,此反应中涉及元素的第一电离能大小关系为
,此反应中涉及元素的第一电离能大小关系为_______ ;此反应中涉及物质中互为等电子体的是_______ ; 的结构式为
的结构式为_______ 。
(3)元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为:_______ 。
(1)A是在地壳中含量最多的元素,该元素原子的电子排布图是
(2)汽车尾气含有CO和NO等有毒气体,净化有毒气体的反应方程式为:
 ,此反应中涉及元素的第一电离能大小关系为
,此反应中涉及元素的第一电离能大小关系为 的结构式为
的结构式为(3)元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】推导下列元素,回答有关问题:
(1)具有1个4p电子的元素为________ (写元素名称)。基态Fe原子有____ 个未成对电子。Fe3+的电子排布式为_____________ 。
(2)3d能级全充满,4s能级只有1个电子的元素为_______ ,原子序数为________ 。在基态14C原子中,核外存在____ 对自旋相反的电子。基态Si原子中,电子占据的最高能层符号为_____ ,该能层具有的原子轨道数为____ 、电子数为____ 。
(3)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是________ ,M能层有______ 个电子
(1)具有1个4p电子的元素为
(2)3d能级全充满,4s能级只有1个电子的元素为
(3)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C三种分子所含原子的数目依次为1、3、6,且分子中均含有18个电子,B、C是由两种元素组成的,且分子中两种元素原子的个数比均为1:2。请回答下列问题。
(1)A的分子式是__________ ,写出A原子的价电子排布式:__________
(2)B分子的中心原子的杂化类型是__________ ,分子的空间构型是__________ ,该分子属于__________ (填“极性”或“非极性”)分子。
(3)C的化学式是__________ ,分子中含有的化学键类型是____________________ 。
(1)A的分子式是
(2)B分子的中心原子的杂化类型是
(3)C的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)C、H、O三种元素的电负性由小到大的顺序为_______ 。
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_______ 。
(3)A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。四种元素中电负性最大的是_______ (填元素符号),其中C原子的核外电子排布式为_______ 。
(1)C、H、O三种元素的电负性由小到大的顺序为
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是
(3)A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。四种元素中电负性最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)基态Ti原子的核外电子排布式为______ 。
(2)Fe成为阳离子时首先失去______ 轨道电子,Sm的价层电子排布式为价层电子排布式为______ 。
(3) 基态核外电子排布式为
基态核外电子排布式为______ 。
(4)氮原子价S电子的轨道表示式(电子排布图)为______ 。
(5)Co基态原子核外电子排布式为______ 。元素Mn与O中,基态原子核外未成对电子数较多的是______ 。
(2)Fe成为阳离子时首先失去
(3)
 基态核外电子排布式为
基态核外电子排布式为(4)氮原子价S电子的轨道表示式(电子排布图)为
(5)Co基态原子核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1)自然界中存在的碘的稳定性核素是碘-127(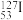 )。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(
)。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(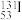 )。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
)。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
(2)核电站为防止发生核辐射事故,通常用含有铅的水泥做成屏蔽罩,内衬钢板,反应的压力容器用铁、铜、锰等具有反辐射合金材料制成。
①水泥中通常含有碳、氧、硅、铝等元素,则四种元素中3p能级上存在电子的是___________ (填元素符号)。
②写出二价铜离子的基态电子排布式:___________ 。
③铅的核电荷数为82,在周期表中___________ (填能级符号)区。
④基态锰原子价电子轨道表示式为___________ ,锰原子中能量最低的电子为___________ 轨道上的电子,其轨道呈___________ 形。
(1)自然界中存在的碘的稳定性核素是碘-127(
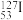 )。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(
)。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(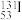 )。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
)。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。A.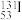 和 和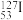 的价电子排布不相同 的价电子排布不相同 |
B.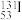 和 和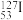 的电负性不相等 的电负性不相等 |
C.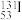 的基态电子排布式中只有1个能级未充满电子 的基态电子排布式中只有1个能级未充满电子 |
| D.碘元素的第一电离能大于氯元素 |
①水泥中通常含有碳、氧、硅、铝等元素,则四种元素中3p能级上存在电子的是
②写出二价铜离子的基态电子排布式:
③铅的核电荷数为82,在周期表中
④基态锰原子价电子轨道表示式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用。回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:___________ ,其价电子轨道表示式为___________ 。
②比较键角大小:气态SeO3分子___________ Se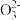 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是___________ 。
(2)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为N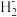 ,反应过程如图所示:
,反应过程如图所示:___________ 。
②与N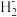 互为等电子体的一种分子为
互为等电子体的一种分子为___________ (填化学式)。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

②比较键角大小:气态SeO3分子
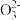 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为N
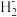 ,反应过程如图所示:
,反应过程如图所示: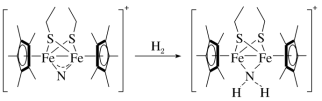
②与N
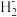 互为等电子体的一种分子为
互为等电子体的一种分子为
您最近一年使用:0次



