氮及其化合物在生产生活中具有广泛应用。氮气经过一系列的变化可以合成氨、氮的氧化物、硝酸等重要的化工原料;NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,减少环境污染。对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)∆H<0,下列有关说法不正确的是
4NO(g)+6H2O(g)∆H<0,下列有关说法不正确的是
 4NO(g)+6H2O(g)∆H<0,下列有关说法不正确的是
4NO(g)+6H2O(g)∆H<0,下列有关说法不正确的是| A.升高温度,该反应的平衡常数增大 |
| B.催化剂降低了正、逆反应的活化能 |
| C.1molN-H断裂同时有1molO-H断裂,说明达该条件下的平衡状态 |
| D.其它条件不变,加入高效的催化剂能提高单位体积内的活化分子百分数 |
更新时间:2023-04-25 21:01:14
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】 的资源化利用有利于缓解温室效应并解决能源转化问题,一种以
的资源化利用有利于缓解温室效应并解决能源转化问题,一种以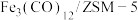 催化
催化 加氢
加氢 合成低碳烯烃的反应过程如下图所示:
合成低碳烯烃的反应过程如下图所示:

下列说法正确的是。
 的资源化利用有利于缓解温室效应并解决能源转化问题,一种以
的资源化利用有利于缓解温室效应并解决能源转化问题,一种以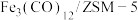 催化
催化 加氢
加氢 合成低碳烯烃的反应过程如下图所示:
合成低碳烯烃的反应过程如下图所示:
下列说法正确的是。
| A.决定整个反应快慢的是第ⅱ步 |
| B.第ⅱ步反应过程中形成了非极性键 |
C.该反应总过程即 加氢合成低碳烯烃的原子利用率为100% 加氢合成低碳烯烃的原子利用率为100% |
D.催化剂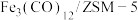 的使用可以提高低碳烯烃的产率 的使用可以提高低碳烯烃的产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】乙烯在加聚反应时,不同温度下可得到支链型聚乙烯或直链型聚乙烯,反应历程与能量变化如图所示( 表示烃基自由基)。下列说法
表示烃基自由基)。下列说法不正确 的是

 表示烃基自由基)。下列说法
表示烃基自由基)。下列说法
| A.取代基越多的烃基自由基越稳定 |
| B.合成等质量的聚乙烯,支链型放出的热量多于直链型 |
| C.支链型聚乙烯的密度小于直链型聚乙烯 |
D.支链型自由基( )的浓度先增大后减小 )的浓度先增大后减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知反应S2O (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若往该溶液中加入含Fe3+的某溶液,反应机理:
(aq)+I2(aq),若往该溶液中加入含Fe3+的某溶液,反应机理:
步骤①:2Fe3+(aq)+2I-(aq) I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)
步骤②:2Fe2+(aq)+S2O (aq)
(aq) 2Fe3+(aq)+2SO
2Fe3+(aq)+2SO (aq)
(aq)
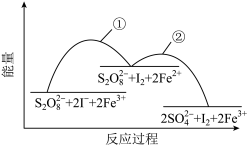
下列有关该反应的说法不正确的是
 (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若往该溶液中加入含Fe3+的某溶液,反应机理:
(aq)+I2(aq),若往该溶液中加入含Fe3+的某溶液,反应机理:步骤①:2Fe3+(aq)+2I-(aq)
 I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)步骤②:2Fe2+(aq)+S2O
 (aq)
(aq) 2Fe3+(aq)+2SO
2Fe3+(aq)+2SO (aq)
(aq)下列有关该反应的说法不正确的是

A.增大S2O 浓度或I-浓度,可增加单位体积内活化分子数,加快化学反应反应速率 浓度或I-浓度,可增加单位体积内活化分子数,加快化学反应反应速率 |
| B.Fe3+是该反应的催化剂,可以增加单位体积内活化分子的百分数 |
| C.据图可知,该反应正反应的活化能比逆反应的活化能小 |
| D.据图可知,反应①的速率大于反应② |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,利用测压法在刚性反应器中研究固体催化剂作用下的A的分解反应: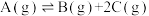 。体系的总压强p随时间t的变化如表所示:
。体系的总压强p随时间t的变化如表所示:
下列说法正确的是
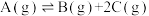 。体系的总压强p随时间t的变化如表所示:
。体系的总压强p随时间t的变化如表所示:| t/'min | 0 | 100 | 150 | 250 | 420 | 540 | 580 | 900 |
| p/kPa | 12.1 | 13.3 | 13.9 | 15.l | 17.14 | 18.58 | 19.06 | a |
A.100~250min,消耗A的平均速率为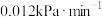 |
| B.推测a一定为22.9 |
| C.适当升高体系温度,改用表面积更大的催化剂可加快反应速率 |
| D.其他条件不变,改用容积更小的刚性反应器,反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验设计及现象能达到实验目的的是
| 选项 | 实验目的 | 实验设计及现象 |
| A | 证明 气体中存在平衡 气体中存在平衡 | 压缩盛有 气体的注射器至原来体积的一半,红棕色变浅 气体的注射器至原来体积的一半,红棕色变浅 |
| B | 比较室温下 、 、 溶度积的大小 溶度积的大小 | 向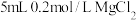 溶液中滴加少量NaOH溶液,充分振荡后,再滴加几滴 溶液中滴加少量NaOH溶液,充分振荡后,再滴加几滴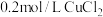 溶液,白色沉淀逐渐转化为蓝色 溶液,白色沉淀逐渐转化为蓝色 |
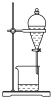
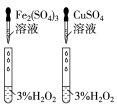
| C | 比较 和 和 的氧化性强弱 的氧化性强弱 | 常温下,向 溶液中加入 溶液中加入 溶液,将带火星的木条放在试管口,木条复燃 溶液,将带火星的木条放在试管口,木条复燃 |
| D | 证明反应生成乙烯 | 乙醇和浓硫酸共热至170℃,将产生的气体通入酸性高锰酸钾溶液中,溶液紫色褪去 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】可逆反应:2NO(g)+O2(g)2NO2(g),在压强不变的密闭容器中反应,一定达到平衡状态的标志是
| A.单位时间内生成nmolO2的同时生成nmolNO2 |
| B.2ν正(NO)=ν逆(O2) |
| C.ν(NO2):ν(NO):ν(O2)=2:2:1的状态 |
| D.混合气体的密度不再改变的状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反应为 ,以铁触媒(主要成分是
,以铁触媒(主要成分是 和
和 )为催化剂。实验室用加热
)为催化剂。实验室用加热 和
和 固体混合物的方法,或将浓氨水与
固体混合物的方法,或将浓氨水与 固体混合来制取少量氨气。工业上可利用氨气等制取硝酸。有关工业合成氨的反应下列有关说法正确的是
固体混合来制取少量氨气。工业上可利用氨气等制取硝酸。有关工业合成氨的反应下列有关说法正确的是
 ,以铁触媒(主要成分是
,以铁触媒(主要成分是 和
和 )为催化剂。实验室用加热
)为催化剂。实验室用加热 和
和 固体混合物的方法,或将浓氨水与
固体混合物的方法,或将浓氨水与 固体混合来制取少量氨气。工业上可利用氨气等制取硝酸。有关工业合成氨的反应下列有关说法正确的是
固体混合来制取少量氨气。工业上可利用氨气等制取硝酸。有关工业合成氨的反应下列有关说法正确的是| A.其它条件不变,升高温度,可提高活化分子百分数,加快反应速率 |
B.反应的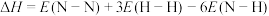 (E表示键能) (E表示键能) |
C.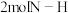 断裂同时有 断裂同时有 形成,说明达该条件下的平衡状态 形成,说明达该条件下的平衡状态 |
| D.将氨气液化并移走,可提高原料的平衡转化率及平衡时的反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
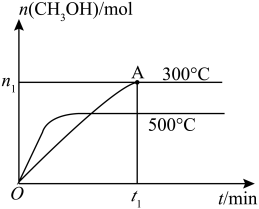
【推荐1】在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是
CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是
 CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是
CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是
| A.该反应的△H>0 |
| B.其他条件不变,升高温度反应的平衡常数增大 |
C.300℃时,0-t1min内CH3OH的平均生成速率为 mol•L-1min-1 mol•L-1min-1 |
D.A点的反应体系从300℃升高到500℃,达到平衡时 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】优化焦炭水蒸气重整工艺可制得CO含量较低的氢燃料。0.1MPa下,按n(H2O):n(C)=4向容器中加入一定量的焦炭和水蒸气。体系中发生如下反应:
反应I:C(s)+H2O(g)=CO(g)+H2(g) ΔH=131.3kJ·mol-1
反应II:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
反应III:2CO(g)+2H2(g)=CH4(g)+CO2(g) ΔH=-205.8kJ·mol-1
达到平衡时,H2的产率和CO、CO2、CH4干态气体的物质的量体积分数(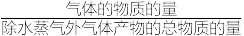 )随温度变化如图所示。下列说法正确的是
)随温度变化如图所示。下列说法正确的是

反应I:C(s)+H2O(g)=CO(g)+H2(g) ΔH=131.3kJ·mol-1
反应II:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
反应III:2CO(g)+2H2(g)=CH4(g)+CO2(g) ΔH=-205.8kJ·mol-1
达到平衡时,H2的产率和CO、CO2、CH4干态气体的物质的量体积分数(
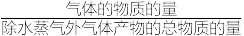 )随温度变化如图所示。下列说法正确的是
)随温度变化如图所示。下列说法正确的是
| A.曲线B表示CO2干态体积分数随温度变化 |
| B.制备CO含量低的氢燃料应选择200~600℃ |
| C.800~1400℃,随温度升高H2的产率降低,是因为反应III正向进行程度增大 |
| D.1200℃,向平衡体系中通入水蒸气,再次达到平衡时c(CO)·c(H2)的值比原平衡的大 |
您最近一年使用:0次

 晶体
晶体 ,发生反应:
,发生反应:
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法正确的是
的物质的量随时间的变化关系如图所示。下列说法正确的是 


 减小
减小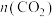 减小
减小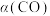 增大
增大

