向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式_______ (如果系数是1,不用填写):

(2)整个过程中的还原剂是_______ 。
(3)把KI换成KBr,则CCl4层变为_______ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)500kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2_______ L(标准状况,保留2位小数)。
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式

(2)整个过程中的还原剂是
(3)把KI换成KBr,则CCl4层变为
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)500kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2
更新时间:2023-04-26 19:56:02
|
相似题推荐
【推荐1】NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)在催化剂作用下,NH3可与NO2发生如下反应:8NH3+6NO2 7N2+12H2O
7N2+12H2O
①该反应的氧化剂是____ 。
②用单线桥表示该反应中电子转移的方向和数目:____ 。
③为研究哪些物质能将NOx转化为N2以消除污染,根据氧化还原反应的知识可知,下列物质中不适宜选用的是_______ (填序号)。
A.CO B.H2 C.CO2
(2)水体中含有较多的硝酸盐会污染水质。一种用铁粉处理水体中的硝酸盐的反应如下:Fe+ +H+-Fe2++
+H+-Fe2++ +H2O(未配平)
+H2O(未配平)
①配平后的反应中H+前的化学计量数为_________ 。
②由反应可知酸性条件下粒子的氧化性大小:____ >____ 。
(1)在催化剂作用下,NH3可与NO2发生如下反应:8NH3+6NO2
 7N2+12H2O
7N2+12H2O①该反应的氧化剂是
②用单线桥表示该反应中电子转移的方向和数目:
③为研究哪些物质能将NOx转化为N2以消除污染,根据氧化还原反应的知识可知,下列物质中不适宜选用的是
A.CO B.H2 C.CO2
(2)水体中含有较多的硝酸盐会污染水质。一种用铁粉处理水体中的硝酸盐的反应如下:Fe+
 +H+-Fe2++
+H+-Fe2++ +H2O(未配平)
+H2O(未配平)①配平后的反应中H+前的化学计量数为
②由反应可知酸性条件下粒子的氧化性大小:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求写出化学方程式:
(1)浓硫酸与木炭粉在加热条件下发生反应:___ 。
(2)铁粉与足量浓硫酸在加热条件下发生反应:___ 。
(3)一种治疗胃酸过多的药物的主要成分是碳酸氢钠:___ 。
(4)二氧化硫使浅绿色氯水褪色:___ 。
(5) K2Cr2O7+ HCl═ KCl+ CrCl3+ Cl2↑+ H2O,以上反应中失电子的物质是___ 。还原产物是___ ,K2Cr2O7的氧化性___ Cl2的氧化性(填“>”或“<”),氧化剂与还原剂的物质的量之比为___ 。
(1)浓硫酸与木炭粉在加热条件下发生反应:
(2)铁粉与足量浓硫酸在加热条件下发生反应:
(3)一种治疗胃酸过多的药物的主要成分是碳酸氢钠:
(4)二氧化硫使浅绿色氯水褪色:
(5) K2Cr2O7+ HCl═ KCl+ CrCl3+ Cl2↑+ H2O,以上反应中失电子的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)在 、
、 、
、 、
、 、
、 、
、 、
、 中,只有氧化性的是
中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有一种制备高铁酸钠的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有一种制备高铁酸钠的化学反应原理可用离子方程式表示为:

①由上述反应可知,氧化性强弱:
___________  (填“>”或“<”);
(填“>”或“<”);
②请用单线桥法表示该反应中电子的转移情况:___________ 。
(3) 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
①该反应中,氧化剂是___________ , 氧化剂在反应过程中转移电子数是
氧化剂在反应过程中转移电子数是___________ ;
②将以上物质填入下面横线上,并配平该反应。
___________ 。
(1)在
 、
、 、
、 、
、 、
、 、
、 、
、 中,只有氧化性的是
中,只有氧化性的是(2)高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有一种制备高铁酸钠的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有一种制备高铁酸钠的化学反应原理可用离子方程式表示为:
①由上述反应可知,氧化性强弱:

 (填“>”或“<”);
(填“>”或“<”);②请用单线桥法表示该反应中电子的转移情况:
(3)
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。①该反应中,氧化剂是
 氧化剂在反应过程中转移电子数是
氧化剂在反应过程中转移电子数是②将以上物质填入下面横线上,并配平该反应。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据题目要求回答下列问题。
(1)23.4g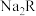 含
含 0.6mol,R的相对原子质量为
0.6mol,R的相对原子质量为______ 。含Na的质量为6.9g的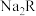 ,其物质的量为
,其物质的量为_____ 。
(2)按照物质的分类,次磷酸( )属于一元酸,其与足量的NaOH溶液反应的化学方程式为
)属于一元酸,其与足量的NaOH溶液反应的化学方程式为_____ 。
(3) 的氧化性比
的氧化性比 强得多,实验室也可以用
强得多,实验室也可以用 固体和浓盐酸反应制取氯气,反应的化学方程式为
固体和浓盐酸反应制取氯气,反应的化学方程式为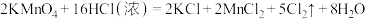 。
。
①氧化剂和还原剂的物质的量之比为_______ ;
②当有0.4mol电子发生转移时,被氧化的HCl的质量是_______ 。
(1)23.4g
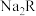 含
含 0.6mol,R的相对原子质量为
0.6mol,R的相对原子质量为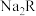 ,其物质的量为
,其物质的量为(2)按照物质的分类,次磷酸(
 )属于一元酸,其与足量的NaOH溶液反应的化学方程式为
)属于一元酸,其与足量的NaOH溶液反应的化学方程式为(3)
 的氧化性比
的氧化性比 强得多,实验室也可以用
强得多,实验室也可以用 固体和浓盐酸反应制取氯气,反应的化学方程式为
固体和浓盐酸反应制取氯气,反应的化学方程式为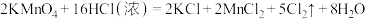 。
。①氧化剂和还原剂的物质的量之比为
②当有0.4mol电子发生转移时,被氧化的HCl的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高铁酸钾( )是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,是一种新型、高效、多功能水处理剂。
)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,是一种新型、高效、多功能水处理剂。
I.工业上干法制高铁酸钾有两种方法:
方法一:反应原理为: ,将制得的高铁酸钠进一步转化成高铁酸钾。
,将制得的高铁酸钠进一步转化成高铁酸钾。
(1)根据上述方程式判断还原剂为___ ,每生成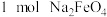 转移的电子数为
转移的电子数为______ 。
方法二: 、
、 、
、 混合加热共熔生成高铁酸盐和
混合加热共熔生成高铁酸盐和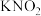 等产物。
等产物。
(2)该反应氧化剂与还原剂的物质的量之比为______ 。
II.某学习小组设计如图方案制备高铁酸钾:

(3)其中第一步操作是:在 溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1小时,则采用的合适控温方式是
溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1小时,则采用的合适控温方式是___________ 。反应的离子方程式为___________ 。
(4)高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生一种气体,写出反应的离子方程式为___________ 。
(5)在低温下,向 溶液中加入饱和
溶液中加入饱和 溶液能析出
溶液能析出 ,其原因是
,其原因是_____ 。
 )是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,是一种新型、高效、多功能水处理剂。
)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,是一种新型、高效、多功能水处理剂。I.工业上干法制高铁酸钾有两种方法:
方法一:反应原理为:
 ,将制得的高铁酸钠进一步转化成高铁酸钾。
,将制得的高铁酸钠进一步转化成高铁酸钾。(1)根据上述方程式判断还原剂为
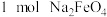 转移的电子数为
转移的电子数为方法二:
 、
、 、
、 混合加热共熔生成高铁酸盐和
混合加热共熔生成高铁酸盐和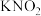 等产物。
等产物。(2)该反应氧化剂与还原剂的物质的量之比为
II.某学习小组设计如图方案制备高铁酸钾:

(3)其中第一步操作是:在
 溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1小时,则采用的合适控温方式是
溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1小时,则采用的合适控温方式是(4)高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生一种气体,写出反应的离子方程式为
(5)在低温下,向
 溶液中加入饱和
溶液中加入饱和 溶液能析出
溶液能析出 ,其原因是
,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】亚硝酸钠是一种具有咸味、有毒的工业用盐,工业上常用作防腐剂。
(1)NaNO2中N的化合价为_______ ,由N的化合价推测NaNO2具有_______ (填“氧化性”、“还原性”或“氧化性、还原性”)。
(2)NaNO2易溶于水,水溶液显碱性。写出HNO2的电离方程式_______ 。
(3)酸性条件下, 能与
能与 反应得到
反应得到 ,写出此反应的离子方程式
,写出此反应的离子方程式_______ 。
(4)NaNO2与HI反应:2NaNO2+4HI =2NO↑+I2+2NaI+2H2O,若有0.5 mol氧化剂被还原,则被氧化的还原剂的物质的量是_______ mol。
(5)工业废水中含有亚硝酸盐,以氯化铵处理亚硝酸盐的新工艺已在工业上广泛使用。该反应的生成物不会给环境带来任何污染,写出反应的离子方程式_______ ,理论上53.5 kg NH4Cl可除去废水中的
_______ mol。
(1)NaNO2中N的化合价为
(2)NaNO2易溶于水,水溶液显碱性。写出HNO2的电离方程式
(3)酸性条件下,
 能与
能与 反应得到
反应得到 ,写出此反应的离子方程式
,写出此反应的离子方程式(4)NaNO2与HI反应:2NaNO2+4HI =2NO↑+I2+2NaI+2H2O,若有0.5 mol氧化剂被还原,则被氧化的还原剂的物质的量是
(5)工业废水中含有亚硝酸盐,以氯化铵处理亚硝酸盐的新工艺已在工业上广泛使用。该反应的生成物不会给环境带来任何污染,写出反应的离子方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】烟道气中的NOx是主要的大气污染物之一,为了监测某工厂烟道气中NOx含量,采集标准状况下50.00mL烟道气经除尘、干燥后缓慢通入适量酸化的H2O2的溶液中,使NOx完全被氧化为NO ,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO
,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO 的还原产物全为NO,且NO全部从溶液中逸出)
的还原产物全为NO,且NO全部从溶液中逸出)
(1)写出NO被H2O2氧化为NO 的离子方程式
的离子方程式_______
(2)与量取的20.00mL溶液中NO 反应的Fe2+为
反应的Fe2+为_______ mol?若FeSO4标准溶液部分变质,会使NOx含量测定结果如何_______ (答偏高、偏低或者无影响)
(3)标准状况下该工程烟道气中NOx(折合为NO2)的含量为每立方米_______ 毫克?
 ,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO
,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO 的还原产物全为NO,且NO全部从溶液中逸出)
的还原产物全为NO,且NO全部从溶液中逸出)(1)写出NO被H2O2氧化为NO
 的离子方程式
的离子方程式(2)与量取的20.00mL溶液中NO
 反应的Fe2+为
反应的Fe2+为(3)标准状况下该工程烟道气中NOx(折合为NO2)的含量为每立方米
您最近一年使用:0次
填空题
|
适中
(0.64)
名校
【推荐2】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。回答下列有关双氧水的一些问题:
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同)______________
(2)保存过氧化氢试剂瓶上的最适合贴上的一个标签是___________ (填字母代号)。
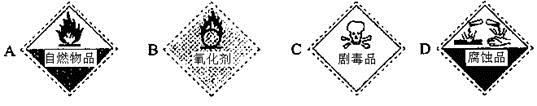
(3)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
①写出该反应的离子方程式并配平_______________________________ 。
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子数目为_________________ 。
(4)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为_____________ ,并阐明H2O2被称为绿色氧化剂的理由是_____________ 。
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同)
| A.Na2O2+2HCl=2NaCl+H2O2 |
| B.Ag2O+H2O2=2Ag+O2↑+H2O |
| C.2H2O2=2H2O+O2↑ |
| D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O |
(2)保存过氧化氢试剂瓶上的最适合贴上的一个标签是
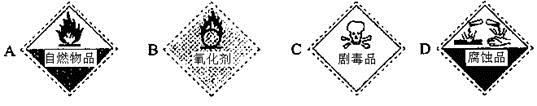
(3)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
①写出该反应的离子方程式并配平
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子数目为
(4)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为
您最近一年使用:0次



