元素周期表是元素周期律的具体表现,是学习和研究化学的一种重要工具。下图是元素周期表的一部分:
回答下列问题:
(1)As元素在周期表中的位置是:___________ 。
(2)元素①气态氢化物分子的空间构型是___________ 。请用一个方程式比较元素①和元素②的非金属性强弱:___________ 。
(3)元素③、④、⑤的简单离子半径由大到小排序为:___________ (用离子符号表示)。
(4)元素⑤、⑥非金属性更强的是:___________ (用元素符号表示),请从原子结构的角度解释:___________ 。
电离能是指由气态原子失去电子形成阳离子需要的能量。从中性原子中失去第一个电子所需要的能量为第一电离能( ),失去第二个电子所需要的能量为第二电离能(
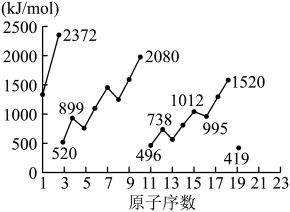
),失去第二个电子所需要的能量为第二电离能( ),依次类推。下图为1-19号元素第一电离能
),依次类推。下图为1-19号元素第一电离能 。
。
回答下列问题:
(5)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常,预测下列关系式中正确的是___________(填编号)。
(6)10号元素Ne的 值较大的原因是
值较大的原因是___________ 。
| ① | ② | ③ | ||
| ④ | P | ⑤ | ⑥ | |
| Ga | Ge | As | Se | Br |
回答下列问题:
(1)As元素在周期表中的位置是:
(2)元素①气态氢化物分子的空间构型是
(3)元素③、④、⑤的简单离子半径由大到小排序为:
(4)元素⑤、⑥非金属性更强的是:
电离能是指由气态原子失去电子形成阳离子需要的能量。从中性原子中失去第一个电子所需要的能量为第一电离能(
 ),失去第二个电子所需要的能量为第二电离能(
),失去第二个电子所需要的能量为第二电离能( ),依次类推。下图为1-19号元素第一电离能
),依次类推。下图为1-19号元素第一电离能 。
。
回答下列问题:
(5)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常,预测下列关系式中正确的是___________(填编号)。
A.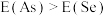 | B. | C. | D.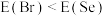 |
 值较大的原因是
值较大的原因是
22-23高一下·上海浦东新·期中 查看更多[1]
(已下线)上海市华东师范大学第二附属中学2022-2023学年高一下学期期中考试化学试题
更新时间:2023-05-17 09:49:38
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】下表为元素周期表的一部分。
(1)表中元素________ 的非金属性最强;元素________ 的金属性最强;元素________ 的单质在室温下呈液态;(写元素符号)。
(2)表中半径最大的元素是_______ ;(写元素符号)
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是_______ ;(写化学式,下同)
(4)表中元素⑥、⑦氢化物的稳定性顺序为________ >________ ;
(5)表中元素最高价氧化物对应水化物酸性最强的酸是_________________ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ⑤ | |||||
| 三 | ③ | ⑥ | |||||
| 四 | ④ | ⑦ | |||||
(1)表中元素
(2)表中半径最大的元素是
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是
(4)表中元素⑥、⑦氢化物的稳定性顺序为
(5)表中元素最高价氧化物对应水化物酸性最强的酸是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】某学习小组探究B及其化合物的性质。
(1)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。
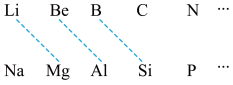
B在元素周期表中的位置是_______ 。其最高价氧化物的化学式为_______ ,与氢氧化钠溶液反应的化学方程式为_______ 。
(2)某科研团队研究发现硼氢化钠( )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
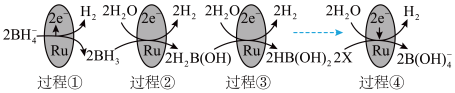
①上图中X的化学式为_______ 。
② 以二聚物的形式存在,分子结构中存在两个
以二聚物的形式存在,分子结构中存在两个 键共用一对共用电子的氢桥键,用
键共用一对共用电子的氢桥键,用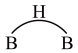 表示,则二聚物结构式为
表示,则二聚物结构式为_______ 。
③图中反应的总化学方程式为_______ 。
④_______ g 的还原能力与标准状况下22.4L
的还原能力与标准状况下22.4L 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
(1)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。

B在元素周期表中的位置是
(2)某科研团队研究发现硼氢化钠(
 )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
①上图中X的化学式为
②
 以二聚物的形式存在,分子结构中存在两个
以二聚物的形式存在,分子结构中存在两个 键共用一对共用电子的氢桥键,用
键共用一对共用电子的氢桥键,用 表示,则二聚物结构式为
表示,则二聚物结构式为③图中反应的总化学方程式为
④
 的还原能力与标准状况下22.4L
的还原能力与标准状况下22.4L 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
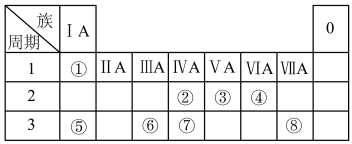
(1)⑦号元素的原子结构示意图为___________________________ 。
(2)②、③、⑤的单质熔点由大到小的顺序为(填化学式)________ 。
(3)①和②、①和③、①和⑦形成的化合物稳定性由强到弱的顺序是(填化学式)__________________________________________________ 。
(4)④、⑤可形成既含离子键又含共价键的化合物,请写出其电子式:________ 。
(5)由①和②组成的最简单的化合物的键角是________ 。
(6)⑤、⑥两种元素形成的最高价氧化物的水化物之间相互反应的离子方程式为__________________________________________________ 。

(1)⑦号元素的原子结构示意图为
(2)②、③、⑤的单质熔点由大到小的顺序为(填化学式)
(3)①和②、①和③、①和⑦形成的化合物稳定性由强到弱的顺序是(填化学式)
(4)④、⑤可形成既含离子键又含共价键的化合物,请写出其电子式:
(5)由①和②组成的最简单的化合物的键角是
(6)⑤、⑥两种元素形成的最高价氧化物的水化物之间相互反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】硫是一种典型的非金属元素,请回答下列问题:
(1)硫元素的非金属性___________ 氯元素(填“大于”或“小于”),请用一个事实来说明_______________________ 。
(2)氧硫化碳(COS)可作储粮杀虫剂,已知COS与CO2的结构相似,试写出COS的电子式______ ,COS属于_______ 分子(填“极性”或“非极性”)。COS的沸点___________ CO2的沸点(填“大于”或“小于”),并说出理由_______________________ 。
(3)冷的浓硫酸可以用铁制容器储存,是因为铁在冷的浓硫酸中发生了_______________ 现象。但是在加热条件下,浓硫酸还是可以和铁反应的。
①写出铁在加热条件下和足量浓硫酸反应的化学方程式,并标出电子转移方向与数目_____________________ 。
②上述反应中________ 元素被还原,还原产物是_________________________ 。
(1)硫元素的非金属性
(2)氧硫化碳(COS)可作储粮杀虫剂,已知COS与CO2的结构相似,试写出COS的电子式
(3)冷的浓硫酸可以用铁制容器储存,是因为铁在冷的浓硫酸中发生了
①写出铁在加热条件下和足量浓硫酸反应的化学方程式,并标出电子转移方向与数目
②上述反应中
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】填写下列空格。
(1)已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要吸收的能量为436.4kJ、242.7kJ、431.8kJ。则由H2和Cl2反应生成1molHCl需要_____ (填“放出”或“吸收”)____ kJ的热量。
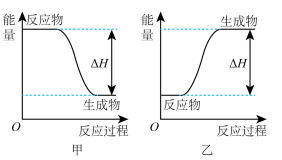
(2)H2可以在Cl2中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图_____ (填“甲”或“乙”)。
(3)已知:H2与Cl2在光照条件下会发生爆炸。同温同压下,反应H2(g)+Cl2(g)=2HCl(g)。在光照和点燃条件下的∆H_____ (填“相等”或“不相等”)。
(4)硅、磷、硫、氯元素的气态氢化物的形成条件和热稳定性如下表所示:
结合元素原子结构等知识,分析以上信息可得出的结论是:同周期非金属元素,随着元素核电荷数的递增,____________________________________ ,因此,Si、P、S、Cl非金属性依次增强。
(1)已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要吸收的能量为436.4kJ、242.7kJ、431.8kJ。则由H2和Cl2反应生成1molHCl需要
(2)H2可以在Cl2中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图

(3)已知:H2与Cl2在光照条件下会发生爆炸。同温同压下,反应H2(g)+Cl2(g)=2HCl(g)。在光照和点燃条件下的∆H
(4)硅、磷、硫、氯元素的气态氢化物的形成条件和热稳定性如下表所示:
| 元素符号 | Si | P | S | Cl |
| 单质与氢气的反应 | 高温下反应 | 磷蒸气与氢气能反应 | 加热时反应 | 光照或点燃时发生爆炸而化合 |
| 气态氢化物的热稳定性 | 不稳定 | 不稳定 | 受热分解 | 稳定 |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】现有a~i 9种短周期元素,它们在同期表中的位置如下,请据此回答下列问题:(请用具体的元素符号及化学用语作答)
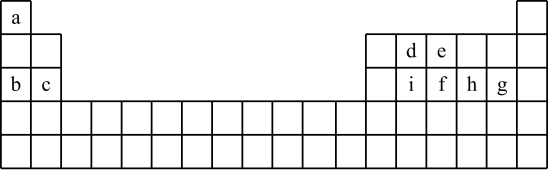
(1)a~i元素中,金属性最强的是________ ,最高价氧化物对应水化物中,酸性最强的物质是___________ 。g所在族的元素形成的氢化物中沸点最低的是____________________ 。
(2)比较b、e、g简单离子半径的大小___________________ (用离子符号作答)。
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式__________________ 、___________________ 。
(4)用一个化学反应方程式表示d的非金属性强于i_______________________________ 。
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是______ (填序号)。
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号_________ ;镓(Ga)与As同周期,最外层有3个电子,Ga与As可以形成一种新型化合物半导体材料,其性能更优越。这种新型化合物化学式为____________________ 。
(6)c与a形成的化合物的电子式为___________ ,用电子式表示a与h形成a2h的过程__________________________________________ 。
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式_________________________________ 。

(1)a~i元素中,金属性最强的是
(2)比较b、e、g简单离子半径的大小
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式
(4)用一个化学反应方程式表示d的非金属性强于i
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号
(6)c与a形成的化合物的电子式为
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)与SeO32-互为等电子体的分子有(写一种物质的化学式即可)_____ 。
(2)分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为_______ , (CN)2称为“拟卤素”,具有类似Cl2的化学性质,则(CN)2与NaOH水溶液反应的化学方程式为____________ 。
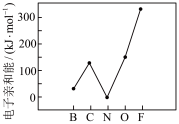
(3)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是__________ 。
(4)基态As原子中,核外电子占据最高能层的符号是_________ ,占据该能层电子的电子云轮廓图形状为___________ 。
(5))As与Se的第一电离能前者_______ 后者(填大于或小于,下同)原子半径前者_______ 后者。
(2)分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
(3)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是

(4)基态As原子中,核外电子占据最高能层的符号是
(5))As与Se的第一电离能前者
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】【化学—选修3:物质结构与性质】
2015年我国自主研制的C919大型客机正式下线,标志着我国成为世界上少数几个掌握研发制造大型客机能力的国家,同时意味着中国高端装备制造业发展到一个全新的高度。
(1)飞机的外壳通常采用镁、铝、钛合金材料,钛的价电子排布图为__________ ,第一电离能:镁 _________ 铝(填“大于”或“小于”)。
(2)Fe与CO能形成配合物羰基铁[Fe(CO)5],该分子中σ键与π键个数比为________ 。
(3)SCl2分子中的中心原子杂化轨道类型是_______ ,该分子构型为_________ 。
(4)已知MgO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69 pm。则熔点:MgO_____ NiO(填“>”、“<”或“=”),理由是_____________ 。
(5)如图1所示,NiO晶胞中离子坐标参数A为(0,0,0),B为(1,0,1),则C离子坐标参数为___________ 。
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为______ g。(用a、NA表示)

2015年我国自主研制的C919大型客机正式下线,标志着我国成为世界上少数几个掌握研发制造大型客机能力的国家,同时意味着中国高端装备制造业发展到一个全新的高度。
(1)飞机的外壳通常采用镁、铝、钛合金材料,钛的价电子排布图为
(2)Fe与CO能形成配合物羰基铁[Fe(CO)5],该分子中σ键与π键个数比为
(3)SCl2分子中的中心原子杂化轨道类型是
(4)已知MgO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69 pm。则熔点:MgO
(5)如图1所示,NiO晶胞中离子坐标参数A为(0,0,0),B为(1,0,1),则C离子坐标参数为
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】根据元素周期表回答下列问题:
(1)写出元素Cu的基态原子的电子排布式:____________________ 。
(2)某元素A的核外价电子排布式为nsnnpn+1,该元素A原子核外最外层电子中成对电子共有________ 对。此元素A原子与O的第一电离能的相对大小为:A________ O(填“<”“>”或“=”)。
(3)元素C形成的最高价氧化物中含有________ 个π键。C和Cl形成化合物的电子式为_____________ ,此化合物中C的杂化方式为________ 。
(4)已知元素钒形成单质的晶胞如下图所示,则其原子的配位数是________ ,假设晶胞的边长为d cm、密度为ρ g·cm-3,则元素钒的相对原子质量为_____________ (NA为阿伏伽德罗常数)。

(1)写出元素Cu的基态原子的电子排布式:
(2)某元素A的核外价电子排布式为nsnnpn+1,该元素A原子核外最外层电子中成对电子共有
(3)元素C形成的最高价氧化物中含有
(4)已知元素钒形成单质的晶胞如下图所示,则其原子的配位数是

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】 、
、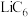 是重要的电极材料,回答下列问题:
是重要的电极材料,回答下列问题:
(1)基态Co原子的价电子排布式为_______________ 。
(2)Co(Ⅲ)可形成多种配合物,如图所示是 结构,
结构, 位于正八面体中心,若其中两个
位于正八面体中心,若其中两个 被
被 取代,则
取代,则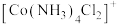 的空间结构有
的空间结构有_______________ 种。

(3) 、
、 在合成化学上应用广泛。
在合成化学上应用广泛。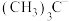 的空间结构为
的空间结构为_______________ ;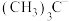 、
、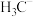 、
、 的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是
的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是_______________ 。
(4)①正极材料 的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有个O;充电时,
的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有个O;充电时, 脱出部分
脱出部分 ,形成
,形成 ,结构如图(b),则
,结构如图(b),则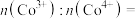
_______________ 。

②负极材料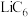 晶胞结构如图(c),Li原子插入石墨层中间,若该晶胞中碳碳键键长为a pm,石墨层间距为d pm,阿伏加德罗常数的值为
晶胞结构如图(c),Li原子插入石墨层中间,若该晶胞中碳碳键键长为a pm,石墨层间距为d pm,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______________  (列出计算式)。
(列出计算式)。

 、
、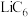 是重要的电极材料,回答下列问题:
是重要的电极材料,回答下列问题:(1)基态Co原子的价电子排布式为
(2)Co(Ⅲ)可形成多种配合物,如图所示是
 结构,
结构, 位于正八面体中心,若其中两个
位于正八面体中心,若其中两个 被
被 取代,则
取代,则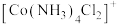 的空间结构有
的空间结构有
(3)
 、
、 在合成化学上应用广泛。
在合成化学上应用广泛。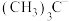 的空间结构为
的空间结构为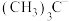 、
、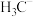 、
、 的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是
的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是(4)①正极材料
 的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有个O;充电时,
的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有个O;充电时, 脱出部分
脱出部分 ,形成
,形成 ,结构如图(b),则
,结构如图(b),则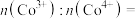

②负极材料
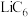 晶胞结构如图(c),Li原子插入石墨层中间,若该晶胞中碳碳键键长为a pm,石墨层间距为d pm,阿伏加德罗常数的值为
晶胞结构如图(c),Li原子插入石墨层中间,若该晶胞中碳碳键键长为a pm,石墨层间距为d pm,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】铜元素可以形成多种重要化合物。回答下列问题:
(1)铜元素位于元素周期表中的__________ 区,其基态原子的价电子轨道表示式为__________ 。
(2)向硫酸铜溶液中加入过量氨水,可形成 溶液,该溶液可用于溶解纤维素。
溶液,该溶液可用于溶解纤维素。
① 中阴离子的立体构型是
中阴离子的立体构型是__________ 。
②在 中,
中, 与
与 之间形成的化学键称为
之间形成的化学键称为__________ ,提供孤电子对的成键原子是__________ 。
③除硫元素外, 中所含元素的电负性由小到大的顺序为
中所含元素的电负性由小到大的顺序为_____ (用元素符号表示)
④ 与
与 的空间构型相同,中心原子的轨道杂化类型均为
的空间构型相同,中心原子的轨道杂化类型均为________ 。
(1)铜元素位于元素周期表中的
(2)向硫酸铜溶液中加入过量氨水,可形成
 溶液,该溶液可用于溶解纤维素。
溶液,该溶液可用于溶解纤维素。①
 中阴离子的立体构型是
中阴离子的立体构型是②在
 中,
中, 与
与 之间形成的化学键称为
之间形成的化学键称为③除硫元素外,
 中所含元素的电负性由小到大的顺序为
中所含元素的电负性由小到大的顺序为④
 与
与 的空间构型相同,中心原子的轨道杂化类型均为
的空间构型相同,中心原子的轨道杂化类型均为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】硼磷化合物
等电子体的应用非常广泛,BN或BP与一些有机物具有等电子体特征。已知B-P单键和B=P双键的键长分别为190~200pm和179~184pm,一些有机基团表示如下:Me表示甲基,Et表示乙基,Ph表示苯基,Mes表示2,4,6-三甲基苯基。
(1)BCl3与LiPEt2在50℃下的乙醚溶液中以1∶3反应,得到四元环化合物A;BrB(PMes2)2与LiPMe2等摩尔反应得到B-P键长为187pm的化合物B;Ph2BCl与PhPH2在三乙胺存在下于甲苯中以2∶1反应得到化合物C。画出A、B、C的立体结构,在结构中标出中心原子的杂化方式_____ 、_____ 、_____ 。
(2)B2Cl4与PCl3以7∶2反应得到化合物D和E,D中的中心原子为sp2杂化,D和E的物质的量之比为10∶1,画出D和E的立体结构_____ 、_____ 。
等电子体的应用非常广泛,BN或BP与一些有机物具有等电子体特征。已知B-P单键和B=P双键的键长分别为190~200pm和179~184pm,一些有机基团表示如下:Me表示甲基,Et表示乙基,Ph表示苯基,Mes表示2,4,6-三甲基苯基。
(1)BCl3与LiPEt2在50℃下的乙醚溶液中以1∶3反应,得到四元环化合物A;BrB(PMes2)2与LiPMe2等摩尔反应得到B-P键长为187pm的化合物B;Ph2BCl与PhPH2在三乙胺存在下于甲苯中以2∶1反应得到化合物C。画出A、B、C的立体结构,在结构中标出中心原子的杂化方式
(2)B2Cl4与PCl3以7∶2反应得到化合物D和E,D中的中心原子为sp2杂化,D和E的物质的量之比为10∶1,画出D和E的立体结构
您最近一年使用:0次



