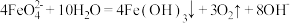下列离子方程式书写正确的是
| A.硝酸银溶液与碘化钾溶液反应: 2Ag+ +2I- =2Ag+I2 |
| B.氧化铁粉末溶于足量氢碘酸: Fe2O3+6H+ =2Fe3+ + 3H2O |
| C.用硫酸铜溶液吸收硫化氢气体: Cu2+ +H2S=CuS↓+2H+ |
D.用惰性电极电解氯化镁溶液: 2C1- +2H2O 2OH- +H2↑ +Cl2↑ 2OH- +H2↑ +Cl2↑ |
2023·贵州贵阳·二模 查看更多[2]
更新时间:2023-05-20 21:25:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式书写正确的是( )
A.少量碳酸氢钠溶液逐滴加入到氢氧化钙溶液中: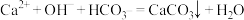 |
B.在溴化亚铁溶液中通入过量的氯气: |
C.在NaHSO4溶液中滴入Ba(OH)2溶液至中性: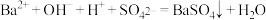 |
D.少量二氧化硫通入漂白粉溶液中: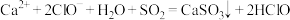 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式正确的是
| A.生活中用食醋除水垢:CaCO3+2H+=Ca2++CO2↑+H2O |
| B.用FeS沉淀工业废水中的Cu2+:FeS(s)+Cu2+(aq)=CuS(s)+Fe2+(aq) |
C.用热碱液洗涤油污:CO +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
| D.稀盐酸除铁锈:Fe(OH)3+3H+=Fe3++3H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】硝酸厂烟气中含有大量氮氧化物 。常温下,将烟气与
。常温下,将烟气与 的混合气体通入
的混合气体通入 与
与 的混合溶液中可实现无害化处理,其转化过程如图所示(以NO为例)。下列说法
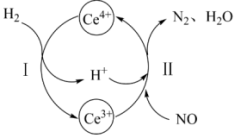
的混合溶液中可实现无害化处理,其转化过程如图所示(以NO为例)。下列说法不正确 的是
 。常温下,将烟气与
。常温下,将烟气与 的混合气体通入
的混合气体通入 与
与 的混合溶液中可实现无害化处理,其转化过程如图所示(以NO为例)。下列说法
的混合溶液中可实现无害化处理,其转化过程如图所示(以NO为例)。下列说法
A.反应I中氧化产物与还原产物的物质的量之比为 |
B.反应Ⅱ的离子方程式为 |
C.反应过程中 和 和 起催化作用 起催化作用 |
D.该转化过程的实质是NO被 氧化成 氧化成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】科研小组用氧化—沉淀法从废电池浸出液中去除铁:用MnO2氧化废电池浸出液中的Fe2+(酸性条件下,MnO2被还原为Mn2+),再加适量Na2CO3溶液调pH使Fe3+转化为Fe(OH)3沉淀。研究发现pH对Fe2+氧化率和铁去除率的影响如图1和图2所示。
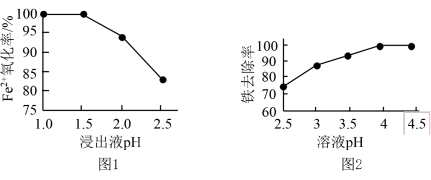
下列说法错误的是

下列说法错误的是
| A.由图1可推断MnO2的氧化性随浸出液pH增大而减弱 |
| B.若起始浸出液pH=1,MnO2与Fe2+反应一段时间后,浸出液pH会减小 |
C.Fe3+转变为沉淀的离子方程式为2Fe3++3CO +3H2O=2Fe(OH)3↓+3CO2↑ +3H2O=2Fe(OH)3↓+3CO2↑ |
| D.推测若用NaHCO3溶液调pH也可以使Fe3+转化为Fe(OH)3沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列离子方程式书写正确的是
A.向 溶液中通入少量 溶液中通入少量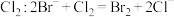 |
B.用白醋浸泡过的淀粉- 试纸检验加碘盐中的 试纸检验加碘盐中的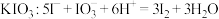 |
C.向 溶液中通入 溶液中通入 气体产生白色沉淀: 气体产生白色沉淀: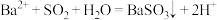 |
D. 的 的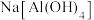 溶液和 溶液和 的 的 溶液等体积混合: 溶液等体积混合: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】现代医学证明“痛风”的病因与关节滑液中形成的尿酸钠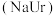 晶体有关,在寒冷季节尤其易诱发关节疼痛。主要原理为:
晶体有关,在寒冷季节尤其易诱发关节疼痛。主要原理为:
①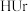 (尿酸)
(尿酸)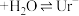 (尿酸离子)
(尿酸离子)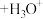
②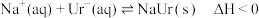
下列叙述错误 的是
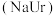 晶体有关,在寒冷季节尤其易诱发关节疼痛。主要原理为:
晶体有关,在寒冷季节尤其易诱发关节疼痛。主要原理为:①
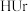 (尿酸)
(尿酸)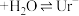 (尿酸离子)
(尿酸离子)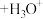
②
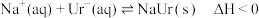
下列叙述
| A.反应①是尿酸的电离方程式 |
| B.热敷能减轻关节疼痛 |
| C.饮食中摄入过多食盐,容易诱发痛风 |
| D.“痛风”患者应多摄入代谢产生较多尿酸的食物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,将等体积的AgCl和AgI的饱和溶液的清液混合,再向其中加入一定量的AgNO3固体,下列说法不正确的是
| A.两溶液混合,AgCl和AgI都沉淀 |
| B.若AgNO3足量,AgCl和AgI都可沉淀,但以AgCl为主 |
| C.向AgI的饱和溶液中加AgNO3,c(Ag+)增大,Ksp(AgI)不变 |
| D.若取0.1435克AgCl固体配成100mL水(忽略体积变化),c(Cl-)约为1.3×10-5mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
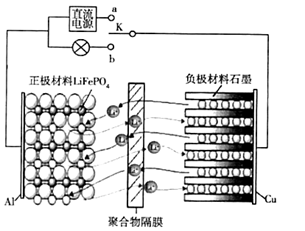
【推荐1】新型高性能电池的开发与研究已成为当下信息产业化时代的迫切要求、某研究团队设计研制了种高性能的磷酸铁锂(LiFePO4,简称LFP)电池。正极材料为磷酸铁锂,与Al相连,负极材料为石墨,与Cu相连,正、负之间存在电解质并通过聚合物隔膜隔开,此膜只允许Li+通过,其工作原理如图所示,总反应为Li(1-x)C6十LiFePO4 LiC6+ Li(1-x) FePO4。下列有关说法正确的是
LiC6+ Li(1-x) FePO4。下列有关说法正确的是
 LiC6+ Li(1-x) FePO4。下列有关说法正确的是
LiC6+ Li(1-x) FePO4。下列有关说法正确的是
| A.当开关K置于a时,Li+由右向左穿过聚合物隔膜到达正极 |
| B.当开关K置于a时,正极材料上的电极反应为: Li(1-x) FePO4 +xLi ++xe- =LiFePO4 |
| C.该电池的正、负极之间可以用Na2SO4水溶液作电解质溶液 |
| D.当开关K置于b时,负极上的电极反应为:LiC6- xe- = Li(1-x) C6+xLi+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列对应的离子方程式正确的是
| A.碳酸镁固体与稀盐酸反应:MgCO3+2H+=Mg2++CO2↑+H2O |
B.向氯化铁溶液中通入二氧化硫:2Fe3++3SO2+6H2O=2Fe2++3 +12H+ +12H+ |
C.用铜电极电解硫酸铜溶液:2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
D.向氯水中加入少量的碳酸钠:Cl2+ =Cl-+ClO-+CO2↑ =Cl-+ClO-+CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时Li+得电子成为Li嵌入该薄膜材料中;电极B为LiCoO2薄膜;集流体起导电作用。下列说法正确的是
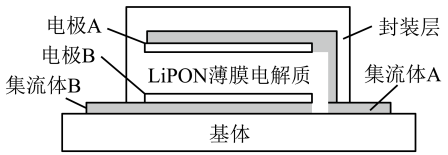

| A.充电时,集流体A与外接电源的正极相连 |
| B.放电时,外电路通过amol电子时,LiPON薄膜电解质损失amolLi+ |
| C.放电时,电极B为正极,反应可表示为Li1-xCoO2+xLi++xe-=LiCoO2 |
| D.放电时,电极A为负极,反应可表示为LixSi-e-=Si+Li+ |
您最近一年使用:0次

 溶液中:
溶液中:
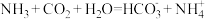
 溶液中通入过量的氯气:
溶液中通入过量的氯气: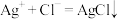
 溶液中加入过量的
溶液中加入过量的  溶液:
溶液: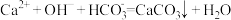
 溶液中通入少量
溶液中通入少量 :
: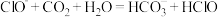
 溶液中加入少量硫酸镁溶液:
溶液中加入少量硫酸镁溶液:
 溶液中滴入少量
溶液中滴入少量 溶液:
溶液: