连二硫酸锰(MnS2O6,其中Mn为+2价)是一种常用的果蔬保鲜剂,易溶于水,室温下其水溶液在pH为2.8~3.5时最稳定。回答下列问题:
[探究一]制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。
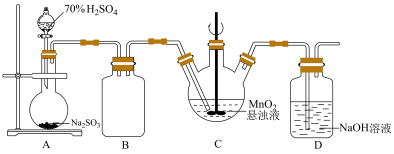
(1)装置A中装有70%H2SO4的仪器名称为_______ ,装置B的作用是_______ 。
(2)装置C中的反应温度需要控制在0°C左右,控制温度的方法是_______ ,实验时需要向C中通入稍过量的SO2,目的是_______ 。
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为_______ ,判断反应完成的现象是_______ ,待反应结束后经除杂、减压蒸发浓缩、结晶可得产品MnS2O6·nH2O。
[探究二]测定产品中Mn的质量分数
称取ag产品充分加热使其分解为MnSO4,然后加水溶解,用cmol·L-1的KMnO4溶液进行滴定(Mn元素均转化为MnO2)。
(4)若多次滴定平均消耗KMnO4溶液的体积为VmL,则产品中Mn的质量分数为_______ 。
(5)下列操作会使得测定结果偏大的是_______。
[探究一]制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为
(2)装置C中的反应温度需要控制在0°C左右,控制温度的方法是
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为
[探究二]测定产品中Mn的质量分数
称取ag产品充分加热使其分解为MnSO4,然后加水溶解,用cmol·L-1的KMnO4溶液进行滴定(Mn元素均转化为MnO2)。
(4)若多次滴定平均消耗KMnO4溶液的体积为VmL,则产品中Mn的质量分数为
(5)下列操作会使得测定结果偏大的是_______。
| A.滴定前锥形瓶用蒸馏水洗后未用待测MnSO4溶液润洗 |
| B.滴定前滴定管中尖嘴处有气泡,滴定后气泡消失 |
| C.滴定前平视读数,滴定结束俯视读数 |
| D.对连二硫酸锰产品进行加热操作时加热不充分 |
2023·四川凉山·三模 查看更多[4]
四川省凉山彝族自治州2023届高三下学期第三次诊断性检测理综化学试题(已下线)物质含量的测定(已下线)2019年高考浙江卷化学试题变式题(实验题)四川省宜宾市第四中学校2023-2024学年高三上学期开学理综化学试题
更新时间:2023-05-25 07:08:18
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】由于雾霾严重,长沙市19年12月15、16日在部分路段施行了限行。已知汽车尾气排放出的 、
、 等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
(1)汽车尾气中的 和
和 在一定温度和催化剂条件下可发生如下反应:
在一定温度和催化剂条件下可发生如下反应:
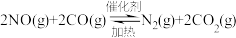

已知:① 燃烧热的
燃烧热的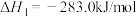
②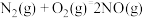
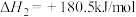 ,则
,则
__________ 。
(2)某研究小组对反应
 进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比
进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比 进行多组实验(各次实验的温度可能相同,也可能不同),测定
进行多组实验(各次实验的温度可能相同,也可能不同),测定 的平衡转化率
的平衡转化率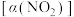 ,部分实验结果如图1所示。
,部分实验结果如图1所示。

①如果将图中 点的平衡状态改变为
点的平衡状态改变为 点的平衡状态,应采取的措施是
点的平衡状态,应采取的措施是__________ 。
②图中 、
、 两点对应的实验温度分别为
两点对应的实验温度分别为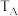 和
和 ,通过判断:
,通过判断: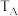
__________  (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(3)工业废气也是产生雾霾的重要原因,某厂采用湿法 氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
① 水解时生成
水解时生成 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:____________________ 。
②过二硫酸钾可通过电解 溶液的方法制得。电解液中含硫微粒主要存在形式与
溶液的方法制得。电解液中含硫微粒主要存在形式与 的关系如图2所示。
的关系如图2所示。
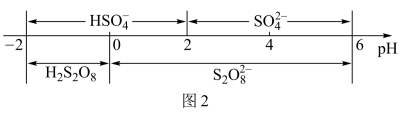
已知在阳极放电的离子主要是 ,阳极区电解质溶液的
,阳极区电解质溶液的 范围为
范围为__________ ;阳极的电极反应式为______________________________ 。
 、
、 等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。(1)汽车尾气中的
 和
和 在一定温度和催化剂条件下可发生如下反应:
在一定温度和催化剂条件下可发生如下反应: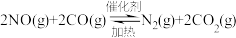

已知:①
 燃烧热的
燃烧热的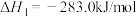
②
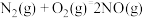
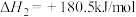 ,则
,则
(2)某研究小组对反应

 进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比
进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比 进行多组实验(各次实验的温度可能相同,也可能不同),测定
进行多组实验(各次实验的温度可能相同,也可能不同),测定 的平衡转化率
的平衡转化率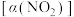 ,部分实验结果如图1所示。
,部分实验结果如图1所示。
①如果将图中
 点的平衡状态改变为
点的平衡状态改变为 点的平衡状态,应采取的措施是
点的平衡状态,应采取的措施是②图中
 、
、 两点对应的实验温度分别为
两点对应的实验温度分别为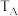 和
和 ,通过判断:
,通过判断: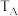
 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。(3)工业废气也是产生雾霾的重要原因,某厂采用湿法
 氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。①
 水解时生成
水解时生成 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:②过二硫酸钾可通过电解
 溶液的方法制得。电解液中含硫微粒主要存在形式与
溶液的方法制得。电解液中含硫微粒主要存在形式与 的关系如图2所示。
的关系如图2所示。
已知在阳极放电的离子主要是
 ,阳极区电解质溶液的
,阳极区电解质溶液的 范围为
范围为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】三氧化二铬 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化:
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。
(1)写出溶液B中的所有阳离子__________ 。写出步骤Ⅱ中生成气体C的离子方程式__________ 。沉淀E的化学式为__________ 。
(2)下列说法正确的是__________。
(3)在碱性条件下, 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式__________ 。根据该反应原理,设计实验检验上述反应后溶液中生成的阴离子__________ 。
 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化: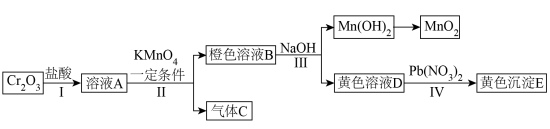
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数
 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。(1)写出溶液B中的所有阳离子
(2)下列说法正确的是__________。
| A.气体C在工业上可通过电解法制备 |
| B.在溶液B中加入乙醇,溶液变为绿色,再变为蓝色 |
| C.将步骤Ⅰ中的盐酸换成硫酸,仅影响步骤Ⅱ的反应 |
| D.在步骤Ⅲ中,溶液B加入纯碱溶液,也能分离出锰元素 |
(3)在碱性条件下,
 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】某研究小组利用某酸性腐蚀废液(含 、
、 、
、 、
、 ),制取铵明矾
),制取铵明矾 的流程如下:
的流程如下:
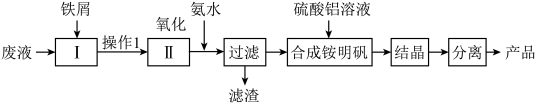
回答下列问题:
(1)请写出加入铁屑时发生反应的离子方程式:___________ 。
(2)为了使步骤Ⅱ中氧化不引入新的杂质,最好选用的氧化剂是___________ (填化学式)。
(3)检验溶液中含有 的方法是
的方法是___________ 。
(4)工业上将流程中产生的滤渣用 碱性溶液氧化可生成一种高效净水剂
碱性溶液氧化可生成一种高效净水剂 ,写出对应的离子方程式:
,写出对应的离子方程式:___________ 。
(5)固体铵明矾加热过程中,固体质量随温度的变化如图所示[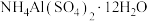 的相对分子质量为
的相对分子质量为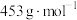 ]。
]。
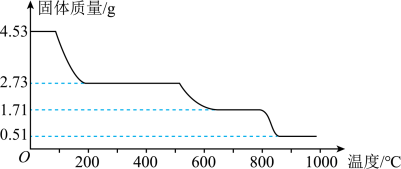
若将铵明矾加热灼烧,400℃时剩余固体成分的化学式为___________ 。
 、
、 、
、 、
、 ),制取铵明矾
),制取铵明矾 的流程如下:
的流程如下:
回答下列问题:
(1)请写出加入铁屑时发生反应的离子方程式:
(2)为了使步骤Ⅱ中氧化不引入新的杂质,最好选用的氧化剂是
(3)检验溶液中含有
 的方法是
的方法是(4)工业上将流程中产生的滤渣用
 碱性溶液氧化可生成一种高效净水剂
碱性溶液氧化可生成一种高效净水剂 ,写出对应的离子方程式:
,写出对应的离子方程式:(5)固体铵明矾加热过程中,固体质量随温度的变化如图所示[
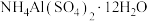 的相对分子质量为
的相对分子质量为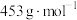 ]。
]。
若将铵明矾加热灼烧,400℃时剩余固体成分的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末,微溶于水,不溶于乙醇和稀硫酸;在空气中迅速被氧化成绿色;见光则易分解,变成褐色,下图是实验室制备CuCl的装置:
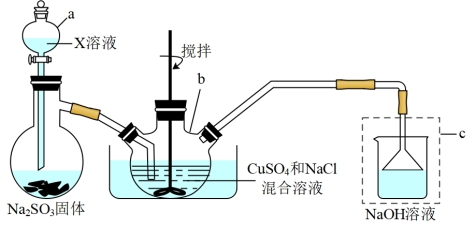
实验步骤:
①将含硫酸铜和氯化钠的水溶液加热至60-70°C,通入二氧化硫气体,直至不再生成氧化亚铜为止。
②过滤得到氯化亚铜,用亚硫酸洗涤,然后用冰醋酸洗涤至洗涤液变成无色,随后将沉淀置于蒸发皿上,用水浴加热蒸发,直到乙酸的气味消失,最后将产物密封保存。
回答下列问题:
(1)仪器a的名称是_______ ;装置c中漏斗的作用为_______ 。
(2)仪器b中发生反应的离子方程式为_______ 。
(3)下列说法正确的是_______。
(4)CuCl晶体用亚硫酸洗涤的目的是_______ 。
(5)氯化亚铜定量分析:
①称取样品0.1000g置于预先放置10mLFeCl3溶液的锥形瓶,不断晃动,待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
②立即用0.1000mol·L-1Ce(SO4)2标准溶液滴定至绿色出现为终点,消耗10.00mLCe(SO4)2溶液,则CuCl的纯度为_______ 。(已知:Fe3++CuCl=Fe2++Cu2++Cl—;Fe2++Ce4+=Fe3++Ce3+)

实验步骤:
①将含硫酸铜和氯化钠的水溶液加热至60-70°C,通入二氧化硫气体,直至不再生成氧化亚铜为止。
②过滤得到氯化亚铜,用亚硫酸洗涤,然后用冰醋酸洗涤至洗涤液变成无色,随后将沉淀置于蒸发皿上,用水浴加热蒸发,直到乙酸的气味消失,最后将产物密封保存。
回答下列问题:
(1)仪器a的名称是
(2)仪器b中发生反应的离子方程式为
(3)下列说法正确的是_______。
| A.X溶液可选用98%浓硫酸 |
| B.搅拌器搅拌的目的是为了加快反应速率 |
| C.装置C中可用Ca(OH)2溶液替代 |
| D.氯化亚铜应保存在棕色细口瓶中 |
(5)氯化亚铜定量分析:
①称取样品0.1000g置于预先放置10mLFeCl3溶液的锥形瓶,不断晃动,待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
②立即用0.1000mol·L-1Ce(SO4)2标准溶液滴定至绿色出现为终点,消耗10.00mLCe(SO4)2溶液,则CuCl的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】 易溶于水和乙醇,在酸性条件下还原性较差,碱性条件下较强。某实验小组用如下装置制备
易溶于水和乙醇,在酸性条件下还原性较差,碱性条件下较强。某实验小组用如下装置制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:
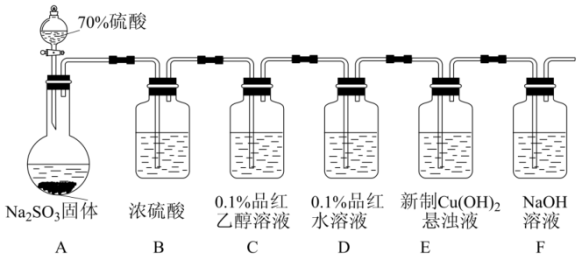
(1)装置B中浓硫酸的作用是_______ ;实验中观察到:装置C中溶液红色没有褪去,装置D中溶液红色褪去。由此可得出的结论是_______ 。
(2)为了进一步探究使品红褪色的主要微粒,进行如下系列实验:
综合上述实验推知, 水溶液使品红褪色时起主要作用的微粒是
水溶液使品红褪色时起主要作用的微粒是_______ (填微粒符号)。
(3)用 溶液和
溶液和 溶液制备新制
溶液制备新制 悬浊液,实验中观察到:装置E中生成大量白色沉淀,溶液呈绿色,与
悬浊液,实验中观察到:装置E中生成大量白色沉淀,溶液呈绿色,与 溶液、
溶液、 溶液的颜色明显不同。
溶液的颜色明显不同。
①为探究白色沉淀的成分,查阅资料如下:CuCl为白色固体,难溶于水,与氨水反应生成 ,在空气中立即被氧化成含有
,在空气中立即被氧化成含有 的蓝色溶液。甲同学向洗涤后的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为
的蓝色溶液。甲同学向洗涤后的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为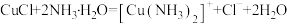 、
、_______ 。装置E中生成白色沉淀的离子方程式为_______ 。
②取少量E中滤液,加入少量稀盐酸,产生无色刺激性气味气体,得到澄清蓝色溶液,故推断溶液显绿色的原因可能是溶液中含有较多 。为进一步实验确认这种可能性,向少量
。为进一步实验确认这种可能性,向少量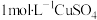 溶液中加入
溶液中加入_______ (填化学式),得到绿色溶液。
 易溶于水和乙醇,在酸性条件下还原性较差,碱性条件下较强。某实验小组用如下装置制备
易溶于水和乙醇,在酸性条件下还原性较差,碱性条件下较强。某实验小组用如下装置制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:
(1)装置B中浓硫酸的作用是
(2)为了进一步探究使品红褪色的主要微粒,进行如下系列实验:
| 实验 | 试管中的溶液 | 滴入溶液 | 实验现象 |
| a | 2mL  溶液(pH=2) 溶液(pH=2) | 各滴入1滴0.1%品红溶液 | 溶液变红逐渐变浅,约90s后完全褪色 |
| b | 2mL 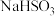 溶液(pH=5) 溶液(pH=5) | 溶液变红后立即变浅,约15s后完全褪色 | |
| C | 2mL  溶液(pH=10) 溶液(pH=10) | 溶液变红后立即褪色 |
 水溶液使品红褪色时起主要作用的微粒是
水溶液使品红褪色时起主要作用的微粒是(3)用
 溶液和
溶液和 溶液制备新制
溶液制备新制 悬浊液,实验中观察到:装置E中生成大量白色沉淀,溶液呈绿色,与
悬浊液,实验中观察到:装置E中生成大量白色沉淀,溶液呈绿色,与 溶液、
溶液、 溶液的颜色明显不同。
溶液的颜色明显不同。①为探究白色沉淀的成分,查阅资料如下:CuCl为白色固体,难溶于水,与氨水反应生成
 ,在空气中立即被氧化成含有
,在空气中立即被氧化成含有 的蓝色溶液。甲同学向洗涤后的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为
的蓝色溶液。甲同学向洗涤后的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为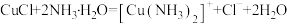 、
、②取少量E中滤液,加入少量稀盐酸,产生无色刺激性气味气体,得到澄清蓝色溶液,故推断溶液显绿色的原因可能是溶液中含有较多
 。为进一步实验确认这种可能性,向少量
。为进一步实验确认这种可能性,向少量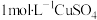 溶液中加入
溶液中加入
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】Ⅰ.部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。
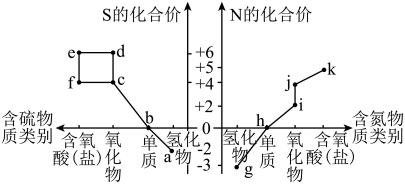
回答下列问题:
(1)j的化学名称是___________ 。
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是___________ (填字母)。
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将pH=1的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是___________ 。
Ⅱ.S4N4(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入S2Cl2的CCl4溶液中,可制得该物质:6S2Cl2+16g=S4N4+S8+12NH4Cl(已知S8是硫单质中最稳定的)。
(4)上述制备反应中,物质g体现的性质有___________ ,其中被氧化的元素是___________ (填元素符号)。
(5)S4N4在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是___________ 。
Ⅲ.二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得,氯气过量则会生成SCl2,S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
(6)该固体是___________ (填名称)。
(7)甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案___________ (填“可行”或“不可行”),原因是___________ 。
(8)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1.25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。
则产品中氯元素的质量分数为___________ ,由此可知产品中___________ (填“含有”或“不含有”)SCl2杂质。

回答下列问题:
(1)j的化学名称是
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将pH=1的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是
Ⅱ.S4N4(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入S2Cl2的CCl4溶液中,可制得该物质:6S2Cl2+16g=S4N4+S8+12NH4Cl(已知S8是硫单质中最稳定的)。
(4)上述制备反应中,物质g体现的性质有
(5)S4N4在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是
Ⅲ.二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得,氯气过量则会生成SCl2,S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
(6)该固体是
(7)甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案
(8)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1.25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。
则产品中氯元素的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】Ⅰ.某学生用 的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入 的标准NaOH溶液至“0”刻度线以上;
的标准NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记录读数;
②量取20.00 mL待测液注入洁净的锥形瓶中,并加入2~3滴酚酞试液;
⑤用标准NaOH溶液滴定至终点,记下滴定管液面读数;
⑥重复以上滴定操作2~3次。
请回答下列问题:
(1)以上步骤有错误的是_______ (填编号),该步骤错误操作会导致测定结果_______ (填“偏大”“偏小”或“无影响”)。
(2)下列操作会导致上述所测盐酸溶液的浓度偏高的是_______(填正确答案标号)。
Ⅱ.乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(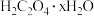 )进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(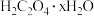 )中的x值。
)中的x值。
通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性 溶液进行滴定:
溶液进行滴定: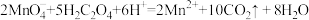
学习小组的同学设计了滴定的方法测定x值
①称取1.260g纯草酸晶体,将其制成100.00 mL水溶液为待测液
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀
③用浓度为 的
的 标准溶液进行滴定,达到终点记录消耗体积。
标准溶液进行滴定,达到终点记录消耗体积。
(3)滴定时,将酸性 标准液装在如图中的
标准液装在如图中的_______ (填“甲”或“乙”)滴定管中。
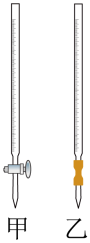
(4)滴定时,左手操作滴定管,右手轻轻摇动锥形瓶,眼睛注视_______ 。
(5)本实验滴定达到终点的标志是_______ 。
(6)为了提高实验的准确性,学习小组共进行3次实验,记录数据如下表:
通过上述数据,可知消耗的 溶液体积为
溶液体积为_______ mL,该“一定质量”草酸晶体中含n(H2C2O4)=_______ mol。
 的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:①用蒸馏水洗涤碱式滴定管,注入
 的标准NaOH溶液至“0”刻度线以上;
的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记录读数;
②量取20.00 mL待测液注入洁净的锥形瓶中,并加入2~3滴酚酞试液;
⑤用标准NaOH溶液滴定至终点,记下滴定管液面读数;
⑥重复以上滴定操作2~3次。
请回答下列问题:
(1)以上步骤有错误的是
(2)下列操作会导致上述所测盐酸溶液的浓度偏高的是_______(填正确答案标号)。
| A.滴定达到终点时,俯视滴定管内液面读数 |
| B.碱式滴定管尖嘴部分开始有气泡,滴定后消失 |
| C.锥形瓶用蒸馏水洗净后未干燥就装入盐酸待测液 |
| D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
Ⅱ.乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(
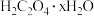 )进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。该组同学的研究课题是:探究测定草酸晶体(
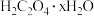 )中的x值。
)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性
 溶液进行滴定:
溶液进行滴定: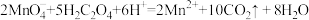
学习小组的同学设计了滴定的方法测定x值
①称取1.260g纯草酸晶体,将其制成100.00 mL水溶液为待测液
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀

③用浓度为
 的
的 标准溶液进行滴定,达到终点记录消耗体积。
标准溶液进行滴定,达到终点记录消耗体积。(3)滴定时,将酸性
 标准液装在如图中的
标准液装在如图中的
(4)滴定时,左手操作滴定管,右手轻轻摇动锥形瓶,眼睛注视
(5)本实验滴定达到终点的标志是
(6)为了提高实验的准确性,学习小组共进行3次实验,记录数据如下表:
| 待测液/mL | 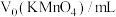 | 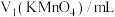 |
| 25.00 | 0.00 | 9.95 |
| 25.00 | 1.05 | 11.10 |
| 25.00 | 0.50 | 13.50 |
 溶液体积为
溶液体积为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】硫氰酸钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰酸钾,并进行相关实验探究。 、水和催化剂,发生反应
、水和催化剂,发生反应 ,该反应比较缓慢且
,该反应比较缓慢且 高于
高于 时易分解,
时易分解, 在高于
在高于 时即分解。
时即分解。
(1)D中盛装 溶液的仪器名称为
溶液的仪器名称为___________ ,E中球形干燥管的作用为___________ 。
(2)制备 溶液:将D中反应混合液加热至
溶液:将D中反应混合液加热至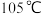 ,打开
,打开 通入氨气。反应一段时间后,关闭
通入氨气。反应一段时间后,关闭 ,保持三颈烧瓶内反应混合液温度为
,保持三颈烧瓶内反应混合液温度为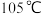 一段时间,该过程的目的为
一段时间,该过程的目的为___________ ;打开 ,缓缓滴入适量的
,缓缓滴入适量的 溶液,继续保持反应混合液温度为
溶液,继续保持反应混合液温度为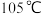 。
。
(3)装置E中发生氧化还原反应的离子方程式是___________ 。
(4)将制备所得硫氰酸钾晶体进行 含量的测定:称取
含量的测定:称取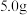 样品,配成
样品,配成 溶液。量取
溶液。量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴 ,用
,用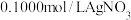 标准溶液滴定,平行滴定四次,消耗标准溶液体积分别为
标准溶液滴定,平行滴定四次,消耗标准溶液体积分别为 ,
,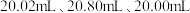 。[已知:滴定时发生的反应为
。[已知:滴定时发生的反应为 白色]
白色]
①滴定终点的现象为___________ 。
②晶体中 的质量分数为
的质量分数为___________ ( 的摩尔质量为
的摩尔质量为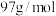 )。
)。
③下列操作或说法正确的是___________ (填标号)。
A.用量筒量取 溶液于锥形瓶中
溶液于锥形瓶中
B.锥形瓶洗净后未干燥,会导致测定结果偏低
C.读数时可以将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.滴定前平视读数,滴定后仰视读数,会导致测定结果偏高
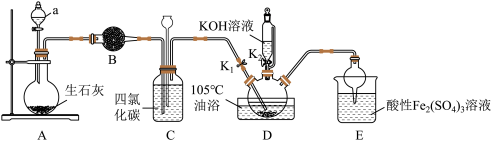
 、水和催化剂,发生反应
、水和催化剂,发生反应 ,该反应比较缓慢且
,该反应比较缓慢且 高于
高于 时易分解,
时易分解, 在高于
在高于 时即分解。
时即分解。(1)D中盛装
 溶液的仪器名称为
溶液的仪器名称为(2)制备
 溶液:将D中反应混合液加热至
溶液:将D中反应混合液加热至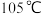 ,打开
,打开 通入氨气。反应一段时间后,关闭
通入氨气。反应一段时间后,关闭 ,保持三颈烧瓶内反应混合液温度为
,保持三颈烧瓶内反应混合液温度为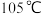 一段时间,该过程的目的为
一段时间,该过程的目的为 ,缓缓滴入适量的
,缓缓滴入适量的 溶液,继续保持反应混合液温度为
溶液,继续保持反应混合液温度为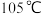 。
。(3)装置E中发生氧化还原反应的离子方程式是
(4)将制备所得硫氰酸钾晶体进行
 含量的测定:称取
含量的测定:称取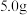 样品,配成
样品,配成 溶液。量取
溶液。量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴 ,用
,用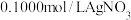 标准溶液滴定,平行滴定四次,消耗标准溶液体积分别为
标准溶液滴定,平行滴定四次,消耗标准溶液体积分别为 ,
,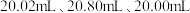 。[已知:滴定时发生的反应为
。[已知:滴定时发生的反应为 白色]
白色]①滴定终点的现象为
②晶体中
 的质量分数为
的质量分数为 的摩尔质量为
的摩尔质量为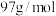 )。
)。③下列操作或说法正确的是
A.用量筒量取
 溶液于锥形瓶中
溶液于锥形瓶中B.锥形瓶洗净后未干燥,会导致测定结果偏低
C.读数时可以将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.滴定前平视读数,滴定后仰视读数,会导致测定结果偏高
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】硼酸(H3BO3能溶于水,可用于玻璃、医药、纺织等工业;碳酸镁可用于制造防火涂料、牙膏等。某工厂以硼镁铁矿(主要成分为Mg2B2O5H2O,杂质有SiO2、FeO、Fe2O3、AI2O3)为原料制备硼酸、碳酸镁的工艺流程如下图所示:
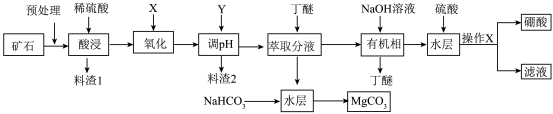
常温时实验条件下几种金属离子形成沉淀的pH
(1)预处理的内容包括矿石的筛选、_______ ,写出料渣1的一种用途_______ 。
(2)X是常用的绿色氧化剂,如O2、_______ ,写出酸浸时Mg2B2O5H2O与硫酸反应的化学方程式_______ 。
(3)为提高产品纯度,试剂Y为_______ (填化学式),写出加入NaHCO3溶液时的离子方程式_______ 。
(4)为测量所得硼酸纯度,取3.00g所制取的硼酸样品溶于甘露醇与蒸馏水混合溶液中,配成500mL溶液,然后取出25.00mL放入锥形瓶中并滴加3滴酚酞试液,用0.1000mol·L-1NaOH标准溶液滴定,滴定终点时消耗22.00mL标准溶液。则滴定终点时的现象是_______ ,样品中硼酸的纯度为_______ (滴定反应为H3BO3+OH-=[B(OH)4]-

常温时实验条件下几种金属离子形成沉淀的pH
| Fe3+ | Fe2+ | Al3+ | Mg2+ | |
| 开始沉淀 | 2.7 | 7.6 | 4.0 | 9.6 |
| 完全沉淀 | 3.2 | 9.6 | 5.2 | 11.1 |
(1)预处理的内容包括矿石的筛选、
(2)X是常用的绿色氧化剂,如O2、
(3)为提高产品纯度,试剂Y为
(4)为测量所得硼酸纯度,取3.00g所制取的硼酸样品溶于甘露醇与蒸馏水混合溶液中,配成500mL溶液,然后取出25.00mL放入锥形瓶中并滴加3滴酚酞试液,用0.1000mol·L-1NaOH标准溶液滴定,滴定终点时消耗22.00mL标准溶液。则滴定终点时的现象是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】LiCoO2是锂离子电池最早使用的电极材料,利用原钴矿(含Cr2O3、NiS等杂质)制备LiCoO2的工艺流程如下:
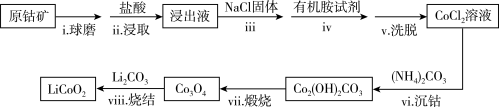
资料:i. 在含一定量Cl−的溶液中,钴离子以CoCl42-形式存在:Co2++4Cl− CoCl42−
CoCl42−
ii. CoCl42−溶于有机胺试剂,有机胺不溶于水。
iii. 盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:
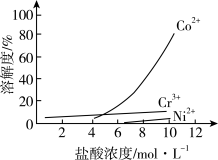
(1)步骤ii选用盐酸的浓度应为__________ 。
a. 4 mol/L b. 6 mol/L c. 10 mol/L
(2)从平衡移动角度解释步骤ⅲ中加入NaCl固体的目的_____________ 。
(3)步骤iv的操作是_______ 。
(4)步骤vi用(NH4)2CO3作沉淀剂,在一定条件下得到碱式碳酸钴(Co2(OH)2CO3)。实验测得在一段时间内加入等量(NH4)2CO3所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因____________ 。
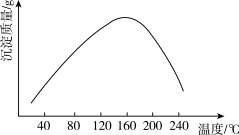
(5)步骤viii中Co3O4 和Li2CO3 混合后,鼓入空气,经高温烧结得到LiCoO2。该反应的化学方程式是_____________ 。
(6)锂离子电池的工作原理如图,充、放电过程中,Li+在LiCoO2电极和碳电极之间传递。电池的总反应为:LixC + Li1-xCoO2 C+LiCoO2
C+LiCoO2
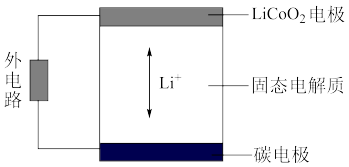
①放电时,电池的负极是______ 。
②充电时,电池的阴极反应式是______ 。

资料:i. 在含一定量Cl−的溶液中,钴离子以CoCl42-形式存在:Co2++4Cl−
 CoCl42−
CoCl42−ii. CoCl42−溶于有机胺试剂,有机胺不溶于水。
iii. 盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:

(1)步骤ii选用盐酸的浓度应为
a. 4 mol/L b. 6 mol/L c. 10 mol/L
(2)从平衡移动角度解释步骤ⅲ中加入NaCl固体的目的
(3)步骤iv的操作是
(4)步骤vi用(NH4)2CO3作沉淀剂,在一定条件下得到碱式碳酸钴(Co2(OH)2CO3)。实验测得在一段时间内加入等量(NH4)2CO3所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因

(5)步骤viii中Co3O4 和Li2CO3 混合后,鼓入空气,经高温烧结得到LiCoO2。该反应的化学方程式是
(6)锂离子电池的工作原理如图,充、放电过程中,Li+在LiCoO2电极和碳电极之间传递。电池的总反应为:LixC + Li1-xCoO2
 C+LiCoO2
C+LiCoO2
①放电时,电池的负极是
②充电时,电池的阴极反应式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】常温下,三硫代碳酸钠(Na2CS3)是玫瑰红色针状固体,与碳酸钠性质相近。在工农业生产中有广泛的用途。某小组设计实验探究三硫代碳酸钠的性质并测定其溶液的浓度。
实验一:探究Na2CS3的性质
(1)向Na2CS3溶液中滴入酚酞试液,溶液变红色。用离子方程式说明溶液呈碱性的原因____________________________________________ 。
实验二:测定Na2CS3溶液的浓度
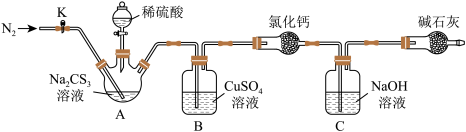
按如图所示连接好装置,职50.0 mL Na2CS3溶液置于三颈瓶中,打开分液漏斗的活塞,滴入足量2.0 mol·L-1稀H2SO4,关闭活塞。已知:Na2CS3+H2SO4=Na2SO4+CS2+H2S↑。CS2和H2S均有毒。CS2不溶于水,沸点46℃,密度1.26 g·mL-1,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。
(2)盛放稀硫酸的仪器的名称是___________ ,碱石灰的作用是________________________ 。
(3)反应结束后打开活塞K,再缓慢通入热N2一段时间,其目的是____________________ 。
(4)B中发生反应的离子方程式是___________________________________ 。
(5)为了计算Na2CS3溶液的浓度,对充分反应后B中混合物进行过滤洗涤、干燥、称重,得8.4 g固体,则三颈瓶中Na2CS3的物质的量浓度为_________ 。
(6)分析上述实验方案,还可以通过测定C中溶液质量的增加值来计算Na2CS3溶液的浓度,若反应结束后将通热N2改为通热空气,计算值___________ (填“偏高”、“偏低”或“无影响”)。
实验一:探究Na2CS3的性质
(1)向Na2CS3溶液中滴入酚酞试液,溶液变红色。用离子方程式说明溶液呈碱性的原因
实验二:测定Na2CS3溶液的浓度

按如图所示连接好装置,职50.0 mL Na2CS3溶液置于三颈瓶中,打开分液漏斗的活塞,滴入足量2.0 mol·L-1稀H2SO4,关闭活塞。已知:Na2CS3+H2SO4=Na2SO4+CS2+H2S↑。CS2和H2S均有毒。CS2不溶于水,沸点46℃,密度1.26 g·mL-1,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。
(2)盛放稀硫酸的仪器的名称是
(3)反应结束后打开活塞K,再缓慢通入热N2一段时间,其目的是
(4)B中发生反应的离子方程式是
(5)为了计算Na2CS3溶液的浓度,对充分反应后B中混合物进行过滤洗涤、干燥、称重,得8.4 g固体,则三颈瓶中Na2CS3的物质的量浓度为
(6)分析上述实验方案,还可以通过测定C中溶液质量的增加值来计算Na2CS3溶液的浓度,若反应结束后将通热N2改为通热空气,计算值
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】以 为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废
为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废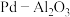 催化剂(主要含有Pd、
催化剂(主要含有Pd、 ,还有少量PdO、
,还有少量PdO、 、C)为原料制备氯化钯的流程如下:
、C)为原料制备氯化钯的流程如下:
(1)“氯化浸出”前必须“焙烧”去除废催化剂表面积碳,原因是_______ ,焙烧时间过长,“氯化浸出”率下降,可能的原因是_______ 。
(2) 中Cl原子的杂化类型是
中Cl原子的杂化类型是_______ ,“氯化浸出”时,若盐酸浓度过高,可能发生的副反应离子方程式为_______ 。
(3)滤渣1主要成分为_______ ,已知 ,若要使溶液中
,若要使溶液中 不高于
不高于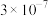 ,则应加入氨水使pH不低于
,则应加入氨水使pH不低于_______ 。
(4)工业上也可用 还原
还原 制取海绵Pd,该历程对环境友好。该反应的化学方程式为
制取海绵Pd,该历程对环境友好。该反应的化学方程式为_______ 。
(5)工业上测定Pd含量的原理为:试样用硝酸及盐酸溶解后,加过量EDTA络合钯,用锌标准溶液滴定过剩的EDTA.具体步聚如下:
I.标定锌标准溶液对钯的滴定度:
a.吸取25mLEDTA溶液置于烧杯中,滴加4~5滴盐酸,加适量水,用锌标准溶液滴定至终点,消耗锌标准溶液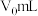 。
。
b.吸取15mL含0.0010gPd的Pd标准溶液于烧杯中,加入25mLEDTA溶液,加适量水用锌标准溶液滴定至试液由黄色变成紫红色为终点,消耗锌标准溶液 。
。
Ⅱ.滴定式样:
称取0.1000g试样置于烧杯中,加适量硝酸及盐酸充分溶解并作妥善处理,加入25mLEDT溶液,用锌标准溶液滴定至终点,消耗锌标准溶液VmL。则试样中Pd的质量分数为_______ %(用含V、 、
、 的式子表示)。
的式子表示)。
 为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废
为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废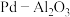 催化剂(主要含有Pd、
催化剂(主要含有Pd、 ,还有少量PdO、
,还有少量PdO、 、C)为原料制备氯化钯的流程如下:
、C)为原料制备氯化钯的流程如下: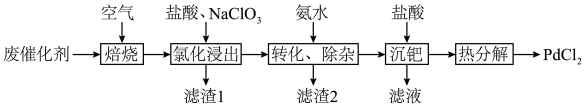
(1)“氯化浸出”前必须“焙烧”去除废催化剂表面积碳,原因是
(2)
 中Cl原子的杂化类型是
中Cl原子的杂化类型是(3)滤渣1主要成分为
 ,若要使溶液中
,若要使溶液中 不高于
不高于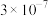 ,则应加入氨水使pH不低于
,则应加入氨水使pH不低于(4)工业上也可用
 还原
还原 制取海绵Pd,该历程对环境友好。该反应的化学方程式为
制取海绵Pd,该历程对环境友好。该反应的化学方程式为(5)工业上测定Pd含量的原理为:试样用硝酸及盐酸溶解后,加过量EDTA络合钯,用锌标准溶液滴定过剩的EDTA.具体步聚如下:
I.标定锌标准溶液对钯的滴定度:
a.吸取25mLEDTA溶液置于烧杯中,滴加4~5滴盐酸,加适量水,用锌标准溶液滴定至终点,消耗锌标准溶液
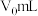 。
。b.吸取15mL含0.0010gPd的Pd标准溶液于烧杯中,加入25mLEDTA溶液,加适量水用锌标准溶液滴定至试液由黄色变成紫红色为终点,消耗锌标准溶液
 。
。Ⅱ.滴定式样:
称取0.1000g试样置于烧杯中,加适量硝酸及盐酸充分溶解并作妥善处理,加入25mLEDT溶液,用锌标准溶液滴定至终点,消耗锌标准溶液VmL。则试样中Pd的质量分数为
 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次



