黑火药是我国古代四大发明之一,它的爆炸反应为: 。完成下列填空:
。完成下列填空:
(1)上述反应中的还原剂为___________ ,还原产物有___________ ,当有 参加反应时,转移电子的数目为
参加反应时,转移电子的数目为___________ 。
(2)写出K2S的电子式:___________ 。
(3)将SO2和Cl2分别通入品红溶液中,产生的现象是___________ ;若将SO2和Cl2等体积混合后再缓缓通入品红溶液,发现品红溶液___________ ,其原因是___________ (用化学方程式解释原因)。
(4)S、C和N三种元素的原子半径从小到大的顺序是___________ 。
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有___________。
(6)硫和氮及其化合物对人类生存和社会发展意义重大,但也造成了不少环境问题,下列说法正确的是___________。
 。完成下列填空:
。完成下列填空:(1)上述反应中的还原剂为
 参加反应时,转移电子的数目为
参加反应时,转移电子的数目为(2)写出K2S的电子式:
(3)将SO2和Cl2分别通入品红溶液中,产生的现象是
(4)S、C和N三种元素的原子半径从小到大的顺序是
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有___________。
| A.单质熔点:C>S | B.酸性: |
C. 中碳元素为 中碳元素为 价,硫元素为 价,硫元素为 价 价 | D.分解温度: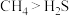 |
A.雷雨天气有助于空气中的 转化为可供植物吸收的 转化为可供植物吸收的 |
B.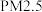 (微粒直径约为 (微粒直径约为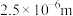 )含氮的分散质分散在空气中形成胶体,能产生丁达尔效应 )含氮的分散质分散在空气中形成胶体,能产生丁达尔效应 |
| C.二氧化硫有毒,严禁将其添加到任何食品和饮品中 |
| D.“酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成的 |
更新时间:2023-05-01 22:21:20
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】按要求完成下列问题
(1)已知实验室制备NO的反应为: 。反应中氧化剂是
。反应中氧化剂是_______ ; 被氧化的元素是_______ ;氧化产物是_______ 。
(2)请配平下列方程式_______
_______Al +_______ + _______NaOH= _______
+ _______NaOH= _______ + _______
+ _______ ↑ + _______
↑ + _______
(3)用 溶液与Cu反应制作的印刷电路板,其制作原理可用
溶液与Cu反应制作的印刷电路板,其制作原理可用 表示。
表示。
①上式中X的化学式为_______ 。
②该反应的离子方程式为_______ 。
③请写出反应物氯化铁的电离方程式_______ 。
(1)已知实验室制备NO的反应为:
 。反应中氧化剂是
。反应中氧化剂是(2)请配平下列方程式
_______Al +_______
 + _______NaOH= _______
+ _______NaOH= _______ + _______
+ _______ ↑ + _______
↑ + _______
(3)用
 溶液与Cu反应制作的印刷电路板,其制作原理可用
溶液与Cu反应制作的印刷电路板,其制作原理可用 表示。
表示。①上式中X的化学式为
②该反应的离子方程式为
③请写出反应物氯化铁的电离方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】钛及其合金在航空航天、生物医学等领域具有非常重要的应用价值和广阔的应用前景,可通过下面的转化制取:

(1)反应①的化学方程式为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为___________ ,发生氧化反应的物质为___________ 。
(2)反应②中,若在标准状况下有5.6L CO参与反应,则转移电子数为___________ ,反应②中生成的甲醇属于___________ 。
A.氧化物 B.碱 C.有机物 D.电解质 E.非电解质
(3)“反应③”须在无氧和非水性 溶剂中进行,原因是___________ 。

(1)反应①的化学方程式为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为
(2)反应②中,若在标准状况下有5.6L CO参与反应,则转移电子数为
A.氧化物 B.碱 C.有机物 D.电解质 E.非电解质
(3)“反应③”须在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以含硅废石(主要成分为SiO2、含少量Fe3O4、Al2O3等杂质)为原料,工业上有以下两种制备高纯硅的工艺。已知:SiCl4沸点57.7℃,遇水强烈水解;SiHCl3沸点31.5℃,且能与H2O强烈反应,并在空气中易自燃。
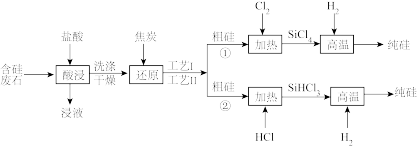
(1) 元素位于元素周期表
元素位于元素周期表_______ ,在硅酸盐中,Si和O构成了_______ 结构。
(2)酸浸所得的浸液中含有的金属离子是_______ 。
(3)写出还原过程的化学方程式_______ 。
(4)写出工艺II在高温条件下制备纯硅这一步的化学方程式:_______ ,工艺II与工艺I相比,其优点是_______ 。
(5)氮化硅陶瓷因其熔点高、耐高温、耐磨蚀,越来越多地被应用于高温等领域,氮化硅的化学式为_______ ,在高温烧结氮化硅陶瓷的过程中,二氧化硅、碳、氮气以物质的量之比为3∶6∶2发生反应生成两种化合物,反应中氧化剂与还原剂的质量之比为_______ 。

(1)
 元素位于元素周期表
元素位于元素周期表(2)酸浸所得的浸液中含有的金属离子是
(3)写出还原过程的化学方程式
(4)写出工艺II在高温条件下制备纯硅这一步的化学方程式:
(5)氮化硅陶瓷因其熔点高、耐高温、耐磨蚀,越来越多地被应用于高温等领域,氮化硅的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】为消除燃煤烟气中的SO2、NOx,研究者提出了若干烟气“脱硫”、“脱硝”的方法。
(1)利用氨水可以吸收SO2、NO2,原理如下图所示:

①氨水吸收SO2的化学方程式为___________ ;
②铵盐溶液中的主要溶质是___________ (填化学式);
③铵盐溶液要减压蒸发的原因是___________ 。
(2)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”。控制溶液的pH=5.5,将烟气中的SO2、NO转化为 、
、 。
。
①次氯酸钠中含有的化学键类型是___________ ;
②NaClO溶液吸收烟气中NO的离子方程式是___________ ;
一定时间内,温度对硫、硝脱除率的影响曲线如图,SO2的脱除率高于NO,可能的原因是___________ (写出1种即可)。

③烟气中SO2和NO的体积比为3∶1,50℃时的脱除率见图,则此吸收液中烟气转化生成的 和Cl−的物质的量之比为
和Cl−的物质的量之比为___________ 。
(1)利用氨水可以吸收SO2、NO2,原理如下图所示:

①氨水吸收SO2的化学方程式为
②铵盐溶液中的主要溶质是
③铵盐溶液要减压蒸发的原因是
(2)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”。控制溶液的pH=5.5,将烟气中的SO2、NO转化为
 、
、 。
。①次氯酸钠中含有的化学键类型是
②NaClO溶液吸收烟气中NO的离子方程式是
一定时间内,温度对硫、硝脱除率的影响曲线如图,SO2的脱除率高于NO,可能的原因是

③烟气中SO2和NO的体积比为3∶1,50℃时的脱除率见图,则此吸收液中烟气转化生成的
 和Cl−的物质的量之比为
和Cl−的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】控制和治理二氧化硫,是解决酸雨问题的有效途径。
(1)SO2是酸性氧化物,可用NaOH溶液吸收含SO2的尾气,该反应的化学方程式为________ 。
(2)用NaClO碱性溶液吸收二氧化硫。工业上控制在40℃~50℃时,将含有SO2的烟气和NaClO碱性溶液按图示方式通入反应釜。

①实验室控制40℃~50℃采取的加热方式是_______ ;
②反应釜中反应的离子方程式为_______ ,该反应中,SO2表现出_______ (填写具体化学性质);
③反应釜中采用“气—液逆流”接触吸收法的优点是_______ 。
(3)碘、水吸收二氧化硫,具体流程如图所示。

已知∶I2易升华;硫酸是高沸点含氧酸,HI易挥发。
①在反应器中,控制温度不超过100℃的目的是_______ 。
②在分离器中,分离H2SO4和HI的方法为_______ (填字母)。
a.过滤 b.蒸馏 c.结晶
③I2、H2O吸收SO2的化学反应方程式为_______ 。
④该工艺中可以循环使用的物质是_______ 。
(1)SO2是酸性氧化物,可用NaOH溶液吸收含SO2的尾气,该反应的化学方程式为
(2)用NaClO碱性溶液吸收二氧化硫。工业上控制在40℃~50℃时,将含有SO2的烟气和NaClO碱性溶液按图示方式通入反应釜。

①实验室控制40℃~50℃采取的加热方式是
②反应釜中反应的离子方程式为
③反应釜中采用“气—液逆流”接触吸收法的优点是
(3)碘、水吸收二氧化硫,具体流程如图所示。

已知∶I2易升华;硫酸是高沸点含氧酸,HI易挥发。
①在反应器中,控制温度不超过100℃的目的是
②在分离器中,分离H2SO4和HI的方法为
a.过滤 b.蒸馏 c.结晶
③I2、H2O吸收SO2的化学反应方程式为
④该工艺中可以循环使用的物质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气中常含有CO、NOx等气体,为减轻污染,一般汽车都加装了“催化净化器”,可将汽车尾气中的有毒气体转化为无污染的气体。某化学兴趣小组在实验室模拟汽车尾气处理,设计了如图所示装置(部分夹持装置已略去)。

(1)装置(III)的主要作用为____ 。
(2)停止加热,打开活塞K,放入适量氧气时,装置(II)中可观察到的现象是____ 。
(3)汽车尾气中含有CO和NO,安装催化转化器,使它们发生反应生成无毒的两种气体,其中一种是单质该反应的化学方程式为____ 。

(1)装置(III)的主要作用为
(2)停止加热,打开活塞K,放入适量氧气时,装置(II)中可观察到的现象是
(3)汽车尾气中含有CO和NO,安装催化转化器,使它们发生反应生成无毒的两种气体,其中一种是单质该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E、F、G为七种短周期主族元素,原子序数依次增大。已知:A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、G在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17,质子数之和为31。D与F同周期,且在该周期中D元素的原子半径最大。回答下列问题:
(1)B、C、G的简单氢化物中稳定性最弱的是____ (填化学式)。
(2)G的某种氧化物能使酸性KMnO4溶液褪色,反应的离子方程式为____ 。
(3)B、C、D、E、F形成的简单离子半径由小到大的顺序为____ (用离子符号表示)。
(4)A与B能形成离子化合物A5B,A5B中既含离子键又含共价键,其电子式为____ ,该物质能与水剧烈反应生成两种气体,这两种气体的化学式是____ 。
(5)F的最高价氧化物对应的水化物和D的最高价氧化物对应的水化物的水溶液发生反应的离子方程式为____ 。
(1)B、C、G的简单氢化物中稳定性最弱的是
(2)G的某种氧化物能使酸性KMnO4溶液褪色,反应的离子方程式为
(3)B、C、D、E、F形成的简单离子半径由小到大的顺序为
(4)A与B能形成离子化合物A5B,A5B中既含离子键又含共价键,其电子式为
(5)F的最高价氧化物对应的水化物和D的最高价氧化物对应的水化物的水溶液发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素R、T、X、Y、Z原子序数依次增大,最外层电子数之和为22,R原子的最外层电子数是其内层电子数的2倍,T是地壳中含量最高的元素, 与T2-具有相同的电子层结构,Z与T同主族
与T2-具有相同的电子层结构,Z与T同主族
(1)T与X形成的化合物中含___________ (填“离子”或“共价”)键;写出X和Z形成的简单化合物的电子式:___________ 。
(2)Z的气态简单氢化物的热稳定性比T的___________ (填“强”或“弱”,下同);Z的最高价氧化物对应水化物的酸性比R的___________ 。
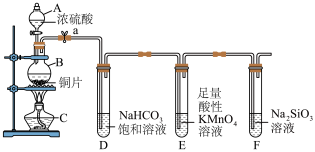
(3)某化学兴趣小组用如图装置探究元素R、Y的非金属性相对强弱:___________ 。
②试管D中通入过量 时发生反应的离子方程式为
时发生反应的离子方程式为___________ (已知酸性强弱:亚硫酸>碳酸)。
③装置E中酸性 溶液需要足量的原因是
溶液需要足量的原因是___________ 。
④能说明元素R的非金属性比元素Y的非金属性强的实验现象为___________ 。
 与T2-具有相同的电子层结构,Z与T同主族
与T2-具有相同的电子层结构,Z与T同主族(1)T与X形成的化合物中含
(2)Z的气态简单氢化物的热稳定性比T的
(3)某化学兴趣小组用如图装置探究元素R、Y的非金属性相对强弱:
②试管D中通入过量
 时发生反应的离子方程式为
时发生反应的离子方程式为③装置E中酸性
 溶液需要足量的原因是
溶液需要足量的原因是④能说明元素R的非金属性比元素Y的非金属性强的实验现象为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】完成下列问题。
(1)现有几种微粒或物质:①H、D、T;②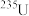 、
、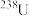 ;③
;③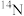 、
、 ;④
;④ 、
、 、
、 ;⑤
;⑤ 、
、 ;⑥金刚石、石墨;⑦
;⑥金刚石、石墨;⑦ 、
、 、
、 。互为同位素的是
。互为同位素的是______ (填序号,下同),互为同素异形体的是_____ ;①②③④中有_____ 种不同的核素,其中包括____ 种主族元素,______ 种短周期元素。
(2)下表为元素周期表的一部分,NA代表阿伏伽德罗常数的数值,请参照元素①-⑩在表中的位置,回答下列问题:

元素⑩在周期表中的位置是___________ ⑨对应离子结构示意图为___________ 。④⑧⑨⑩的气态氢化物中,最稳定的是___________ (用化学式表示)。⑤与①对应的单质隔绝空气加热得到的物质与水剧烈反应,若得到标况下3.36升氢气,该反应转移电子的数目为______ (用含NA的代数式表示)。
(1)现有几种微粒或物质:①H、D、T;②
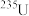 、
、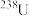 ;③
;③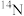 、
、 ;④
;④ 、
、 、
、 ;⑤
;⑤ 、
、 ;⑥金刚石、石墨;⑦
;⑥金刚石、石墨;⑦ 、
、 、
、 。互为同位素的是
。互为同位素的是(2)下表为元素周期表的一部分,NA代表阿伏伽德罗常数的数值,请参照元素①-⑩在表中的位置,回答下列问题:

元素⑩在周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、R、W为五种原子序数依次增大的前四周期元素。X元素的最简单氢化物是天然气的主要成分:Y和Z能形成Z2Y与Z2Y2:两种离子化合物,其中一种为常用的供氧剂;R 元素在短周期,其最高正价与最低负价的代数和为4;W元素有多种氧化物,其中一种为红色涂料的主要成分。回答下列问题:
(1)X在元素周期表中的位置是_______ ,W 元素的原子结构示意图是________ 。
(2)Z2Y的电子式为_____ ,Z2 Y2中含有的化学键类型为__________ 。
(3)元素Y和R的最简单氢化物的沸点由高到低顺序为______ (填化学式)。
(4)无机盐W2(RY4)3在T . F菌存在的酸性溶液中可实现天然气的催化除杂,其原理如图所示:
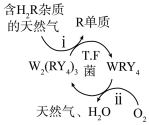
①写出过程i中发生反应的离子方程式_________ ;
②过程ii中的氧化剂是____________ ;
③有关上述过程的说法正确的是__________ (填序号)。
a WRY4是该过程的催化剂
b 该过程需要不断添加W2(RY4)3溶液
c 该过程O2间接氧化H2S
(1)X在元素周期表中的位置是
(2)Z2Y的电子式为
(3)元素Y和R的最简单氢化物的沸点由高到低顺序为
(4)无机盐W2(RY4)3在T . F菌存在的酸性溶液中可实现天然气的催化除杂,其原理如图所示:

①写出过程i中发生反应的离子方程式
②过程ii中的氧化剂是
③有关上述过程的说法正确的是
a WRY4是该过程的催化剂
b 该过程需要不断添加W2(RY4)3溶液
c 该过程O2间接氧化H2S
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图是元素周期表中的前四周期,回答下列问题:

(1)a元素的基态原子的电子排布图是图①、②中的一个。
①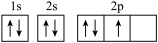 ②
② 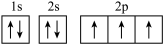
另一个电子排布图错误的原因是:它不符合_______ (填标号)。
A.构造原理 B.泡利原理 C.洪特规则
(2)b、e两种元素的第四电离能大小关系为_______ ,原因是_______ 。
(3)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为_______ (填元素符号)
(4)某元素的原子价电子排布式为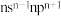 ,该基态原子核外自旋方向相同的电子最多有
,该基态原子核外自旋方向相同的电子最多有_______ 个。

(1)a元素的基态原子的电子排布图是图①、②中的一个。
①
 ②
② 
另一个电子排布图错误的原因是:它不符合
A.构造原理 B.泡利原理 C.洪特规则
(2)b、e两种元素的第四电离能大小关系为
(3)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为
(4)某元素的原子价电子排布式为
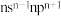 ,该基态原子核外自旋方向相同的电子最多有
,该基态原子核外自旋方向相同的电子最多有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】随着原子序数的递增,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。请回答下列问题:
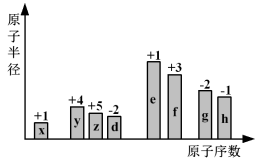
(1)g在元素周期表中的位置是_______ , e离子的结构示意图是_______ 。
(2)比较d与e常见离子的半径大的是_______ ,比较g与h的最高价氧化物的水化物的酸性强的是_______ 。(用化学式表示,下同)
(3)y与h形成的化合物的结构式是_______ ,x与z形成的化合物的电子式是_______ 。
(4)e与f的最高价氧化物的水化物之间相互反应的离子方程式是_______ 。

(1)g在元素周期表中的位置是
(2)比较d与e常见离子的半径大的是
(3)y与h形成的化合物的结构式是
(4)e与f的最高价氧化物的水化物之间相互反应的离子方程式是
您最近一年使用:0次



