周期表前四周期的元素A、B、C、D、E原子序数依次增大。基态原子A的原子轨道半充满,B的价电子层中有3个未成对电子,D的价层电子排布式为nsn-1np2n-2,C与D同族,E的最外层只有1个电子,次外层有18个电子。这5种元素形成的一种1:1型离子化合物中,由C、D所形成的阴离子呈正四面体结构、阳离子呈轴向狭长的八面体结构(如图所示)。下列说法正确的是
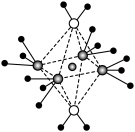
| A.5种原子中第一电离能最大的是C |
| B.A、B所形成的化合物中只含极性键 |
| C.1mol该阳离子中含有24molσ键 |
| D.B、C、D所形成的简单氢化物中,沸点最低的是D |
更新时间:2023-05-29 19:16:21
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是( )
| A | B | C | ||
| D | ||||
| A.原子半径大小比较为D>C>B>A |
| B.生成的氢化物分子间均可形成氢键 |
C.A与C形成的阴离子可能有AC 、A2C 、A2C |
| D.A、B、C、D的单质常温下均不导电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一种由W、X、Y、Z、Q五种短周期主族元素组成的离子结构如图所示,其中X、Q同主族,Y的基态原子s轨道电子数是p轨道的2倍,且W、X、Z原子序数之和为15.下列说法正确的是
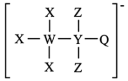
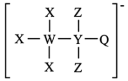
A.电负性: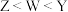 |
B.最高价氧化物对应水化物的酸性: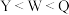 |
C.阴离子还原性: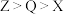 |
| D.X与Z形成的化合物沸点一定高于Y与Z形成的化合物沸点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】1919年卢瑟福在核反应中用 粒子(即氦核轰击短周期非金属
粒子(即氦核轰击短周期非金属 原子,得到核素
原子,得到核素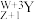 和一新的粒子M,其过程为:
和一新的粒子M,其过程为: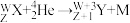 。其中元素X、Y、M的质子数之和为16,下列说法正确的是
。其中元素X、Y、M的质子数之和为16,下列说法正确的是
 粒子(即氦核轰击短周期非金属
粒子(即氦核轰击短周期非金属 原子,得到核素
原子,得到核素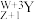 和一新的粒子M,其过程为:
和一新的粒子M,其过程为: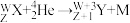 。其中元素X、Y、M的质子数之和为16,下列说法正确的是
。其中元素X、Y、M的质子数之和为16,下列说法正确的是| A.粒子M中含有1个中子 | B.最简单氢化物的还原性:X<Y |
C. 中所有原子均为8电子稳定结构 中所有原子均为8电子稳定结构 | D.X和Y只能形成两种化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3;④1s22s22p5。则下列有关比较中正确的是
| A.第一电离能:④>③>②>① | B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:④>①>③=② |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知 A、B、C、D、E 都是周期表中前四周期的元素,且原子序数依次增大,其中 A 原子核外 有三个未成对电子;A 与 B 可形成离子化合物 B3A2;C 元素是地壳中含量最高的金属元素;D 原 子核外的 M 层中有两对成对电子;E 原子核外最外层只有 1 个电子,其余各层电子均充满。以下 有关说法正确的是
| A.A 离子半径小于 B 离子半径 |
| B.B 和 C 的氯化物晶体类型相同 |
| C.C 和 D 形成的二元化合物不能通过复分解反应得到 |
| D.E 在周期表中位于第四周期 s 区 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】沸石笼作为一种载体对氮氧化物进行催化还原的原理如图所示,下列说法正确的是
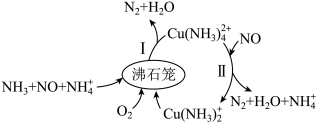

| A.沸石笼能增大气体的吸附面积,从而加快反应I的反应速率 |
| B.反应I中只有两种元素的化合价发生了变化 |
| C.反应II中氧化剂与还原剂的物质的量之比为1:1 |
| D.反应I与反应II均没有极性键与非极性键的形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1mol羟基所含电子数为10NA |
| B.1mol苯分子含碳碳双键数目为3NA |
| C.常温常压下,28g乙烯含σ键数目为6NA |
| D.常温常压下,乙烯和丙烯的混合气体共14g,含原子数为3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】“类推”是一种重要的学习方法,但有时会产生错误,下列“类推”得到的结论正确的是
| A.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| B.氢化物沸点顺序是:GeH4>SH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| C.C=C的键能小于两倍的C-C,则N=N的键能小于两倍的N-N |
D.SO 和P4都为正四面体形,SO 和P4都为正四面体形,SO 中键角为109°28′,P4中键角也为109°28′ 中键角为109°28′,P4中键角也为109°28′ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】四种短周期元素X、Y、Z、W在元素周期表中的相对位置如下表所示,Y、Z质子数之和为21,下列说法中不正确的是
| X | Y | ||
| Z | W |
| A.X、Y、Z、W均为非金属元素 | B.X、Y、W的氢化物中,Y的氢化物沸点最高 |
| C.Z的阳离子与Y的阴离子电子层结构相同 | D.W元素的简单离子半径大于Z元素的简单离子半径 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法中正确的是
①外围电子构型为nsnnpn的原子形成的化合物的种类最多; ②在硫酸铜氨溶液中加入乙醇有深蓝色晶体析出; ③H2O是一种非常稳定的化合物,这是由于H2O分子间存在氢键所致; ④P4、BF3、CH3Cl三种分子中所有原子的最外层均满足8e-稳定结构; ⑤乙醇分子中只含σ键. ⑥键角是描述分子立体结构的重要参数,键长的大小与成键原子的半径和成键数目有关,键能越大,键长越长,共价化合物越稳定
①外围电子构型为nsnnpn的原子形成的化合物的种类最多; ②在硫酸铜氨溶液中加入乙醇有深蓝色晶体析出; ③H2O是一种非常稳定的化合物,这是由于H2O分子间存在氢键所致; ④P4、BF3、CH3Cl三种分子中所有原子的最外层均满足8e-稳定结构; ⑤乙醇分子中只含σ键. ⑥键角是描述分子立体结构的重要参数,键长的大小与成键原子的半径和成键数目有关,键能越大,键长越长,共价化合物越稳定
| A.①③⑤正确 | B.③④⑥正确 | C.①②⑤正确 | D.⑤正确,其他均不正确 |
您最近一年使用:0次

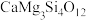 ,其组成也可写成余化物形式:
,其组成也可写成余化物形式: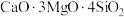 。下列说法正确的是
。下列说法正确的是 的熔点比
的熔点比 的高
的高 和
和 在催化剂表面合成氨的微观历程及能量变化的示意图如下,用
在催化剂表面合成氨的微观历程及能量变化的示意图如下,用 、
、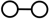 、
、 分别表示
分别表示 ,已知:
,已知: ,反应释放热量,下列说法正确的是
,反应释放热量,下列说法正确的是
 键的断裂
键的断裂

