元素周期表中锑元素的数据如图。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第___________ 周期,第___________ 族。
(2)基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(3)基态锑原子的5s轨道形状为___________ 形,该原子最外层电子占有___________ 个轨道。
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb___________ Bi;原子半径Sb___________ Bi (填“>”或“<”)。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第
(2)基态锑原子中有
(3)基态锑原子的5s轨道形状为
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb
更新时间:2023-05-06 18:16:49
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有________ 种,金属性最强的元素与氧反应生成的化合物有(填两种化合物的化学式)________ 、___________ 。
(2)属于稀有气体元素的是(填元素符号,下同)_____________ 。
(3)形成化合物种类最多的两种元素是_________ 、_________ 。
(4)推测Si、N最简单氢化物的稳定性:________ 大于________ (填化学式)。
(1)属于金属元素的有
(2)属于稀有气体元素的是(填元素符号,下同)
(3)形成化合物种类最多的两种元素是
(4)推测Si、N最简单氢化物的稳定性:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表列出了A~R 9种元素在周期表中的位置:
请回答下列问题。
(1)写出下列几种元素符号:B___________ ,D___________ ,H___________ ,R___________ 。9种元素中化学性质最不活泼的是___________ 。
(2)A与F形成的一种化合物可作供氧剂,写出该化合物作供氧剂时的反应原理:___________ 。
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___________ 。
(4)A、B、C三种元素按原子半径由大到小的顺序排列为___________ 。
(5)H元素与A元素形成化合物的化学式是___________ ,高温灼烧该化合物时,火焰呈___________ 色。
| 周期 | 族 | |||||||
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
请回答下列问题。
(1)写出下列几种元素符号:B
(2)A与F形成的一种化合物可作供氧剂,写出该化合物作供氧剂时的反应原理:
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(4)A、B、C三种元素按原子半径由大到小的顺序排列为
(5)H元素与A元素形成化合物的化学式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。下表列出了a-j 10种元素在周期表中的位置:
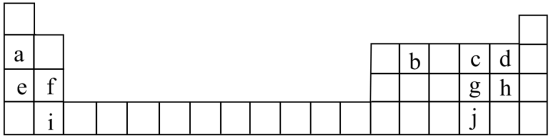
(1)元泰a的原于结构示意图为__________ 。
(2)元素b可以形成多种单质,写出其中的两种____________________ (填名称)。
(3)元素a~j中非金属性最强的是___________ (填元素符号)。
(4)若e单质着火,可用于灭火的物质是___________ (填字母)
A 自来水 B CO2. C 干沙子 D 湿抹布
(5)元素h和i形成的化合物中化学键的类型是___________ 键。h单质与NaOH溶液反应的离子方程式为____________ 。
(6)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有___________ (填字母)。
A a的金属性比e弱 B 自然界中,e的储量比a高
B a的原子半径比e大 D 基于a的电池质量轻、易携带

(1)元泰a的原于结构示意图为
(2)元素b可以形成多种单质,写出其中的两种
(3)元素a~j中非金属性最强的是
(4)若e单质着火,可用于灭火的物质是
A 自来水 B CO2. C 干沙子 D 湿抹布
(5)元素h和i形成的化合物中化学键的类型是
(6)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有
A a的金属性比e弱 B 自然界中,e的储量比a高
B a的原子半径比e大 D 基于a的电池质量轻、易携带
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求回答下列问题:
(1)基态Ti原子的核外电子排布式为___ 。
(2)Fe成为阳离子时首先失去___ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___ 。
(3)Cu2+基态核外电子排布式为___ 。
(4)Zn原子核外电子排布式为___ 。
(5)氮原子价层电子的轨道表达式(电子排布图)为__ 。
(6)Co基态原子核外电子排布式为___ 。
(1)基态Ti原子的核外电子排布式为
(2)Fe成为阳离子时首先失去
(3)Cu2+基态核外电子排布式为
(4)Zn原子核外电子排布式为
(5)氮原子价层电子的轨道表达式(电子排布图)为
(6)Co基态原子核外电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.回答下列问题:
(1)核外电子排布时遵循一定的原则:在一个原子轨道里,最多只能容纳2个电子,它们的自旋相反,这个原理称为泡利不相容原理;对于基态原子,核外电子在能量相同的原子轨道上排布时,将尽可能分占不同的原子轨道并且自旋状态相同称为洪特规则。依据以上原则,下列原子或离子的核外电子排布正确的是_______ ,违反能量最低原理的是_______ ,违反洪特规则的是_______ ,违反泡利不相容原理的是_______ 。
①Ca2+:1s22s22p63s23p6 ②F-:1s22s22p5 ③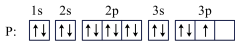 ④Cr:1s22s22p63s23p63d44s2 ⑤K:1s22s22p63s23p63d1 ⑥Mg:1s22s22p63s2 ⑦C:
④Cr:1s22s22p63s23p63d44s2 ⑤K:1s22s22p63s23p63d1 ⑥Mg:1s22s22p63s2 ⑦C:
Ⅱ.2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(2)写出铜的基态原子的电子排布式:______ 。
(3)Fe3+的电子排布式为______ 。
(4)p电子的原子轨道呈______ 形。
(1)核外电子排布时遵循一定的原则:在一个原子轨道里,最多只能容纳2个电子,它们的自旋相反,这个原理称为泡利不相容原理;对于基态原子,核外电子在能量相同的原子轨道上排布时,将尽可能分占不同的原子轨道并且自旋状态相同称为洪特规则。依据以上原则,下列原子或离子的核外电子排布正确的是
①Ca2+:1s22s22p63s23p6 ②F-:1s22s22p5 ③
 ④Cr:1s22s22p63s23p63d44s2 ⑤K:1s22s22p63s23p63d1 ⑥Mg:1s22s22p63s2 ⑦C:
④Cr:1s22s22p63s23p63d44s2 ⑤K:1s22s22p63s23p63d1 ⑥Mg:1s22s22p63s2 ⑦C:
Ⅱ.2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(2)写出铜的基态原子的电子排布式:
(3)Fe3+的电子排布式为
(4)p电子的原子轨道呈
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】a、b、c、d四种短周期元素,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族。请完成下列空白:
(1)a和b形成的共价化合物,分子的空间结构呈三角锥形,该分子的中心原子的杂化轨道类型为___________ ;a和c形成的共价化合物,分子中既含有极性共价键,又含有非极性共价键的化合物是___________ (填化学式)。
(2)这些元素可以形成哪些含氧酸_______ ?分析每种含氧酸酸根离子的空间结构和中心原子的杂化轨道类型___________ 。
(1)a和b形成的共价化合物,分子的空间结构呈三角锥形,该分子的中心原子的杂化轨道类型为
(2)这些元素可以形成哪些含氧酸
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】电子排布式和电子排布图的书写。
(1)[2020·全国卷Ⅱ,35(1)]基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
(2)[2019·全国卷Ⅱ,35(2)] 成为阳离子时首先失去
成为阳离子时首先失去_______ 轨道电子, 的价层电子排布式
的价层电子排布式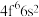 ,
, 价层电子排布式为
价层电子排布式为_______ 。
(3)[2019·全国卷Ⅰ,35(1)]下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填字母)。
(4)[2018·全国卷Ⅱ,35(1)节选]基态 原子价层电子的电子排布图(轨道表达式)为
原子价层电子的电子排布图(轨道表达式)为_______ 。
(5)[2021·天津,13(1)]基态 原子的价层电子排布式为
原子的价层电子排布式为_______ 。
(1)[2020·全国卷Ⅱ,35(1)]基态
 原子的核外电子排布式为
原子的核外电子排布式为(2)[2019·全国卷Ⅱ,35(2)]
 成为阳离子时首先失去
成为阳离子时首先失去 的价层电子排布式
的价层电子排布式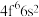 ,
, 价层电子排布式为
价层电子排布式为(3)[2019·全国卷Ⅰ,35(1)]下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填字母)。
A. | B. | C. | D. |
 原子价层电子的电子排布图(轨道表达式)为
原子价层电子的电子排布图(轨道表达式)为(5)[2021·天津,13(1)]基态
 原子的价层电子排布式为
原子的价层电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】现有A、B、C、D、E五种元素,均为前四周期元素、它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)写出下列元素的元素符号:B:___________ C:___________ D:___________
(2)用元素符号表示A2B2的电子式为___________ 。
(3)E元素在元素周期表的位置为:___________ ,属于___________ 区,它有___________ 个能层。
(4)D原子核外电子排布式为___________ , 离子价层电子轨道表示式为
离子价层电子轨道表示式为___________ , 价层电子排布式的特点是
价层电子排布式的特点是___________ 。
(5)检验某溶液中是否含有 ,通常所用的试剂是
,通常所用的试剂是___________ 和___________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| C元素基态原子核外有17个不同运动状态的电子 |
| D元素位于元素周期表中的第八列,在地壳中的含量居前四位 |
| E元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)用元素符号表示A2B2的电子式为
(3)E元素在元素周期表的位置为:
(4)D原子核外电子排布式为
 离子价层电子轨道表示式为
离子价层电子轨道表示式为 价层电子排布式的特点是
价层电子排布式的特点是(5)检验某溶液中是否含有
 ,通常所用的试剂是
,通常所用的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH2=CH2)与四氟乙烯(CF2=CF2)的共聚物(ETFE)制成。回答下列问题:
(1)基态F原子的价电子轨道表示式为___________ 。
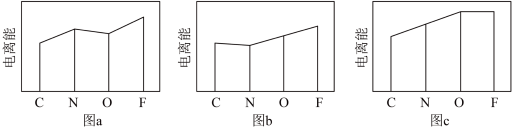
(2)图a、b、c分别表示 C、N、O和F的逐级电离能 I变化趋势(纵坐标的标度不同)。第一电离能的变化图是___________ (填标号)。
(3)CF2=CF2和 ETFE 分子中 C 的杂化轨道类型分别为___________ 和___________ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因___________ 。
(1)基态F原子的价电子轨道表示式为
(2)图a、b、c分别表示 C、N、O和F的逐级电离能 I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(3)CF2=CF2和 ETFE 分子中 C 的杂化轨道类型分别为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。
下面是某些短周期元素的x值:
(1)通过分析x值变化规律,确定Mg的x值范围:____ <x(Mg)< _____ 。
(2)推测x值与原子半径的关系是____ ;根据短周期元素的x值变化特点,体现了元素性质的________ 变化规律。
(3)某有机化合物结构式为 ,其中S—N中,你认为共用电子对偏向谁?
,其中S—N中,你认为共用电子对偏向谁?__ (写原子名称)。
(4)经验规律告诉我们:当成键的两原子相应元素的差值(Δx),当Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键类型是______ 。
(5)预测元素周期表中,x值最小的元素位置:_________ (放射性元素除外)。
下面是某些短周期元素的x值:
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| x值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(2)推测x值与原子半径的关系是
(3)某有机化合物结构式为
 ,其中S—N中,你认为共用电子对偏向谁?
,其中S—N中,你认为共用电子对偏向谁?(4)经验规律告诉我们:当成键的两原子相应元素的差值(Δx),当Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键类型是
(5)预测元素周期表中,x值最小的元素位置:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有_______ 种。
(2)O、F、Cl电负性由大到小的顺序为________ ;OF2分子的空间构型为_______ ;OF2的熔、沸点_______ (填“高于”或“低于”)Cl2O,原因是________ 。
(1)基态F原子核外电子的运动状态有
(2)O、F、Cl电负性由大到小的顺序为
您最近一年使用:0次




