下表列出了A~R 9种元素在周期表中的位置:
请回答下列问题。
(1)写出下列几种元素符号:B___________ ,D___________ ,H___________ ,R___________ 。9种元素中化学性质最不活泼的是___________ 。
(2)A与F形成的一种化合物可作供氧剂,写出该化合物作供氧剂时的反应原理:___________ 。
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___________ 。
(4)A、B、C三种元素按原子半径由大到小的顺序排列为___________ 。
(5)H元素与A元素形成化合物的化学式是___________ ,高温灼烧该化合物时,火焰呈___________ 色。
| 周期 | 族 | |||||||
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
请回答下列问题。
(1)写出下列几种元素符号:B
(2)A与F形成的一种化合物可作供氧剂,写出该化合物作供氧剂时的反应原理:
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(4)A、B、C三种元素按原子半径由大到小的顺序排列为
(5)H元素与A元素形成化合物的化学式是
更新时间:2021-05-07 22:12:30
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】2022年央视春晚的节目《只此青绿》,提到了颜料石绿{铜绿,又名孔雀石,主要成分是碱式碳酸铜[Cu2(OH)2CO3]}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:

(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:_______ 。
(2)将绿豆大小的金属钠投入盛有A溶液的烧杯中,溶液中出现蓝色絮状沉淀,振荡摇匀即为悬浊液,悬浊液与溶液的本质区别是_______ 。若投入的钠块比较大,可能会出现黑色固体,原因是_______ 。
(3)A、B在无色火焰上灼烧时,其焰色_______ (填“相同”或“不相同”),该原理是_______ (填“物理”或“化学”)变化。
(4)完成步骤②和③可选用的试剂分别为_______ 、_______ 。(填标号)
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
写出所选试剂的溶质在水溶液里的电离方程式:_______ 、_______ 。

(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)将绿豆大小的金属钠投入盛有A溶液的烧杯中,溶液中出现蓝色絮状沉淀,振荡摇匀即为悬浊液,悬浊液与溶液的本质区别是
(3)A、B在无色火焰上灼烧时,其焰色
(4)完成步骤②和③可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
写出所选试剂的溶质在水溶液里的电离方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】因在航空、核能、电池等高技术领域的重要作用——锂被称为“21世纪的能源金属”。
(1)氢化锂(LiH)中阴离子半径大于阳离子半径,其原因是___________ 。
(2)下列关于碱金属元素及其单质的叙述中,正确的是___________ (填字母)。
(3)宁德时代推出的钠离子电池,比磷酸亚铁锂电池成本更低,请画出钠离子(Na+)结构示意图___________ 。
(4)磷酸亚铁锂(LiFePO4)是新型锂离子电池的电极材料,P位于元素周期表的___________ 周期,第___________ 族,LiFePO4含有锂、铁两种金属元素,它们焰色试验的颜色分别是___________ (填序号)。
A.紫红色、无焰色现象 B.黄色、无焰色现象
C.黄色、紫色 D.洋红色、黄绿色
(1)氢化锂(LiH)中阴离子半径大于阳离子半径,其原因是
(2)下列关于碱金属元素及其单质的叙述中,正确的是___________ (填字母)。
| A.金属钠着火,要用泡沫灭火剂扑灭 |
| B.水溶液中阳离子氧化性:Li+>Na+>K+>Rb+ |
| C.单质熔点:Li<Na<K<Rb |
| D.与水反应的能力:Na<K |
(4)磷酸亚铁锂(LiFePO4)是新型锂离子电池的电极材料,P位于元素周期表的
A.紫红色、无焰色现象 B.黄色、无焰色现象
C.黄色、紫色 D.洋红色、黄绿色
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】研究物质会涉及物质的组成、分类、性质等方面。
(1)根据物质的性质分类, 属于
属于___________ ,检验其组成中所含阳离子的方法是___________ ,实验现象为___________ 。
(2)将酚酞滴入 溶液中,观察到溶液呈红色,说明
溶液中,观察到溶液呈红色,说明 溶液呈
溶液呈___________ 性。用胶头滴管将盐酸逐滴滴入含有酚酞的 溶液中,刚开始可观察到溶液红色褪去,一段时间后有黄绿色气体生成。该实验过程中,溶液红色褪去的原因可能有两种:①
溶液中,刚开始可观察到溶液红色褪去,一段时间后有黄绿色气体生成。该实验过程中,溶液红色褪去的原因可能有两种:①___________ ;②___________ 。请设计实验证明是①或②:___________ 。实验过程中最终生成黄绿色气体的离子反应方程式为___________ 。
(1)根据物质的性质分类,
 属于
属于(2)将酚酞滴入
 溶液中,观察到溶液呈红色,说明
溶液中,观察到溶液呈红色,说明 溶液呈
溶液呈 溶液中,刚开始可观察到溶液红色褪去,一段时间后有黄绿色气体生成。该实验过程中,溶液红色褪去的原因可能有两种:①
溶液中,刚开始可观察到溶液红色褪去,一段时间后有黄绿色气体生成。该实验过程中,溶液红色褪去的原因可能有两种:①
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:

(1)溶液Ⅰ中的溶质为_________ (填化学式,下同),溶液Ⅱ中的溶质为__________ 。
(2)上述第③步反应中,生成沉淀的离子方程式为____________ 。
(3)该合金中铝的含量为__________ 。

(1)溶液Ⅰ中的溶质为
(2)上述第③步反应中,生成沉淀的离子方程式为
(3)该合金中铝的含量为
您最近一年使用:0次
填空题
|
较易
(0.85)
真题
解题方法
【推荐2】胃舒平主要成分是氢氧化铝,同时含有三硅酸镁( )等化合物。
)等化合物。
(1)三硅酸镁的氧化物形式为_______ ,某元素与镁元素不同周期但在相邻一族,且性质和镁元素十分相似,该元素原子核外电子排布式为_______ 。
(2)铝元素的原子核外共有________ 种不同运动状态的电子、_______ 种不同能级的电子。
(3)某元素与铝元素同周期且原子半径比镁原子半径大,该元素离子半径比铝离子半径____ (填“大”或“小”),该元素与铝元素的最高价氧化物的水化物之间发生反应的离子方程式为:______
(4) 、Mg0和
、Mg0和 都可以制耐火材料, 其原因是
都可以制耐火材料, 其原因是______ 。
a. 、Mg0和
、Mg0和 都不溶于水
都不溶于水
b. 、Mg0和
、Mg0和 都是白色固体
都是白色固体
c. 、Mg0和
、Mg0和 都是氧化物
都是氧化物
d. 、Mg0和
、Mg0和 都有很高的熔点
都有很高的熔点
 )等化合物。
)等化合物。(1)三硅酸镁的氧化物形式为
(2)铝元素的原子核外共有
(3)某元素与铝元素同周期且原子半径比镁原子半径大,该元素离子半径比铝离子半径
(4)
 、Mg0和
、Mg0和 都可以制耐火材料, 其原因是
都可以制耐火材料, 其原因是a.
 、Mg0和
、Mg0和 都不溶于水
都不溶于水b.
 、Mg0和
、Mg0和 都是白色固体
都是白色固体 c.
 、Mg0和
、Mg0和 都是氧化物
都是氧化物 d.
 、Mg0和
、Mg0和 都有很高的熔点
都有很高的熔点
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空。
(1)已知甲、乙、丙三种物质分别由H、C、Na、O、Cl、Fe、Al元素中的一种或几种组成。
①若甲物质为碱性氧化物,则甲的化学式为_______ (写2种)。
②若乙物质可作为呼吸面具中氧气的来源,则乙物质的电子式_______ ,其供氧原理是_______ (用化学方程式表示)。
③丙物质是两性氢氧化物,它能与强碱溶液反应,则反应的离子方程式为_______ 。
(2)在横线上填入合适的化学式:_______ +2H+=CO2↑+H2O+Ba2+;并判断其所属化合物类型_______ (填写“离子化合物”或“共价化合物”)。
(3)写出氯气与水反应的化学方程式,并用双线桥法标出电于转移的方向和数目:_______ 。
(4)酸性高锰酸钾溶液具有强氧化性。某反应中参加反应的离子为MnO 、H+和一种未知离子,产物为Fe3+、Mn2+和H2O,该反应的离子方程式为
、H+和一种未知离子,产物为Fe3+、Mn2+和H2O,该反应的离子方程式为_______ 。
(1)已知甲、乙、丙三种物质分别由H、C、Na、O、Cl、Fe、Al元素中的一种或几种组成。
①若甲物质为碱性氧化物,则甲的化学式为
②若乙物质可作为呼吸面具中氧气的来源,则乙物质的电子式
③丙物质是两性氢氧化物,它能与强碱溶液反应,则反应的离子方程式为
(2)在横线上填入合适的化学式:
(3)写出氯气与水反应的化学方程式,并用双线桥法标出电于转移的方向和数目:
(4)酸性高锰酸钾溶液具有强氧化性。某反应中参加反应的离子为MnO
 、H+和一种未知离子,产物为Fe3+、Mn2+和H2O,该反应的离子方程式为
、H+和一种未知离子,产物为Fe3+、Mn2+和H2O,该反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】如图是元素周期表的一部分。
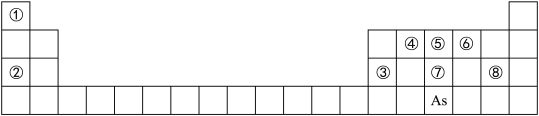
(1)②、⑥、⑧的离子半径由大到小的顺序为____________ (用离子符号表示)。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_____ (用化学式表示)。
(3)As的原子结构示意图为_________ 其氢化物的化学式为__________ ;
(4)Y由②、⑥、⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As 可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为__________ ,当消耗l mol还原剂时,电子转移了_____ mol。

(1)②、⑥、⑧的离子半径由大到小的顺序为
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)As的原子结构示意图为
(4)Y由②、⑥、⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As 可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,根据表中给出的10种元素,按要求使用化学用语填空作答:
(1)地壳中含量最高的元素是_______ (填元素符号,下同);金属性最强的元素是_______ ;单质的化学性质最不活泼的元素是_______ ;气体单质有颜色的元素_______ ;可运输浓硫酸的金属元素是_______ 。
(2)最高价氧化物对应水化物酸性最强的是_______ ,碱性最强的是_______ (填化合物化学式);最高价氧化物不溶于水,但既溶于稀硫酸又溶于氢氧化钠溶液的是_______ (填化合物化学式);
(3)第三周期中两种金属元素的最高价氧化物对应的水化物相互反应的化学方程式为:_______ ,氢氧化铝治疗胃酸分泌过多的离子方程式:_______ 。
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | H | |||||||
| 2 | C | N | O | Ne | ||||
| 3 | Na | Al | P | S | Cl |
(2)最高价氧化物对应水化物酸性最强的是
(3)第三周期中两种金属元素的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为___________________ ;
(2)②、③两元素的原子半径较大的是______________ (填元素符号);
(3)④和⑤两种元素的金属性较强的是_____________ (填元素符号);
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式___________________ 。
 | IA | 0 | |||||||
| 1 | ① | II A | III A | IV A | V A | VI A | VIIA | ||
| 2 | ② | ③ | |||||||
| 3 | ④ | ⑤ | ⑥ | ||||||
请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为
(2)②、③两元素的原子半径较大的是
(3)④和⑤两种元素的金属性较强的是
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】安全气囊在汽车部件中非常重要,它的工作原理是汽车碰撞时传感器产生的电流触发气体发生如下反应:
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为___________ ;某元素的最外层电子数是电子层数的3倍,则其简单离子的电子式为___________ ,能量最高的电子为___________ 层上的电子。反应中涉及的主族元素的简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是___________ ,其水溶液显___________ 性(填“酸”、“碱”或“中”),原因是___________ (用离子方程式表示)。
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有___________ 个氮原子(保留三个有效数字);已知获得上述N2需要NaN3130g,反应生成N2的产率是___________ %(产率= ×100%)
×100%)
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有
 ×100%)
×100%)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】分子筛是一类具有规整孔道结构的多孔材料,能够选择性吸附空间结构各异和不同尺寸的分子,在化学工业中有着广泛的应用。近年来,我国科学家在分子筛研究领域不断取得新的突破。这些研究中涉及的部分元素在周期表中位置如下:
(1)近期我国科学家制备了一种无缺陷的分子筛膜,可高效分离CH4与CO2两种气体。下列有关分子空间结构的描述正确的是_______
(2)传统的分子筛主要含有O、Na、Al和Si元素,通过调控这 4种元素的比例,可获得不同性能的分子筛产品。这4种元素描述中正确的是_______ 。
(3)通过将分子筛中的元素Na替换为K或Ca,可改变分子筛的孔径大小。这3种元素中说法正确的是_______
(4)N2常用于分子筛的孔结构测试,H、O和N元素可形成多种物质。下列说法正确的是_______
(5)某些分子筛可以选择性吸附Ar。Ar位于元素周期表的_______
| 周期 | 族 | ||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | H | ||||||
| 2 | C | N | O | ||||
| 3 | Na | Al | Si | ||||
| 4 | K | Ca | |||||
| A.CH4是平面结构 | B.CO2是V形结构 |
| C.CH4是正四面体结构 | D.CO2是直线形结构 |
| A.非金属性最强的是O |
| B.核外电子数最少的是 Na |
| C.金属性最强的是Al |
| D.原子半径最大的是Si |
| A.仅Na可与Cl2反应 |
| B.K的单质与水的反应最剧烈 |
| C.Na的氧化物与水的反应均为化合反应 |
| D.Ca的最高价氧化物的水化物碱性最强 |
| A.N2中含有共价三键 |
| B.NO可由NH3催化氧化得到 |
| C.NH3的水溶液呈碱性 |
| D.稀HNO3与Cu反应产生H2 |
| A.第二周期 | B.Ⅷ族 | C.第三周期 | D.0族 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空:
(1)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子半径由大到小的顺序是__________________ 。
(2)A+、Bˉ、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:___________ ,____________ 。
(3)已知: N2(g)+
N2(g)+ H2(g)=N(g)+3H(g)ΔH1=+akJ·mol-1
H2(g)=N(g)+3H(g)ΔH1=+akJ·mol-1
N(g)+3H(g)=NH3(g)ΔH2=-bkJ·mol-1
NH3(g)=NH3(l)ΔH3=-ckJ·mol-1
写出N2(g)和H2(g)反应生成液氨的热化学方程式____________________________ 。
(4)下列原子: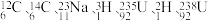 中共有
中共有____ 种元素,_____ 种核素。
(1)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子半径由大到小的顺序是
(2)A+、Bˉ、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:(3)已知:
 N2(g)+
N2(g)+ H2(g)=N(g)+3H(g)ΔH1=+akJ·mol-1
H2(g)=N(g)+3H(g)ΔH1=+akJ·mol-1N(g)+3H(g)=NH3(g)ΔH2=-bkJ·mol-1
NH3(g)=NH3(l)ΔH3=-ckJ·mol-1
写出N2(g)和H2(g)反应生成液氨的热化学方程式
(4)下列原子:
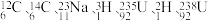 中共有
中共有
您最近一年使用:0次



