如图是元素周期表的一部分,图中所列字母分别代表某一化学元素。
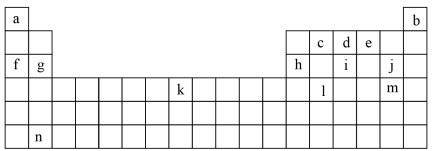
试回答下列问题:
(1)基态原子j核外电子总共有___________ 种运动状态,电子占据的能量最高轨道的形状为___________ 。
(2)e与a反应的产物的分子空间构型为___________ ,其分子的中心原子杂化方式为___________ ,该分子是___________ (填“极性”或“非极性”)分子。
(3)f、g和h的第一电离能数值由大到小的顺序为:___________ (用元素符号作答)。
(4)请画出k基态原子价电子轨道表示式为________ ,该元素属于________ 区元素。
(5) 与k两元素的部分电离能数据列于下表:
与k两元素的部分电离能数据列于下表:
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,对此,你的解释是
再失去一个电子难,对此,你的解释是___________ 。

试回答下列问题:
(1)基态原子j核外电子总共有
(2)e与a反应的产物的分子空间构型为
(3)f、g和h的第一电离能数值由大到小的顺序为:
(4)请画出k基态原子价电子轨道表示式为
(5)
 与k两元素的部分电离能数据列于下表:
与k两元素的部分电离能数据列于下表:| 元素 | Mn | K | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,对此,你的解释是
再失去一个电子难,对此,你的解释是
更新时间:2023-06-08 23:42:49
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】氧、硫形成的化合物种类繁多,日常生活中应用广泛。如硫代硫酸钠(Na2S2O3)可作为照相业的定影剂,反应的化学方程式如下:AgBr+2Na2S2O3===Na3[Ag(S2O3)2]+NaBr。回答下列问题:
(1)基态S的价电子排布图为____________ 。
(2)下列关于物质结构与性质的说法,正确的是________ 。
A.玻尔原子结构模型能够成功地解释各种原子光谱
B.Br、S、O三种元素的电负性顺序为 O>Br>S
C.Na的第一电离能小于 Mg,但其第二电离能却远大于 Mg
D.水分子间存在氢键,故H2O的熔沸点及稳定性均大于H2S
(3)依据VSEPR理论推测 的空间构型为
的空间构型为______ ,中心原子S的杂化方式为________ ,[Ag(S2O3)2]3-中存在的化学键有________ (填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键
(4)第一电子亲和能(E1)是指元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量(单位为kJ·mol-1),电子亲和能越大,该元素原子越易得电子。已知第三周期部分元素第一电子亲和能如下表:
表中元素的E1自左而右呈增大趋势,试分析P元素呈现异常的原因___________ 。
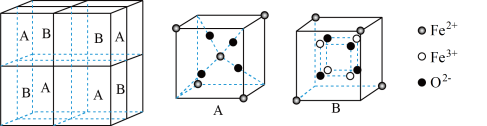
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B组成。则该氧化物的化学式为_____ ,已知该晶体的晶胞参数为a nm,阿伏加 德罗常数的值为NA,则密度ρ为______ g·cm-3(用含a和NA的代数式表示)。
(1)基态S的价电子排布图为
(2)下列关于物质结构与性质的说法,正确的是
A.玻尔原子结构模型能够成功地解释各种原子光谱
B.Br、S、O三种元素的电负性顺序为 O>Br>S
C.Na的第一电离能小于 Mg,但其第二电离能却远大于 Mg
D.水分子间存在氢键,故H2O的熔沸点及稳定性均大于H2S
(3)依据VSEPR理论推测
 的空间构型为
的空间构型为A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键
(4)第一电子亲和能(E1)是指元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量(单位为kJ·mol-1),电子亲和能越大,该元素原子越易得电子。已知第三周期部分元素第一电子亲和能如下表:
| 元素 | Al | Si | P | S | Cl |
| E1/(kJ·mol-1) | 42.5 | 134 | 72.0 | 200 | 349 |
表中元素的E1自左而右呈增大趋势,试分析P元素呈现异常的原因
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B组成。则该氧化物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】已知:A、B、C、D、E、F六种元素核电荷数依次增大,属于周期表中前四周期的元素。其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为__________ 。(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点___________ (填“高”或“低”),理由是______________ 。
(3)E的最高价氧化物分子的空间构型是__________ 。
(4)F的核外电子排布式是____________________ ,F的高价离子与A的简单氢化物形成的配离子的化学式为_______________ 。
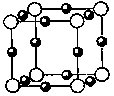
(5)A、F形成某种化合物的晶胞结构如图所示,则其化学式为_________ 。(黑色球表示F原子)
(6)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料。其晶体中所含的化学键类型为__________ 。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点比D的氯化物的熔点
(3)E的最高价氧化物分子的空间构型是
(4)F的核外电子排布式是
(5)A、F形成某种化合物的晶胞结构如图所示,则其化学式为

(6)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料。其晶体中所含的化学键类型为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】I.铬单质硬度大,耐腐蚀,是重要的合金材料。
(1)基态铬原子的价电子轨道表示式为_______ ;CrO2Cl2常温下为深红色液体,能与CCl4互溶,据此判断CrO2Cl2的晶体类型属于_______ 。
(2)配合物CrCl3·6H2O的配位数为6,它有三种不同组成、不同颜色的固体,其中一种为浅绿色固体,该固体与足量硝酸银溶液反应时,0.5mol固体可生成1mol氯化银沉淀,则这种浅绿色固体的配体个数比(Cl-:H2O)为_______ 。
II.砷化镓为第三代半导体材料,晶胞结构如图所示:

(3)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的化学方程式为_______ 。
(4)AsH3分子的立体构型为_______ ,其中As原子的杂化方式是_______ 。1个(CH3)3Ga分子中含有_______ 个σ键,砷的第一电离能_______ (填“>”或“<”)镓的第一电离能。
(5)砷化镓晶体中砷和镓的最近原子核间距为a nm,砷化镓的摩尔质量为bg·mol-1,阿伏伽德罗常数值为NA,则砷化镓晶体的密度表达式是_______ g·cm-3.
(1)基态铬原子的价电子轨道表示式为
(2)配合物CrCl3·6H2O的配位数为6,它有三种不同组成、不同颜色的固体,其中一种为浅绿色固体,该固体与足量硝酸银溶液反应时,0.5mol固体可生成1mol氯化银沉淀,则这种浅绿色固体的配体个数比(Cl-:H2O)为
II.砷化镓为第三代半导体材料,晶胞结构如图所示:

(3)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的化学方程式为
(4)AsH3分子的立体构型为
(5)砷化镓晶体中砷和镓的最近原子核间距为a nm,砷化镓的摩尔质量为bg·mol-1,阿伏伽德罗常数值为NA,则砷化镓晶体的密度表达式是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】现有五种元素,其中A、B、C、D、E为原子序数依次增大,且原子序数都不超过36.请根据下列相关信息,回答问题。
(1)请把B以及B同周期且原子序数比B小的原子按第一电离能从大到小的顺序排列:_______ (用相应的元素符号表示)。A、D两种元素中,电负性A_______ D(填“>”或“<”)
(2)基态B原子的价电子排布图为_______ ,占据最高能级的电子云轮廓图形状为_______ 。
(3)C的最高价含氧酸根离子的空间构型为_______ ,中心原子杂化轨道类型为_______ 。
(4)下图是E与镍形成的合金的立方晶胞结构,其中原子A的坐标参数为(0,1,0)。

①原子B的坐标参数为_______
②)若该晶体密度为 ,则E与镍原子间最短距离为
,则E与镍原子间最短距离为_______ pm(用含d和NA的式子表示)
(5)Ni属于_______ 区的元素,元素E与镍的第二电离能分别为: ,
, ,从原子结构知识解释
,从原子结构知识解释 的原因是
的原因是_______ 。
| A | 基态原子最外层电子数是次外层的三倍 |
| B | 基态原子核外有13种不同运动状态的电子 |
| C | 与B同一周期,原子中未成对电子数是同周期中最多 |
| D |  的核外电子排布与氩原子相同 的核外电子排布与氩原子相同 |
| E | 是ds区原子序数最小的元素 |
(2)基态B原子的价电子排布图为
(3)C的最高价含氧酸根离子的空间构型为
(4)下图是E与镍形成的合金的立方晶胞结构,其中原子A的坐标参数为(0,1,0)。

①原子B的坐标参数为
②)若该晶体密度为
 ,则E与镍原子间最短距离为
,则E与镍原子间最短距离为(5)Ni属于
 ,
, ,从原子结构知识解释
,从原子结构知识解释 的原因是
的原因是
您最近一年使用:0次
【推荐2】氟及其化合物用途非常广泛。回答下列问题:
(1)基态F原子价层电子的轨道表达式为____ ,其核外电子中占据能量最高的能级的电子云轮廓图为____ 。
(2)[H2F]+[SbF6]-(氟酸锑)是一种超强酸,其中[H2F]+离子的空间构型为____ ,写出一种与[H2F]+具有相同空间构型和键合形式的微粒____ 。
(3)H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序____ (填元素符号),BF 中B原子的杂化方式为
中B原子的杂化方式为____ 。
(4)SF6被广泛用作高压电气设备绝缘介质。SF6是一种共价化合物,可通过类似于Born—Haber循环能量构建能量图(见图a)计算相联系的键能。则S—F的键能为____ kJ·mol-1。

(5)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
①CuF比CuCl熔点高的原因是____ 。
②已知NA为阿伏加德罗常数。CuF的晶胞结构如“图b”。则CuF的晶胞参数a=____ nm(列出计算式)。

(1)基态F原子价层电子的轨道表达式为
(2)[H2F]+[SbF6]-(氟酸锑)是一种超强酸,其中[H2F]+离子的空间构型为
(3)H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序
 中B原子的杂化方式为
中B原子的杂化方式为(4)SF6被广泛用作高压电气设备绝缘介质。SF6是一种共价化合物,可通过类似于Born—Haber循环能量构建能量图(见图a)计算相联系的键能。则S—F的键能为

(5)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
①CuF比CuCl熔点高的原因是
②已知NA为阿伏加德罗常数。CuF的晶胞结构如“图b”。则CuF的晶胞参数a=

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】近年来,科学家研究的以复合过渡金属镍的氢氧化物为催化剂、三乙醇胺为电子给体以及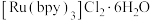 为光敏剂的催化体系,在可见光驱动下可高效催化还原
为光敏剂的催化体系,在可见光驱动下可高效催化还原 。
。
(1)下列有关Ni原子的叙述正确的是___________(填标号)。
(2)三乙醇胺的制备:3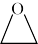 +NH3
+NH3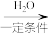 N(CH2CH2OH)3
N(CH2CH2OH)3
①三乙醇胺中所含的元素(除H元素外),第一电离能由小到大的顺序为___________ 。
②下列关于 和
和 的叙述正确的是
的叙述正确的是___________ 。
A.中心原子的价层电子对数相同
B.中心原子的杂化方式不同
C.分子的VSEPR模型相同
D. 分子的键角比
分子的键角比 分子的键角大
分子的键角大
(3)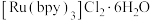 中配体bpy分子的结构简式为
中配体bpy分子的结构简式为 ,分子中N原子的杂化类型为
,分子中N原子的杂化类型为___________ ,则1mol配体bpy分子中含有σ键的数目为___________ 。与bpy分子有相似结构的单环分子吡啶的结构简式为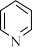 ,吡啶分子中的大
,吡啶分子中的大 键可表示为
键可表示为___________ (用 的形式表示,m表示原子数,n表示电子数)。
的形式表示,m表示原子数,n表示电子数)。
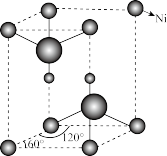
(4)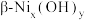 的晶胞结构如图(氧、氢原子均位于晶胞内部)所示。已知晶胞的底边长为apm,高为cpm,阿伏加德罗常数的值为NA,则该晶胞的密度为
的晶胞结构如图(氧、氢原子均位于晶胞内部)所示。已知晶胞的底边长为apm,高为cpm,阿伏加德罗常数的值为NA,则该晶胞的密度为___________ g/cm3(列出表达式)。
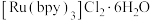 为光敏剂的催化体系,在可见光驱动下可高效催化还原
为光敏剂的催化体系,在可见光驱动下可高效催化还原 。
。(1)下列有关Ni原子的叙述正确的是___________(填标号)。
| A.第一电离能比钙的大 |
B.基态Ni原子的核外价电子排布式为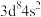 |
C.基态Ni原子形成基态 时,先失去3d轨道上的电子 时,先失去3d轨道上的电子 |
| D.基态Co原子第五电离能比基态Ni原子第五电离能大 |
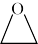 +NH3
+NH3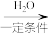 N(CH2CH2OH)3
N(CH2CH2OH)3①三乙醇胺中所含的元素(除H元素外),第一电离能由小到大的顺序为
②下列关于
 和
和 的叙述正确的是
的叙述正确的是A.中心原子的价层电子对数相同
B.中心原子的杂化方式不同
C.分子的VSEPR模型相同
D.
 分子的键角比
分子的键角比 分子的键角大
分子的键角大(3)
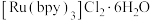 中配体bpy分子的结构简式为
中配体bpy分子的结构简式为 ,分子中N原子的杂化类型为
,分子中N原子的杂化类型为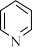 ,吡啶分子中的大
,吡啶分子中的大 键可表示为
键可表示为 的形式表示,m表示原子数,n表示电子数)。
的形式表示,m表示原子数,n表示电子数)。(4)
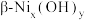 的晶胞结构如图(氧、氢原子均位于晶胞内部)所示。已知晶胞的底边长为apm,高为cpm,阿伏加德罗常数的值为NA,则该晶胞的密度为
的晶胞结构如图(氧、氢原子均位于晶胞内部)所示。已知晶胞的底边长为apm,高为cpm,阿伏加德罗常数的值为NA,则该晶胞的密度为
您最近一年使用:0次



