按要求回答下列问题:
(1)写出O的电子排布式:___________
(2)写出P的价层电子排布式:___________
(3)写出Cu的简化电子排布式:___________
(4)写出基态Fe2+的价电子排布图:___________
(1)写出O的电子排布式:
(2)写出P的价层电子排布式:
(3)写出Cu的简化电子排布式:
(4)写出基态Fe2+的价电子排布图:
更新时间:2023-05-11 15:34:44
|
相似题推荐
【推荐1】a,b,c,d为四种由短周期元素构成的中性粒子,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为______________ 。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为________ 。人一旦吸入b气体后,就易引起中毒,是因为__________ 而中毒。
(3)c是双核单质,写出其电子式____________ 。c分子中所含共价键的类型为_______ (填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是________________________ 。
(4)d是四核化合物,其结构式为______________ ;d分子内所含共价键有________ 个σ键,________ 个π键;σ键与π键的强度大小关系为σ___ π(填“>”、“<”或“=”),原因是:__________ 。
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为
(2)b是双核化合物,常温下为无色无味气体。b的化学式为
(3)c是双核单质,写出其电子式
(4)d是四核化合物,其结构式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】锰是国家紧缺战略矿产资源,广泛用于新能源、新材料等战略新兴产业,贵州地矿局研发的“气液喷溢沉积型锰矿”的找矿勘查关键技术体系,荣获贵州省2022年度十大科技创新成果。黔东地区集中分布的富锰矿床资源主体是菱锰矿( )。工业上可用菱锰矿生产锰的一种配合物
)。工业上可用菱锰矿生产锰的一种配合物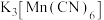 ,其主要应用于制药、电镀、造纸、钢铁生产。
,其主要应用于制药、电镀、造纸、钢铁生产。
(1)Mn元素在周期表中的位置为_____ ,基态Mn原子价电子排布式为_____ ,基态N原子核外电子空间运动状态有_____ 种。
(2)C、N、O三种元素中电负性最小的是_____ ,第一电离能最大的是_____ (填元素符号), 中的键角大小为
中的键角大小为_____ 。
(3)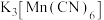 中Mn的化合价为+3价,则C的化合价为
中Mn的化合价为+3价,则C的化合价为_____ ,配体为_____ ,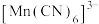 中
中 键与
键与 键的数目之比为
键的数目之比为_____ 。
 )。工业上可用菱锰矿生产锰的一种配合物
)。工业上可用菱锰矿生产锰的一种配合物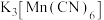 ,其主要应用于制药、电镀、造纸、钢铁生产。
,其主要应用于制药、电镀、造纸、钢铁生产。(1)Mn元素在周期表中的位置为
(2)C、N、O三种元素中电负性最小的是
 中的键角大小为
中的键角大小为(3)
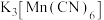 中Mn的化合价为+3价,则C的化合价为
中Mn的化合价为+3价,则C的化合价为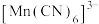 中
中 键与
键与 键的数目之比为
键的数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知A、B、C、D、E、F六种元素的原子序数依次递增,前四种元素为短周期元素。A位于元素周期表s区,电子层数与未成对电子数相等;B基态原子中电子占据三种能量不同的原子轨道,且每轨道中的电子总数相同;D原子核外成对电子数为未成对电子数的3倍;F位于第四周期d区,最高能级的原子轨道内只有2个未成对电子;E的一种氧化物具有磁性。
(1)E基态原子的价层电子排布式为__________________ 。第二周期基态原子未成对电子数与F相同且电负性最小的元素名称为____________ 。
(2)CD3- 的空间构型为_______________ 。
(3)A、B、D三元素组成的一种化合物X是家庭装修材料中常含有的一种有害气体,X分子中的中心原子采用_____________ 杂化。
(4)F(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=________ 。根据等电子原理,B、D 分子内σ键与π键的个数之比为______________ 。
(5)一种EF的合金晶体具有面心立方最密堆积的结构。在晶胞中,F位于顶点,E位于面心,该合金中EF的原子个数之比为_________________ 。若晶胞边长a pm,则合金密度为______________ g·cm3(列式表达,不计算)。
(1)E基态原子的价层电子排布式为
(2)CD3- 的空间构型为
(3)A、B、D三元素组成的一种化合物X是家庭装修材料中常含有的一种有害气体,X分子中的中心原子采用
(4)F(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=
(5)一种EF的合金晶体具有面心立方最密堆积的结构。在晶胞中,F位于顶点,E位于面心,该合金中EF的原子个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1)写出铜的基态原子的电子排布式:______ 。
(2)基态Fe原子有______ 个未成对电子,Fe3+的电子排布式为______ 。
(3)Fe在周期表中位于第______ 周期第______ 族,属于______ 区。
Ⅱ.回答下列问题:
(4)p电子的原子轨道呈______ 形。
(5)基态Al3+核外共有______ 种不同运动状态的电子。
(6)钒(V)元素广泛用于催化及钢铁工业,其价层电子的轨道表示式为_______ 。
(1)写出铜的基态原子的电子排布式:
(2)基态Fe原子有
(3)Fe在周期表中位于第
Ⅱ.回答下列问题:
(4)p电子的原子轨道呈
(5)基态Al3+核外共有
(6)钒(V)元素广泛用于催化及钢铁工业,其价层电子的轨道表示式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下列问题:
(1)第三周期中半径最大的元素A,其基态原子的价层电子轨道表示式为_______ ;
(2)B元素的负二价离子电子层结构与氖相同,写出B离子的电子排布式_______ ;
(3)元素C的M层p轨道电子比s轨道电子多2个,写出元素的原子结构示意图:_______ ;
(4)元素D处于周期表第四周期第ⅦB族,其原子的价电子排布式为_______ ;
(5)某元素E的激发态原子的电子排布式为1s22s22p63s23p34s1,则该元素基态原子的电子排布式为_______ ;
(6)元素F基态原子核外有8个原子轨道占有电子,则该原子电子排布式是:_______ ;
(7)G元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,G的元素符号为_______ ,其基态原子的电子排布式为_______ 。
(1)第三周期中半径最大的元素A,其基态原子的价层电子轨道表示式为
(2)B元素的负二价离子电子层结构与氖相同,写出B离子的电子排布式
(3)元素C的M层p轨道电子比s轨道电子多2个,写出元素的原子结构示意图:
(4)元素D处于周期表第四周期第ⅦB族,其原子的价电子排布式为
(5)某元素E的激发态原子的电子排布式为1s22s22p63s23p34s1,则该元素基态原子的电子排布式为
(6)元素F基态原子核外有8个原子轨道占有电子,则该原子电子排布式是:
(7)G元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,G的元素符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】水是自然界中普遍存在的一种重要物质,根据下列信息回答问题:
(1)氧原子基态时价层电子的电子排布图为____________ 。
(2)已知2H2O H3O+ +OH-,H3O+的立体构型是
H3O+ +OH-,H3O+的立体构型是____________ ,中心原子的杂化类型是___________ 。
(3)下列关于水的说法正确的是__________ (选填序号)。
①在冰晶体中每一个水分子内含有两个氢键;
②水分子是由极性键构成的极性分子;
③水在化学反应中可以作氧化剂,也可以作还原剂;
④水分子中既含σ键,又含有π键;
⑤纯水呈中性,所以在任何条件下纯水的PH均为7;
⑥水分子中的氧原子的杂化类型是sp3杂化,价层电子对数是2。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低。
稳定性:___________________ 沸点:___________________
(1)氧原子基态时价层电子的电子排布图为
(2)已知2H2O
 H3O+ +OH-,H3O+的立体构型是
H3O+ +OH-,H3O+的立体构型是(3)下列关于水的说法正确的是
①在冰晶体中每一个水分子内含有两个氢键;
②水分子是由极性键构成的极性分子;
③水在化学反应中可以作氧化剂,也可以作还原剂;
④水分子中既含σ键,又含有π键;
⑤纯水呈中性,所以在任何条件下纯水的PH均为7;
⑥水分子中的氧原子的杂化类型是sp3杂化,价层电子对数是2。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低。
稳定性:
您最近一年使用:0次



