我国科学家利用Fe2Na3红紫素催化剂实现CO2还原制备CO,利用可见光催化还原CO2,将CO2转化为增值化学原料(HCOOH、HCHO、CH3OH等),这被认为是一种可持续的CO2资源化有效途径。
(1)已知几种物质的燃烧热(△H)如表所示:
已知:H2O(g)=H2O(l) △H=—44kJ•mol-1,CO2(g)+2H2(g) HCHO(g)+H2O(g) △H=
HCHO(g)+H2O(g) △H=_______ kJ•mol-1。
(2)在一定温度下,将1molCO2(g)和3molH2(g)通入某恒容密闭容器中,发生反应CO2(g)+H2(g) HCOOH(g),测得不同时刻容器中CO2的体积分数[φ(CO2)]如表所示:
HCOOH(g),测得不同时刻容器中CO2的体积分数[φ(CO2)]如表所示:
达到平衡时CO2的转化率为________ 。
(3)将n(CO2):n(H2)=1:4的混合气体充入某密闭容器中,同时发生反应1和反应2。
反应1:CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41.2kJ•mol-1
CO(g)+H2O(g) △H1=+41.2kJ•mol-1
反应2:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2<0。
CH3OH(g)+H2O(g) △H2<0。
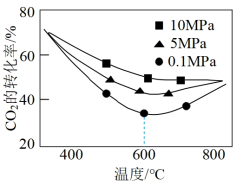
在不同温度、压强下,测得相同时间内CO2的转化率如图,0.1MPa时,CO2的转化率在600℃之后随温度升高而增大的主要原因是________ 。
(4)在一定温度下,向容积为2L的恒容密闭容器中充入1molCO2(g)和nmolH2(g),仅发生(3)中的反应2。实验测得CH3OH的平衡分压与起始投料比[ ]的关系如图:
]的关系如图:
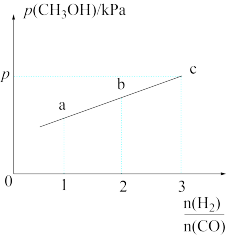
①起始时容器内气体的总压强为8pkPa,若10min时反应到达c点,则0~10min内,v(H2)=________ mol•L-1•min-1。
②b点时反应的平衡常数Kp=_______ (用含p的表达式表示)(kPa)-2。(已知:用气体分压计算的平衡常数为Kp,分压=总压×物质的量分数)
(5)我国科学家开发催化剂,以惰性材料为阳极,在酸性条件下电解还原CO2制备HCHO,其阴极的电极反应式为________ 。
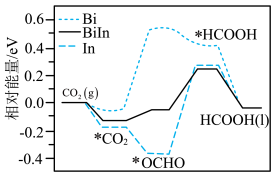
(6)我国学者探究了Biln合金催化剂电化学还原CO2生产HCOOH的催化性能及机理,并通过DFT计算催化剂表面该还原过程的物质的相对能量,如图所示(带“*”表示物质处于吸附态),试从图分析,采用Biln合金催化剂优于单金属Bi催化剂的原因:________ 。
(1)已知几种物质的燃烧热(△H)如表所示:
| 物质 | HCHO(g) | H2(g) |
| 燃烧热(△H)/(kJ•mol-1) | -570.8 | -285.8 |
 HCHO(g)+H2O(g) △H=
HCHO(g)+H2O(g) △H=(2)在一定温度下,将1molCO2(g)和3molH2(g)通入某恒容密闭容器中,发生反应CO2(g)+H2(g)
 HCOOH(g),测得不同时刻容器中CO2的体积分数[φ(CO2)]如表所示:
HCOOH(g),测得不同时刻容器中CO2的体积分数[φ(CO2)]如表所示:| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| φ(CO2) | 0.250 | 0.230 | 0.215 | 0.205 | 0.200 | 0.200 |
(3)将n(CO2):n(H2)=1:4的混合气体充入某密闭容器中,同时发生反应1和反应2。
反应1:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+41.2kJ•mol-1
CO(g)+H2O(g) △H1=+41.2kJ•mol-1反应2:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2<0。
CH3OH(g)+H2O(g) △H2<0。在不同温度、压强下,测得相同时间内CO2的转化率如图,0.1MPa时,CO2的转化率在600℃之后随温度升高而增大的主要原因是

(4)在一定温度下,向容积为2L的恒容密闭容器中充入1molCO2(g)和nmolH2(g),仅发生(3)中的反应2。实验测得CH3OH的平衡分压与起始投料比[
 ]的关系如图:
]的关系如图:
①起始时容器内气体的总压强为8pkPa,若10min时反应到达c点,则0~10min内,v(H2)=
②b点时反应的平衡常数Kp=
(5)我国科学家开发催化剂,以惰性材料为阳极,在酸性条件下电解还原CO2制备HCHO,其阴极的电极反应式为
(6)我国学者探究了Biln合金催化剂电化学还原CO2生产HCOOH的催化性能及机理,并通过DFT计算催化剂表面该还原过程的物质的相对能量,如图所示(带“*”表示物质处于吸附态),试从图分析,采用Biln合金催化剂优于单金属Bi催化剂的原因:

更新时间:2023-06-11 09:59:08
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】缓冲和供氧是维持人体正常生理活动的两个重要平衡系统,回答下列问题:
Ⅰ.人体血液中存在平衡:H2CO3 (aq) H+(aq)+HCO3-(aq) ΔH,该平衡可使血液的pH维持在一定范围内。
H+(aq)+HCO3-(aq) ΔH,该平衡可使血液的pH维持在一定范围内。
(1)已知:CO2(g) CO2(aq) ΔH1=akJ·mol-l;
CO2(aq) ΔH1=akJ·mol-l;
CO2(aq)+H2O(l) H2CO3 (aq) ΔH2=bkJ·mol-1;
H2CO3 (aq) ΔH2=bkJ·mol-1;
HCO (aq)
(aq) H+(aq)+CO
H+(aq)+CO (aq) ΔH3=ckJ·mol-1;
(aq) ΔH3=ckJ·mol-1;
CO2(g)+H2O(l) 2H+(aq)+ CO
2H+(aq)+ CO (aq) ΔH4=dkJ·mol-1。
(aq) ΔH4=dkJ·mol-1。
则上述电离方程式中ΔH =_____________ (用含a、b、c、d的代数式表示)。
(2)若某人血液中c(HCO ):c(H2CO3) = 20:1,pKa1(H2CO3)=6.1,则该人血液的pH为
):c(H2CO3) = 20:1,pKa1(H2CO3)=6.1,则该人血液的pH为______________ 。(lg2=0.3)若pH升高,则c(H2CO3)/c(HCO )=
)=___________ (填“增大”“减小”或“不变”)。
(3)当有少量酸性物质进入血液后,血液的pH变化不大,用平衡移动原理解释上述现象:_____________ 。
Ⅱ.肌细胞石储存氧气和分配氧气时存在如下平衡

(4)经测定动物体温升高,氧气的结合度[α(MbO2),氧合肌红蛋白的浓度占肌红蛋白初始浓度的百分数]降低,则该反应的ΔH_______________ (填“>”或“<”)0。
(5)温度为37 ℃时,氧气的结合度[α(MbO2)与氧气的平衡分压[p(O2)]关系如下图所示:
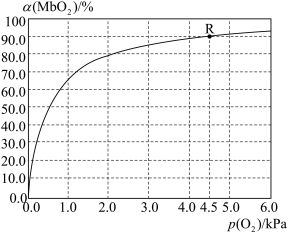
①利用R点所示数据,计算37 ℃时该反应的平衡常数K=_________________ (氧气的平衡浓度可用氧气的平衡分压代替求算)。
②已知37 ℃时,该反应的正反应速率v(正)=k1c(Mb)×p(O2),逆反应速率v(逆)=k2c(MbO2),若k2=60s-1,则k1=___________________ 。
Ⅰ.人体血液中存在平衡:H2CO3 (aq)
 H+(aq)+HCO3-(aq) ΔH,该平衡可使血液的pH维持在一定范围内。
H+(aq)+HCO3-(aq) ΔH,该平衡可使血液的pH维持在一定范围内。(1)已知:CO2(g)
 CO2(aq) ΔH1=akJ·mol-l;
CO2(aq) ΔH1=akJ·mol-l;CO2(aq)+H2O(l)
 H2CO3 (aq) ΔH2=bkJ·mol-1;
H2CO3 (aq) ΔH2=bkJ·mol-1;HCO
 (aq)
(aq) H+(aq)+CO
H+(aq)+CO (aq) ΔH3=ckJ·mol-1;
(aq) ΔH3=ckJ·mol-1;CO2(g)+H2O(l)
 2H+(aq)+ CO
2H+(aq)+ CO (aq) ΔH4=dkJ·mol-1。
(aq) ΔH4=dkJ·mol-1。则上述电离方程式中ΔH =
(2)若某人血液中c(HCO
 ):c(H2CO3) = 20:1,pKa1(H2CO3)=6.1,则该人血液的pH为
):c(H2CO3) = 20:1,pKa1(H2CO3)=6.1,则该人血液的pH为 )=
)=(3)当有少量酸性物质进入血液后,血液的pH变化不大,用平衡移动原理解释上述现象:
Ⅱ.肌细胞石储存氧气和分配氧气时存在如下平衡

(4)经测定动物体温升高,氧气的结合度[α(MbO2),氧合肌红蛋白的浓度占肌红蛋白初始浓度的百分数]降低,则该反应的ΔH
(5)温度为37 ℃时,氧气的结合度[α(MbO2)与氧气的平衡分压[p(O2)]关系如下图所示:

①利用R点所示数据,计算37 ℃时该反应的平衡常数K=
②已知37 ℃时,该反应的正反应速率v(正)=k1c(Mb)×p(O2),逆反应速率v(逆)=k2c(MbO2),若k2=60s-1,则k1=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】运用化学知识回答下列问题:
(1)载人航天器中,可通过如下反应将航天员呼出的 转化为
转化为 ,再通过电解
,再通过电解 获得
获得 。
。
已知:①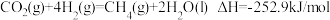
②
则 和
和 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
(2)已知 和
和 可以相互转化:
可以相互转化: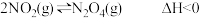 。现将一定量
。现将一定量 和
和 的混合气体通入体积为2L的恒温密闭容器中,物质浓度随时间的变化关系如图1所示。
的混合气体通入体积为2L的恒温密闭容器中,物质浓度随时间的变化关系如图1所示。
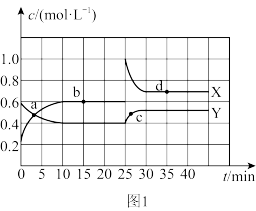
①图中曲线_______ (填“X”或“Y”)表示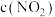 随时间的变化。
随时间的变化。
②a、b、c、d四个点中,表示化学反应处于平衡状态的是_______ (填字母)。d点的平衡常数K=_______ (计算结果精确到0.1)。
③ 内,
内,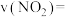
_______ 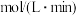 。
。
(3) 催化氧化生成
催化氧化生成 :
: ,混合体系中
,混合体系中 的百分含量与温度(T)的关系如图2所示(曲线上任何一点都表示平衡状态)。
的百分含量与温度(T)的关系如图2所示(曲线上任何一点都表示平衡状态)。
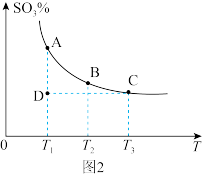
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡_______ (填“向左”、“向右”或“不”)移动。
②若反应进行到状态D时,
_______ (填“>”、“<”或“=”,下同) 。
。
③平衡常数K(A)_______ K(C)。
(1)载人航天器中,可通过如下反应将航天员呼出的
 转化为
转化为 ,再通过电解
,再通过电解 获得
获得 。
。已知:①
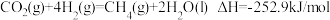
②

则
 和
和 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)已知
 和
和 可以相互转化:
可以相互转化: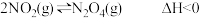 。现将一定量
。现将一定量 和
和 的混合气体通入体积为2L的恒温密闭容器中,物质浓度随时间的变化关系如图1所示。
的混合气体通入体积为2L的恒温密闭容器中,物质浓度随时间的变化关系如图1所示。
①图中曲线
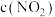 随时间的变化。
随时间的变化。②a、b、c、d四个点中,表示化学反应处于平衡状态的是
③
 内,
内,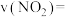
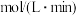 。
。(3)
 催化氧化生成
催化氧化生成 :
: ,混合体系中
,混合体系中 的百分含量与温度(T)的关系如图2所示(曲线上任何一点都表示平衡状态)。
的百分含量与温度(T)的关系如图2所示(曲线上任何一点都表示平衡状态)。 
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡
②若反应进行到状态D时,

 。
。③平衡常数K(A)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】CO、CO2、CH3OH等含碳物质是重要的基础化工原料。回答下列问题:
(1)CH3OH(l)气化时吸收的热量为27 kJ∙mol−1, CH3OH(g)的燃烧热为677 kJ∙mol−1,写出CH3OH(l)完全燃烧的热化学方程式:_________ 。
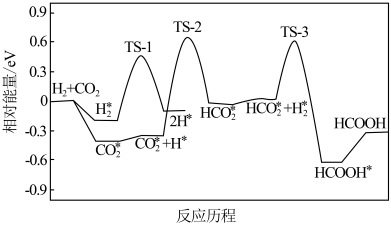
(2)CO2的资源化利用和转化技术的研究对实现碳达峰和碳中和有重要意义。在席夫碱(含“−RC=N−”有机物)修饰的纳米金催化剂上,CO2直接催化加氢生成甲酸。其反应历程如图所示,其中吸附在催化剂表面上的物质用*标注,TS为过渡态。该历程中起决速步骤的化学方程式是_________ 。
(3)在恒温恒容密闭容器中投入足量石墨与CO2进行反应C(s)+CO2(g) 2CO(g),可判定其达到平衡的条件有_______(填序号)。
2CO(g),可判定其达到平衡的条件有_______(填序号)。
(4)CO2与H2在催化剂作用下可转化为CH3OH,主要反应如下:
反应1:CO2(g) +3H2(g) CH3OH(g) +H2O(g) ΔH1
CH3OH(g) +H2O(g) ΔH1
反应2:CO2(g) +H2(g) CO(g) +H2O(g) ΔH2
CO(g) +H2O(g) ΔH2
若起始按 =3投料,测得CO2的平衡转化率(X-CO2)和CH3OH的选择性(S–CH3OH)随温度、压强的变化如图所示[已知:S–CH3OH =
=3投料,测得CO2的平衡转化率(X-CO2)和CH3OH的选择性(S–CH3OH)随温度、压强的变化如图所示[已知:S–CH3OH =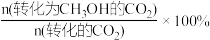 ]
]

①p1_____ (填 “>”或“<”)p2。
②温度高于350°C后,在压强p1和p2下,CO2的平衡转化率几乎交于一点的原因是_____ 。
③250 °C时反应2的压强平衡常数Kp=_______ (结果保留2位有效数字)。
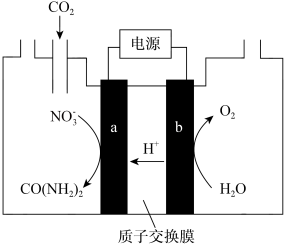
(5)近年研究发现,电催化CO2和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示,则电解过程中生成尿素的电极反应式是
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示,则电解过程中生成尿素的电极反应式是_________ 。
(1)CH3OH(l)气化时吸收的热量为27 kJ∙mol−1, CH3OH(g)的燃烧热为677 kJ∙mol−1,写出CH3OH(l)完全燃烧的热化学方程式:
(2)CO2的资源化利用和转化技术的研究对实现碳达峰和碳中和有重要意义。在席夫碱(含“−RC=N−”有机物)修饰的纳米金催化剂上,CO2直接催化加氢生成甲酸。其反应历程如图所示,其中吸附在催化剂表面上的物质用*标注,TS为过渡态。该历程中起决速步骤的化学方程式是

(3)在恒温恒容密闭容器中投入足量石墨与CO2进行反应C(s)+CO2(g)
 2CO(g),可判定其达到平衡的条件有_______(填序号)。
2CO(g),可判定其达到平衡的条件有_______(填序号)。| A.容器总压保持不变 | B.相同时间内,消耗1molCO2的同时生成2molCO |
| C.CO的体积分数保持不变 | D.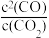 保持不变 保持不变 |
(4)CO2与H2在催化剂作用下可转化为CH3OH,主要反应如下:
反应1:CO2(g) +3H2(g)
 CH3OH(g) +H2O(g) ΔH1
CH3OH(g) +H2O(g) ΔH1反应2:CO2(g) +H2(g)
 CO(g) +H2O(g) ΔH2
CO(g) +H2O(g) ΔH2若起始按
 =3投料,测得CO2的平衡转化率(X-CO2)和CH3OH的选择性(S–CH3OH)随温度、压强的变化如图所示[已知:S–CH3OH =
=3投料,测得CO2的平衡转化率(X-CO2)和CH3OH的选择性(S–CH3OH)随温度、压强的变化如图所示[已知:S–CH3OH =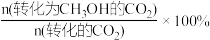 ]
]
①p1
②温度高于350°C后,在压强p1和p2下,CO2的平衡转化率几乎交于一点的原因是
③250 °C时反应2的压强平衡常数Kp=
(5)近年研究发现,电催化CO2和含氮物质(
 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示,则电解过程中生成尿素的电极反应式是
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示,则电解过程中生成尿素的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】苯甲醛(C6H5CHO)和丙酮(CH3COCH3)在固体碱催化剂下发生Aldol反应生成β-羟基酮(C10H12O2),β-羟基酮进一步脱水反应生成苄叉丙酮(C10H10O)。
Aldol反应:C6H5CHO(l)+CH3COCH3(l) C10H12O2(l) ΔH1<0
C10H12O2(l) ΔH1<0
脱水反应:C10H12O2(l) C10H10O(l)+H2O(l) ΔH2>0
C10H10O(l)+H2O(l) ΔH2>0
取0.05 mol苯甲醛和0.16 mol丙酮,加入固体碱催化剂,反应180 min达到化学平衡状态。测得不同温度下,苯甲醛、β-羟基酮、苄叉丙酮的物质的量随时间的关系如图甲、乙所示。

(1)反应中维持较大酮醛比[n(丙酮)/n(苯甲醛)],除利用反应物丙酮作溶剂外,还可能是________________________________ 。
(2)根据图甲、图乙可知,温度升高时,苯甲醛的转化率增大,但β-羟基酮的产率降低。请简述其可能原因:________________________________ 。
(3)反应温度为20 ℃,加入0.5 g固体催化剂,反应180 min后,苯甲醛的转化率为80%,苄叉丙酮的产率为60%,测得反应后混合物总体积为V L。
①β-羟基酮的产率为=________ 。
②脱水反应的平衡常数KC=________ 。
(4)苄叉丙酮电羧化可用于固定CO2。室温下镁棒为辅助电极,银棒为工作电极,常压下通入CO2 30 min至饱和后开始电解苄叉丙酮(C10H10O)。电解过程中持续通入CO2,在工作电极附近得到电羧化产物2-苯基乙酰丙酸(C11H12O3)。
①镁棒作________ 极(填“阴”或“阳”)。
②写出苄叉丙酮转化为2-苯基乙酰丙酸的电极反应式:________________ (有机物用分子式表示)。
③在电解过程中维持电流强度为I(A),t min后制得2-苯基乙酰丙酸b g。则工作电极的法拉第电流效率为________________ 。【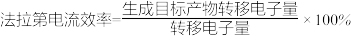 ,Q=It=ne×F,法拉第常数为F,单位C/mol】
,Q=It=ne×F,法拉第常数为F,单位C/mol】
Aldol反应:C6H5CHO(l)+CH3COCH3(l)
 C10H12O2(l) ΔH1<0
C10H12O2(l) ΔH1<0脱水反应:C10H12O2(l)
 C10H10O(l)+H2O(l) ΔH2>0
C10H10O(l)+H2O(l) ΔH2>0取0.05 mol苯甲醛和0.16 mol丙酮,加入固体碱催化剂,反应180 min达到化学平衡状态。测得不同温度下,苯甲醛、β-羟基酮、苄叉丙酮的物质的量随时间的关系如图甲、乙所示。

(1)反应中维持较大酮醛比[n(丙酮)/n(苯甲醛)],除利用反应物丙酮作溶剂外,还可能是
(2)根据图甲、图乙可知,温度升高时,苯甲醛的转化率增大,但β-羟基酮的产率降低。请简述其可能原因:
(3)反应温度为20 ℃,加入0.5 g固体催化剂,反应180 min后,苯甲醛的转化率为80%,苄叉丙酮的产率为60%,测得反应后混合物总体积为V L。
①β-羟基酮的产率为=
②脱水反应的平衡常数KC=
(4)苄叉丙酮电羧化可用于固定CO2。室温下镁棒为辅助电极,银棒为工作电极,常压下通入CO2 30 min至饱和后开始电解苄叉丙酮(C10H10O)。电解过程中持续通入CO2,在工作电极附近得到电羧化产物2-苯基乙酰丙酸(C11H12O3)。
①镁棒作
②写出苄叉丙酮转化为2-苯基乙酰丙酸的电极反应式:
③在电解过程中维持电流强度为I(A),t min后制得2-苯基乙酰丙酸b g。则工作电极的法拉第电流效率为
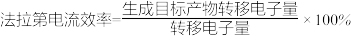 ,Q=It=ne×F,法拉第常数为F,单位C/mol】
,Q=It=ne×F,法拉第常数为F,单位C/mol】
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】 既是化工原料,但也是空气污染物。回答下列问题:
既是化工原料,但也是空气污染物。回答下列问题:
(1)已知反应:
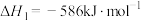 ;
;

 ;
;
则反应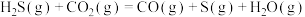 的
的
_______  。
。
(2) 与
与 在高温下发生反应:
在高温下发生反应: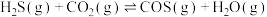
 。在610K时,将
。在610K时,将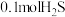 与
与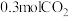 充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时
充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时 的物质的量分数为0.125,用
的物质的量分数为0.125,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
_______ 。 的平衡转化率
的平衡转化率
______ %。
(3)利用 的热分解反应可生产
的热分解反应可生产 :
: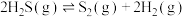 。现将
。现将 通入某恒压(压强
通入某恒压(压强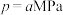 )密闭容器中,在不同温度下测得
)密闭容器中,在不同温度下测得 的平衡转化率如图所示。
的平衡转化率如图所示。

已知:对于气相反应,用某组分(B)的平衡分压( )代替物质的量浓度(
)代替物质的量浓度(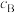 )也可表示平衡常数(
)也可表示平衡常数( )。(
)。(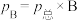 的物质的量分数,
的物质的量分数, 为平衡时气体总压强)。
为平衡时气体总压强)。
温度升高时,混合气体的平均摩尔质量_______ (填“增大”“减小”或“不变”)。温度为 ℃时。该反应的平衡常数
℃时。该反应的平衡常数
_______ MPa(用含a的代数式表示)。
(4)据预测,到2040年我国煤炭消费仍将占能源结构的三分之一左右。 在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
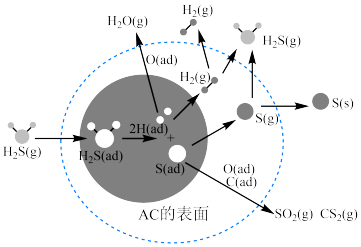
① 、
、 、
、 的键角从小到大排列顺序为
的键角从小到大排列顺序为_______ 。
②下列有关叙述错误的是_______ (填字母)。
A.图中阴影部分表示 分子的吸附与解离
分子的吸附与解离
B.AC表面的温度不同, 的去除率不同
的去除率不同
C. 在AC表面作用生成的产物有
在AC表面作用生成的产物有 、
、 、S、
、S、 、
、 等
等
D.图中反应过程中只有 链的断裂。没有
链的断裂。没有 健的形成
健的形成
 既是化工原料,但也是空气污染物。回答下列问题:
既是化工原料,但也是空气污染物。回答下列问题:(1)已知反应:

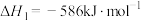 ;
;
 ;
;则反应
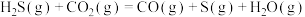 的
的
 。
。(2)
 与
与 在高温下发生反应:
在高温下发生反应: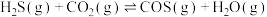
 。在610K时,将
。在610K时,将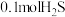 与
与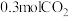 充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时
充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时 的物质的量分数为0.125,用
的物质的量分数为0.125,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
 的平衡转化率
的平衡转化率
(3)利用
 的热分解反应可生产
的热分解反应可生产 :
: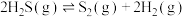 。现将
。现将 通入某恒压(压强
通入某恒压(压强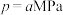 )密闭容器中,在不同温度下测得
)密闭容器中,在不同温度下测得 的平衡转化率如图所示。
的平衡转化率如图所示。
已知:对于气相反应,用某组分(B)的平衡分压(
 )代替物质的量浓度(
)代替物质的量浓度(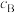 )也可表示平衡常数(
)也可表示平衡常数( )。(
)。(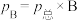 的物质的量分数,
的物质的量分数, 为平衡时气体总压强)。
为平衡时气体总压强)。温度升高时,混合气体的平均摩尔质量
 ℃时。该反应的平衡常数
℃时。该反应的平衡常数
(4)据预测,到2040年我国煤炭消费仍将占能源结构的三分之一左右。
 在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
①
 、
、 、
、 的键角从小到大排列顺序为
的键角从小到大排列顺序为②下列有关叙述错误的是
A.图中阴影部分表示
 分子的吸附与解离
分子的吸附与解离B.AC表面的温度不同,
 的去除率不同
的去除率不同C.
 在AC表面作用生成的产物有
在AC表面作用生成的产物有 、
、 、S、
、S、 、
、 等
等D.图中反应过程中只有
 链的断裂。没有
链的断裂。没有 健的形成
健的形成
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】大气中氮氧化物( )是造成灰霾、光化学烟雾的重要原因,对氮氧化物的研究具有重要意义。回答下列问题:
)是造成灰霾、光化学烟雾的重要原因,对氮氧化物的研究具有重要意义。回答下列问题:
(1)已知在催化条件下 与CO发生反应:
与CO发生反应: 。
。
①在 ℃,将
℃,将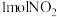 和1molCO加入容积为0.5L的密闭容器中发生上述反应,2min末,测得CO为0.8mol。在0~2min内,用
和1molCO加入容积为0.5L的密闭容器中发生上述反应,2min末,测得CO为0.8mol。在0~2min内,用 浓度变化表示的化学反应速率为
浓度变化表示的化学反应速率为_______ 。
②研究表明,在 ℃,
℃, 与CO还会发生副反应
与CO还会发生副反应 。若在
。若在 ℃,恒容下,向平衡体系中再充入少量
℃,恒容下,向平衡体系中再充入少量 ,反应
,反应 的平衡将
的平衡将_______ (填“正向移动”“逆向移动”或“不移动”)。
(2)若在温度和体积相同的两个密闭容器中,按不同方式投入反应物,只发生反应 ,测得平衡时有关数据如下表:
,测得平衡时有关数据如下表:
α=_______ ,写出该反应的热化学方程式_______ ( 用含
用含 或
或 的表达式表示)。
的表达式表示)。
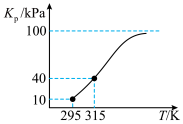
(3)将一定量 气体充入压强为100kPa的恒压容器中,发生反应
气体充入压强为100kPa的恒压容器中,发生反应
 ,测得平衡常数
,测得平衡常数 (用各物质的平衡分压代替平衡浓度计算)随温度的变化如图所示。
(用各物质的平衡分压代替平衡浓度计算)随温度的变化如图所示。
①
_______ 0(填“>”“=”或“<”)。
②向体积相等的丙、丁两个密闭容器中分别加入等量的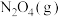 ,发生反应并达到平衡。保持丙容器恒容、丁容器恒压,将两体系的温度均从295K升至315K,则
,发生反应并达到平衡。保持丙容器恒容、丁容器恒压,将两体系的温度均从295K升至315K,则_______ (填“丙”或“丁”)容器中的平衡移动程度更大,原因是_______ 。
 )是造成灰霾、光化学烟雾的重要原因,对氮氧化物的研究具有重要意义。回答下列问题:
)是造成灰霾、光化学烟雾的重要原因,对氮氧化物的研究具有重要意义。回答下列问题:(1)已知在催化条件下
 与CO发生反应:
与CO发生反应: 。
。①在
 ℃,将
℃,将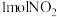 和1molCO加入容积为0.5L的密闭容器中发生上述反应,2min末,测得CO为0.8mol。在0~2min内,用
和1molCO加入容积为0.5L的密闭容器中发生上述反应,2min末,测得CO为0.8mol。在0~2min内,用 浓度变化表示的化学反应速率为
浓度变化表示的化学反应速率为②研究表明,在
 ℃,
℃, 与CO还会发生副反应
与CO还会发生副反应 。若在
。若在 ℃,恒容下,向平衡体系中再充入少量
℃,恒容下,向平衡体系中再充入少量 ,反应
,反应 的平衡将
的平衡将(2)若在温度和体积相同的两个密闭容器中,按不同方式投入反应物,只发生反应
 ,测得平衡时有关数据如下表:
,测得平衡时有关数据如下表:| 容器 | 甲 | 乙 |
| 反应物投入量 | 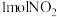 、 、 | 2molNO、 |
| CO或NO的转化率 | 40% | α |
| 能量变化 | 放出 | 吸收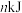 |
 用含
用含 或
或 的表达式表示)。
的表达式表示)。(3)将一定量
 气体充入压强为100kPa的恒压容器中,发生反应
气体充入压强为100kPa的恒压容器中,发生反应
 ,测得平衡常数
,测得平衡常数 (用各物质的平衡分压代替平衡浓度计算)随温度的变化如图所示。
(用各物质的平衡分压代替平衡浓度计算)随温度的变化如图所示。
①

②向体积相等的丙、丁两个密闭容器中分别加入等量的
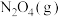 ,发生反应并达到平衡。保持丙容器恒容、丁容器恒压,将两体系的温度均从295K升至315K,则
,发生反应并达到平衡。保持丙容器恒容、丁容器恒压,将两体系的温度均从295K升至315K,则
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】氮氧化物的排放与雾霾天气的产生有关,对其进行无害化处理是化学工作者研究的重要课题。
(1)已知拆开1molN2(g)、1molO2(g)、1molN2O(g)分子中的化学键分别需要吸收945kJ、498kJ、1112.5kJ能量,请写出对N2O进行无害化处理时的热化学方程式_______ 。
(2)去除NOx的一种方法是用活性炭吸附。已知发生的反应如下:
反应I:C(s)+2NO(g) N2(g)+CO2(g) ∆H=-34.0 kJ/mol
N2(g)+CO2(g) ∆H=-34.0 kJ/mol
反应II:2C(s)+2NO2(g) N2(g)+2CO2(g) ∆H=-64.2 kJ/mol
N2(g)+2CO2(g) ∆H=-64.2 kJ/mol
①若将足量的活性炭和一定的NO2气体加入某密闭容器,维持温度为T℃,图1为不同压强下反应II经过相同时间后NO2的转化率。下列关于反应II说法正确的是_______ 。
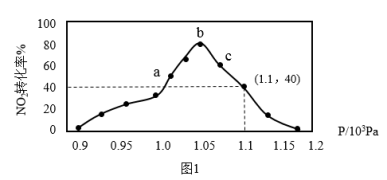
A.a点处于化学平衡状态
B.c点处于化学平衡状态
C.b点反应速率最大
D.b点与c点平衡常数相同
②用某物质的平衡分压代替其物质的浓度也可以表示化学平衡常数(记作Kp);根据①中图1求反应II在T℃、1.1 106Pa时的化学平衡常数Kp=
106Pa时的化学平衡常数Kp=_______ Pa(用表込式表示);已知:气体分压(p分)=气体总压(p总) 体积分数。
体积分数。
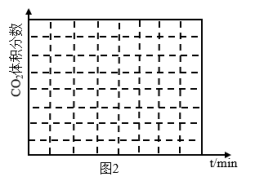
③T℃、恒容条件下,在某密闭容器中加入足量的活性炭和一定的NOx[n(NO2):n(NO)=1:1的混合气体]气体,假设反应l和反应II同时发生,且速率vII>vI,请在图2中画出反应体系中CO2体积分数随肘向t变化的总趋势图______ 。
(3)电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如图所示:
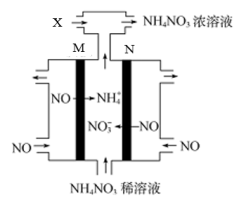
①写出N极的电极反应式___________ 。
②加入的物质X为___________ (填化学式)。
(1)已知拆开1molN2(g)、1molO2(g)、1molN2O(g)分子中的化学键分别需要吸收945kJ、498kJ、1112.5kJ能量,请写出对N2O进行无害化处理时的热化学方程式
(2)去除NOx的一种方法是用活性炭吸附。已知发生的反应如下:
反应I:C(s)+2NO(g)
 N2(g)+CO2(g) ∆H=-34.0 kJ/mol
N2(g)+CO2(g) ∆H=-34.0 kJ/mol反应II:2C(s)+2NO2(g)
 N2(g)+2CO2(g) ∆H=-64.2 kJ/mol
N2(g)+2CO2(g) ∆H=-64.2 kJ/mol①若将足量的活性炭和一定的NO2气体加入某密闭容器,维持温度为T℃,图1为不同压强下反应II经过相同时间后NO2的转化率。下列关于反应II说法正确的是

A.a点处于化学平衡状态
B.c点处于化学平衡状态
C.b点反应速率最大
D.b点与c点平衡常数相同
②用某物质的平衡分压代替其物质的浓度也可以表示化学平衡常数(记作Kp);根据①中图1求反应II在T℃、1.1
 106Pa时的化学平衡常数Kp=
106Pa时的化学平衡常数Kp= 体积分数。
体积分数。③T℃、恒容条件下,在某密闭容器中加入足量的活性炭和一定的NOx[n(NO2):n(NO)=1:1的混合气体]气体,假设反应l和反应II同时发生,且速率vII>vI,请在图2中画出反应体系中CO2体积分数随肘向t变化的总趋势图

(3)电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如图所示:

①写出N极的电极反应式
②加入的物质X为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】CO2催化加氢制烯烃(CnH2n)是缓解化石能源消耗、实现减排的重要途径之一。FT转化路径(CO2→CO→COnH2n)涉及的主要反应如下:
ⅰ. CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=41.1kJ·mol−1
ⅱ. nCO(g)+2nH2(g)=CnH2n(g)+nH2O(g) n=2时,ΔH2=-210.2kJ·mol−1
ⅲ. CO(g)+3H2(g)=CH4(g)+H2O(g) ΔH3=−205.9kJ·mol−1
(1)2CO2(g)+6H2(g)=C2H4(g)+4H2O(g) ΔH=_______ kJ·mol−1。
(2)有利于提高CO2平衡转化率的措施有_______(填标号)。
(3) n(CO2):n(H2)投料比为1:3、压力为1MPa时,无烷烃产物的平衡体系中CO2转化率和产物选择性随反应温度变化曲线如图。
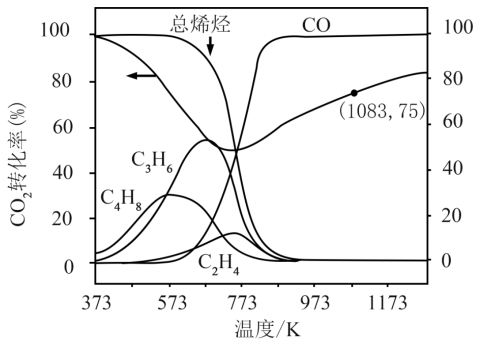
①有利于短链烯烃(n≤4)生成的温度范围为_______ (填标号)。
A.373~573K B.573~773K C.773~973K D.973~1173K
②计算1083K时,反应ⅰ的Kp=_______ 。
③373~1273K范围内,CO2的转化率先降低后升高的原因是_______ 。
(4)FT转化路径存在CH4含量过高问题,我国科学家采用Cr2O3(SG)和H-SAPO-34复合催化剂极大提高短链烯烃选择性。CO2在催化剂Cr2O3 (SG)表面转化为甲醇的各步骤所需要克服的能垒及甲醇在H-SAPO-34作用下产生乙烯、丙烯示意图如下。
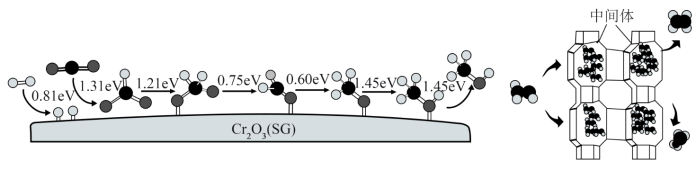
①吸附态用*表示,CO2→甲氧基(H3CO*)过程中,_______ 的生成是决速步骤(填化学式)。
②H-SAPO-34具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。从结构角度推测,短链烯烃选择性性提高的原因_______ 。
ⅰ. CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=41.1kJ·mol−1
ⅱ. nCO(g)+2nH2(g)=CnH2n(g)+nH2O(g) n=2时,ΔH2=-210.2kJ·mol−1
ⅲ. CO(g)+3H2(g)=CH4(g)+H2O(g) ΔH3=−205.9kJ·mol−1
(1)2CO2(g)+6H2(g)=C2H4(g)+4H2O(g) ΔH=
(2)有利于提高CO2平衡转化率的措施有_______(填标号)。
| A.增大n(CO2):n(H2)投料比 | B.增大体系压强 |
| C.使用高效催化剂 | D.及时分离H2O |

①有利于短链烯烃(n≤4)生成的温度范围为
A.373~573K B.573~773K C.773~973K D.973~1173K
②计算1083K时,反应ⅰ的Kp=
③373~1273K范围内,CO2的转化率先降低后升高的原因是
(4)FT转化路径存在CH4含量过高问题,我国科学家采用Cr2O3(SG)和H-SAPO-34复合催化剂极大提高短链烯烃选择性。CO2在催化剂Cr2O3 (SG)表面转化为甲醇的各步骤所需要克服的能垒及甲醇在H-SAPO-34作用下产生乙烯、丙烯示意图如下。

①吸附态用*表示,CO2→甲氧基(H3CO*)过程中,
②H-SAPO-34具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。从结构角度推测,短链烯烃选择性性提高的原因
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】减弱温室效应的方法之一是将 回收利用,科学家研究利用回收的
回收利用,科学家研究利用回收的 制取甲醛(
制取甲醛( ),反应的热化学方程式为
),反应的热化学方程式为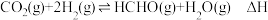 。请回答下列问题:
。请回答下列问题:
(1)已知:①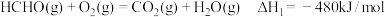
②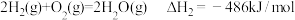
则由 和
和 合成甲醛的热化学方程式为:
合成甲醛的热化学方程式为:_______ 。
(2)一定条件下,将 的混合气体充入恒温恒容的密闭容器中,发生反应
的混合气体充入恒温恒容的密闭容器中,发生反应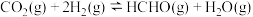 。
。
①下列说明反应已经达到平衡状态的是_______ (填选项字母)。
a.混合气体的平均相对分子质量不变 b.该反应的平衡常数保持不变
c. 的体积分数保持不变 d.容器内气体密度保持不变
的体积分数保持不变 d.容器内气体密度保持不变
②下列措施既能提高 的转化率又能加快反应速率的是
的转化率又能加快反应速率的是_______ (填选项字母)。
a.升高温度 b.使用高效催化剂 c.扩大容器体积 d.缩小容器体积
(3)实验室在 密闭容器中进行模拟上述合成甲醛(
密闭容器中进行模拟上述合成甲醛( 的实验。
的实验。 时,将
时,将 和
和 充入容器中,每隔一定时间测得容器内
充入容器中,每隔一定时间测得容器内 的物质的量如表所示:
的物质的量如表所示:
①反应开始20min内, 的平均反应速率为
的平均反应速率为_______ 。
②T1℃时,反应的平衡常数为K=_______ (保留三位有效数字)
③达到平衡时 的转化率为
的转化率为_______ 。
 回收利用,科学家研究利用回收的
回收利用,科学家研究利用回收的 制取甲醛(
制取甲醛( ),反应的热化学方程式为
),反应的热化学方程式为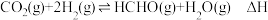 。请回答下列问题:
。请回答下列问题:(1)已知:①
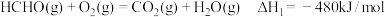
②
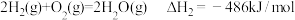
则由
 和
和 合成甲醛的热化学方程式为:
合成甲醛的热化学方程式为:(2)一定条件下,将
 的混合气体充入恒温恒容的密闭容器中,发生反应
的混合气体充入恒温恒容的密闭容器中,发生反应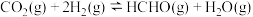 。
。①下列说明反应已经达到平衡状态的是
a.混合气体的平均相对分子质量不变 b.该反应的平衡常数保持不变
c.
 的体积分数保持不变 d.容器内气体密度保持不变
的体积分数保持不变 d.容器内气体密度保持不变②下列措施既能提高
 的转化率又能加快反应速率的是
的转化率又能加快反应速率的是a.升高温度 b.使用高效催化剂 c.扩大容器体积 d.缩小容器体积
(3)实验室在
 密闭容器中进行模拟上述合成甲醛(
密闭容器中进行模拟上述合成甲醛( 的实验。
的实验。 时,将
时,将 和
和 充入容器中,每隔一定时间测得容器内
充入容器中,每隔一定时间测得容器内 的物质的量如表所示:
的物质的量如表所示:| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
 的物质的量/mol 的物质的量/mol | 1.00 | 0.60 | 0.46 | 0.32 | 0.20 | 0.20 | 0.20 |
 的平均反应速率为
的平均反应速率为②T1℃时,反应的平衡常数为K=
③达到平衡时
 的转化率为
的转化率为
您最近一年使用:0次
【推荐1】生活污水中的氮和磷主要以铵盐和磷酸盐形式存在,可用电解法从溶液中去除。电解装置如图:以铁作阴极、石墨作阳极,可进行除氮;翻转电源正负极,以铁作阳极、石墨作阴极,可进行除磷。
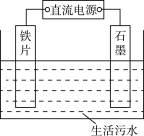
I.电解除氮
(1)在碱性溶液中,NH3能直接在电极放电,转化为N2,相应的电极反应式为:_______ 。
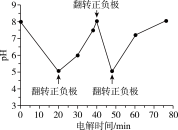
(2)有Cl-存在时,除氮原理如图1所示,主要依靠有效氯(HClO、ClO-)将NH4+ 或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度如图2:

①当pH<8时,主要发生HClO氧化NH4+ 的反应,其离子方程式为:____________ 。
②结合平衡移动原理解释,当pH<8时,氮的去除率随pH的降低而下降的原因是:_____ 。
③当pH>8时,ClO-发生歧化导致有效氯浓度下降,而氮的去除率却并未明显下降,可能的原因是(答出一点即可):______ 。
II.电解除磷
(3)除磷的原理是利用Fe2+ 将PO43- 转化为Fe3(PO4)2沉淀。
①用化学用语表示产生Fe2+的主要过程:_______________ 。
②如图为某含Cl- 污水在氮磷联合脱除过程中溶液pH的变化。推测在20-40 min时脱除的元素是________ 。
(4)测定污水磷含量的方法如下:取100mL污水,调节至合适pH后用AgNO3溶液使磷全部转化为Ag3PO4沉淀。将沉淀过滤并洗涤后,用硝酸溶解,再使用NH4SCN溶液滴定产生的Ag+,发生反应Ag++SCN-=AgSCN↓,共消耗c mol/LNH4SCN溶液V mL。则此污水中磷的含量为___ mg/L(以磷元素计)。

I.电解除氮
(1)在碱性溶液中,NH3能直接在电极放电,转化为N2,相应的电极反应式为:
(2)有Cl-存在时,除氮原理如图1所示,主要依靠有效氯(HClO、ClO-)将NH4+ 或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度如图2:

①当pH<8时,主要发生HClO氧化NH4+ 的反应,其离子方程式为:
②结合平衡移动原理解释,当pH<8时,氮的去除率随pH的降低而下降的原因是:
③当pH>8时,ClO-发生歧化导致有效氯浓度下降,而氮的去除率却并未明显下降,可能的原因是(答出一点即可):
II.电解除磷
(3)除磷的原理是利用Fe2+ 将PO43- 转化为Fe3(PO4)2沉淀。
①用化学用语表示产生Fe2+的主要过程:
②如图为某含Cl- 污水在氮磷联合脱除过程中溶液pH的变化。推测在20-40 min时脱除的元素是

(4)测定污水磷含量的方法如下:取100mL污水,调节至合适pH后用AgNO3溶液使磷全部转化为Ag3PO4沉淀。将沉淀过滤并洗涤后,用硝酸溶解,再使用NH4SCN溶液滴定产生的Ag+,发生反应Ag++SCN-=AgSCN↓,共消耗c mol/LNH4SCN溶液V mL。则此污水中磷的含量为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】CO2和H2一定条件下可以合成甲醇,该过程存在副反应二
反应一:
反应二:
(1)已知25℃和101kPa下,H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0kJ·mol-1,
H2O(1)=H2O(g)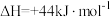 ,
,
则ΔH2=___________ kJ/mol。
(2)工业上可用CO2来制甲醇。
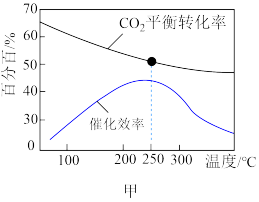
①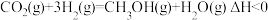 。根据图甲分析,实际工业生产中,反应温度选择250℃的理由是
。根据图甲分析,实际工业生产中,反应温度选择250℃的理由是___________ 。
②利用光电催化原理,由CO2和H2O制备CH3OH的装置如图乙。写出右侧的电极反应式:___________

(3)在恒容密闭容器内,充入1molCO2和3molH2,测得平衡时CO2转化率,CO和CH3OH选择性随温度变化如图所示【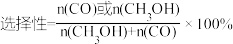 】。250℃下达平衡时,n(H2O)=
】。250℃下达平衡时,n(H2O)=___________ mol,其他条件不变,210℃比230℃平衡时生成的CH3OH___________ (填“多”或“少”)。

(4)在某密闭容器中充入n(CO2):n(H2)=5:17的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。
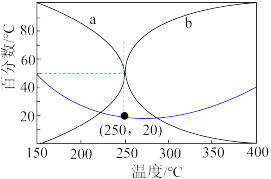
①表示平衡时CH3OH在含碳产物中物质的量百分数的曲线是___________ (填“a”或“b”)。
②CO2平衡转化率随温度的升高先减小后增大,增大的原因可能是___________ 。
反应一:

反应二:

(1)已知25℃和101kPa下,H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0kJ·mol-1,
H2O(1)=H2O(g)
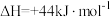 ,
,则ΔH2=
(2)工业上可用CO2来制甲醇。
①
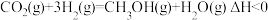 。根据图甲分析,实际工业生产中,反应温度选择250℃的理由是
。根据图甲分析,实际工业生产中,反应温度选择250℃的理由是
②利用光电催化原理,由CO2和H2O制备CH3OH的装置如图乙。写出右侧的电极反应式:

(3)在恒容密闭容器内,充入1molCO2和3molH2,测得平衡时CO2转化率,CO和CH3OH选择性随温度变化如图所示【
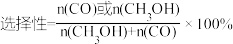 】。250℃下达平衡时,n(H2O)=
】。250℃下达平衡时,n(H2O)=
(4)在某密闭容器中充入n(CO2):n(H2)=5:17的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。

①表示平衡时CH3OH在含碳产物中物质的量百分数的曲线是
②CO2平衡转化率随温度的升高先减小后增大,增大的原因可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】CO2是一种温室气体,对人类的生存环境产生巨大的影响,将CO2作为原料转化为有用化学品,对实现碳中和及生态环境保护有着重要意义。
Ⅰ.工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:
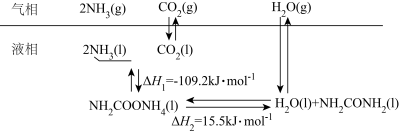
(1)液相中,合成尿素的热化学方程式为:2NH3(l)+CO2(l)=H2O(l)+NH2CONH2(l) △H=____ kJ/mol。
(2)在恒容密闭容器中发生反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) △H<0,下列说法错误的是_______ 。
Ⅱ.由 与
与 制备甲醇是当今研究的热点之一。
制备甲醇是当今研究的热点之一。
(3)在一定条件下,向0.5L恒容密闭容器中充入xmolCO2和ymolH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3=-50kJ·mol-1。
CH3OH(g)+H2O(g) △H3=-50kJ·mol-1。
①若x=1、y=3,测得在相同时间内,不同温度下H2的转化率如图1所示,T2时,若起始压强为10atm,Kp=_______ atm-2(结果保留一位小数,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
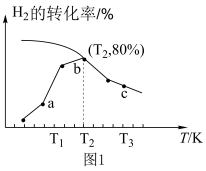
②已知速率方程v正=k正c(CO2)•c3(H2),v逆=k逆c(CH3OH)•c(H2O),k正、k逆是速率常数,只受温度影响,图2表示速率常数k正、k逆的对数lgk与温度的倒数 之间的关系, A、B、D、E分别代表图1中a点、c点的速率常数,点
之间的关系, A、B、D、E分别代表图1中a点、c点的速率常数,点_______ 表示c点的lgk逆。

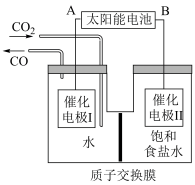
(4)我国科学家设计出如图装置实现CO2的转化,可有效解决温室效应及能源问题,总反应为CO2+NaCl CO+NaClO。忽略气体在溶液中的溶解及溶液的体积变化。
CO+NaClO。忽略气体在溶液中的溶解及溶液的体积变化。
①电极II的电极反应式为___________ ;
②理论上转化44gCO2,左室溶液质量增重___________ 。
Ⅰ.工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为:2NH3(l)+CO2(l)=H2O(l)+NH2CONH2(l) △H=
(2)在恒容密闭容器中发生反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) △H<0,下列说法错误的是
| A.反应在任何温度下都能自发进行 |
| B.增大CO2的浓度,有利于NH3的转化率增大 |
| C.当混合气体的密度不再发生改变时反应达平衡状态 |
| D.充入He,压强增大,平衡向正反应移动 |
Ⅱ.由
 与
与 制备甲醇是当今研究的热点之一。
制备甲醇是当今研究的热点之一。(3)在一定条件下,向0.5L恒容密闭容器中充入xmolCO2和ymolH2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3=-50kJ·mol-1。
CH3OH(g)+H2O(g) △H3=-50kJ·mol-1。①若x=1、y=3,测得在相同时间内,不同温度下H2的转化率如图1所示,T2时,若起始压强为10atm,Kp=

②已知速率方程v正=k正c(CO2)•c3(H2),v逆=k逆c(CH3OH)•c(H2O),k正、k逆是速率常数,只受温度影响,图2表示速率常数k正、k逆的对数lgk与温度的倒数
 之间的关系, A、B、D、E分别代表图1中a点、c点的速率常数,点
之间的关系, A、B、D、E分别代表图1中a点、c点的速率常数,点
(4)我国科学家设计出如图装置实现CO2的转化,可有效解决温室效应及能源问题,总反应为CO2+NaCl
 CO+NaClO。忽略气体在溶液中的溶解及溶液的体积变化。
CO+NaClO。忽略气体在溶液中的溶解及溶液的体积变化。①电极II的电极反应式为
②理论上转化44gCO2,左室溶液质量增重

您最近一年使用:0次



