17. 亚硝酸钠(NaNO
2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。某化学兴趣小组设计实验制备NaNO
2并探究其性质。
查阅资料信息:①2NO+Na
2O
2 =2NaNO
2;2NO
2 +Na
2O
2=2NaNO
3.②酸性KMnO
4溶液可将低价氮的氧化物或酸根离子氧化为

。
(1)NaNO
2的制备(夹持装置和加热装置均已略,已检查装置气密性)。
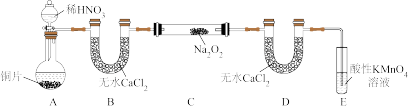
①若没有装置B,则装置C中Na
2O
2与水发生反应:
_______(填化学方程式)。
②制得的NaNO
2固体中混有的杂质主要为NaNO
3,改进措施是在装置A、B间添加
_______,提高NaNO
2的纯度。
③装置E中发生的主要反应的离子方程式为
_______。
(2)验证亚硝酸钠与70%硫酸反应的气体产物为NO和NO
2的混合气体。
已知:FeSO
4溶液可吸收NO;NO
2的沸点为21° C ,熔点为-11° C
。
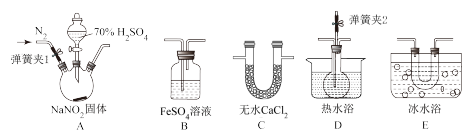
①为了检验装置A中生成的气体产物,装置的连接顺序是A→
_______。(按气流方向从左到右)
②反应前应打开弹簧夹1, 先通入一段时间氮气,目的是
_______。
③再关闭弹簧夹1,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。
设计实验检验装置A中产生的气体含有NO的操作及现象:
_______。
(3)查阅资料知:酸性条件下NaNO
2具有氧化性。利用所供试剂,设计实验方案验证此信息:
_______(供选用的试剂有NaNO
2溶液、FeSO
4溶液、稀硫酸、KSCN溶液)
(4)测定某亚硝酸钠样品的纯度。
设该样品的杂质均不与酸性KMnO
4溶液反应,可用酸性KMnO
4溶液测定NaNO
2的含量。称取2.0 g亚硝酸钠样品溶于水配成250 mL溶液,取出25. 00 mL溶液于锥形瓶中,再用0. 1000 mol· L
-1的酸性KMnO
4标准溶液进行滴定,消耗酸性KMnO
4标准溶液的体积如表:
| 实验组 | 第一组 | 第二组 | 第三组 | 第四组 |
| 消耗酸性KMnO4标准溶液的体积/mL | 9.97 | 10.02 | 12. 01 | 10. 01 |
该亚硝酸钠样品中NaNO
2的质量分数为
_______。