填空。
(1)某温度时,在容积为2L的密闭容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示。请分析图中数据,回答下列问题。
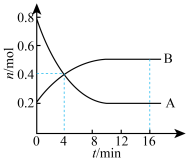
①该反应的化学方程式为___________ 。
②该反应进行到4min时,B的平均反应速率为___________ ,A的转化率为___________ 。
③4min时,反应是否达到平衡?___________ (填“是”或“否”);16min时,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(2)如图所示。
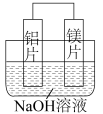
负极为___________ (填“铝片”或“镁片”)写出其电极反应式:___________ 。
(3)根据下列信息判断氢气燃烧生成水时的热量变化:
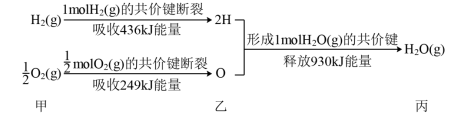
①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为___________ kJ;
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:___________ 。
(1)某温度时,在容积为2L的密闭容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示。请分析图中数据,回答下列问题。

①该反应的化学方程式为
②该反应进行到4min时,B的平均反应速率为
③4min时,反应是否达到平衡?
(2)如图所示。

负极为
(3)根据下列信息判断氢气燃烧生成水时的热量变化:

①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:
更新时间:2023-05-11 23:00:42
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】减少 的排放、捕集并利用
的排放、捕集并利用 是我国能源领域的一个重要战略方向。回答下列问题:
是我国能源领域的一个重要战略方向。回答下列问题:
Ⅰ.在 加氢合成甲醇的体系中,同时存在以下反应:
加氢合成甲醇的体系中,同时存在以下反应:
反应ⅰ:
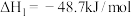
反应ⅱ:
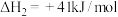
(1)反应ⅲ: 的
的
______ 。
(2)某温度下,向容积恒为1L的密闭容器中通入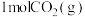 和
和 ,l0min后体系达到平衡,此时
,l0min后体系达到平衡,此时 的转化率为20%。
的转化率为20%。 的选择性为50%。
的选择性为50%。
已知: 的选择性:
的选择性: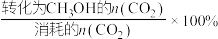
则0~10min内 的平均生成速率
的平均生成速率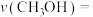
______ 。
(3)在恒容绝热条件下,下列说法能表明反应ii(不考虑反应i)达到平衡的是_______(填字母)。
Ⅱ.运用电化学原理可以很好利用资源。
(4)科学家研究出如图所示装置,可以将温室气体 转化为燃料气体CO(电解质溶液为稀硫酸)。该装置工作时,b电极的电极反应式为
转化为燃料气体CO(电解质溶液为稀硫酸)。该装置工作时,b电极的电极反应式为______________ 。导线中通过2mol电子后,a极电解质溶液的pH______ (填“增大”、“减小”或“不变”),b极电解质溶液变化的质量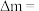
______ g 电池供电,该电池装置如下图:
电池供电,该电池装置如下图:_____________ 。
 的排放、捕集并利用
的排放、捕集并利用 是我国能源领域的一个重要战略方向。回答下列问题:
是我国能源领域的一个重要战略方向。回答下列问题:Ⅰ.在
 加氢合成甲醇的体系中,同时存在以下反应:
加氢合成甲醇的体系中,同时存在以下反应:反应ⅰ:

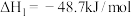
反应ⅱ:

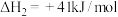
(1)反应ⅲ:
 的
的
(2)某温度下,向容积恒为1L的密闭容器中通入
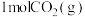 和
和 ,l0min后体系达到平衡,此时
,l0min后体系达到平衡,此时 的转化率为20%。
的转化率为20%。 的选择性为50%。
的选择性为50%。已知:
 的选择性:
的选择性: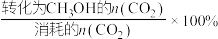
则0~10min内
 的平均生成速率
的平均生成速率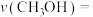
(3)在恒容绝热条件下,下列说法能表明反应ii(不考虑反应i)达到平衡的是_______(填字母)。
| A.当混合气体的压强不再改变时 |
| B.当混合气体的密度保持不变时 |
| C.断开1molH-H键的同时断开2molH-O键 |
| D.当混合气体的平均相对分子质量保持不变时 |
Ⅱ.运用电化学原理可以很好利用资源。
(4)科学家研究出如图所示装置,可以将温室气体
 转化为燃料气体CO(电解质溶液为稀硫酸)。该装置工作时,b电极的电极反应式为
转化为燃料气体CO(电解质溶液为稀硫酸)。该装置工作时,b电极的电极反应式为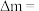

 电池供电,该电池装置如下图:
电池供电,该电池装置如下图: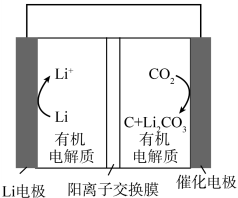
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.恒温恒容下,将2mol A气体和2mol B气体通入体积为2L的密闭容器中发生如下反应:2A(g)+B(g) xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_____ mol/(L·s)。
(2)x=____ 。
(3)下列各项可作为该反应达到平衡状态的标志的是____ 。
A.压强不再变化 B.v(A)正=2v(B)逆
C 气体密度不再变化 D.A的百分含量保持不变
E.A的消耗速率与C的消耗速率之比为2:1
Ⅱ.某鱼雷采用 Al-Ag2O 动力电池,以溶解有KOH 的流动海水为电解液,电池总反应为:2Al+3Ag2O+2KOH=6Ag+2KAlO2+H2O。试回答下列问题:
(1)Ag2O 为电池的____ 极(填“负”或“正”),负极反应式为______ 。
(2)当有 1mol电子流经外电路时,负极质量减少______ g。
(3)溶液中的 OH-向________ 极迁移(填“Ag2O”或“Al”)。
 xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。(1)从开始反应至达到平衡状态,生成C的平均反应速率为
(2)x=
(3)下列各项可作为该反应达到平衡状态的标志的是
A.压强不再变化 B.v(A)正=2v(B)逆
C 气体密度不再变化 D.A的百分含量保持不变
E.A的消耗速率与C的消耗速率之比为2:1
Ⅱ.某鱼雷采用 Al-Ag2O 动力电池,以溶解有KOH 的流动海水为电解液,电池总反应为:2Al+3Ag2O+2KOH=6Ag+2KAlO2+H2O。试回答下列问题:
(1)Ag2O 为电池的
(2)当有 1mol电子流经外电路时,负极质量减少
(3)溶液中的 OH-向
您最近一年使用:0次
【推荐3】830 K时,在1L密闭容器中发生下列可逆反应:CO(g)+H2O(g) CO2(g)+H2(g)ΔH=—40 kJ•mol-1,回答下列问题:
CO2(g)+H2(g)ΔH=—40 kJ•mol-1,回答下列问题:
(1)若起始时,c(CO)=2 mol/L,c(H2O)=3 mol/L,4 s后达到平衡,此时CO的转化率为60%,则:
①在该温度下,该反应的平衡常数K=_______ 。
②用H2O表示的化学反应速率为_______ 。
③达平衡时此反应放出热量为_______ kJ。
(2)在相同温度下,若起始时c(CO)=1 mol/L,c(H2O)=2 mol/L,反应进行一段时间后,测得H2的浓度为0.5 mol/L,则此时该反应是否达到平衡状态:_______ (填“是”或“否”),此时v(正)_______ (填“大于”“小于”或“等于”)v(逆)。
 CO2(g)+H2(g)ΔH=—40 kJ•mol-1,回答下列问题:
CO2(g)+H2(g)ΔH=—40 kJ•mol-1,回答下列问题:(1)若起始时,c(CO)=2 mol/L,c(H2O)=3 mol/L,4 s后达到平衡,此时CO的转化率为60%,则:
①在该温度下,该反应的平衡常数K=
②用H2O表示的化学反应速率为
③达平衡时此反应放出热量为
(2)在相同温度下,若起始时c(CO)=1 mol/L,c(H2O)=2 mol/L,反应进行一段时间后,测得H2的浓度为0.5 mol/L,则此时该反应是否达到平衡状态:
您最近一年使用:0次
【推荐1】碳的化合物的转换在生产、生活中具有重要的应用,如航天员呼吸产生的 用Sabatier反应处理,实现空间站中
用Sabatier反应处理,实现空间站中 的循环利用。
的循环利用。
Sabatier反应: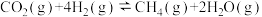 ;
;
水电解反应: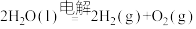 。
。
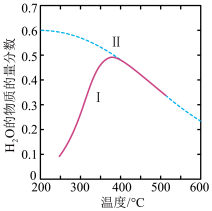
I.将原料气按 置于密闭容器中发生Sabatier反应,测得
置于密闭容器中发生Sabatier反应,测得 的物质的量分数与温度的关系如下图所示(曲线Ⅱ表示平衡曲线)。
的物质的量分数与温度的关系如下图所示(曲线Ⅱ表示平衡曲线)。
(1)在密闭恒温(高于100℃)恒容装置中进行该反应,下列能说明达到平衡状态的是_____ 。
A.混合气体密度不再改变B.混合气体压强不再改变
C.混合气体平均摩尔质量不再改变D.
(2)380℃以后曲线I与曲线Ⅱ重合并且下降的原因是_________________ 。
(3)200℃达到平衡时体系的总压强为p,该反应平衡常数 的计算表达式为
的计算表达式为_____ 。(不必化简,用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)
物质的量分数)
(4)Sabatier反应在空间站运行时,下列措施能提高 转化率的是
转化率的是_____ (填标号)。
A.适当减压B.合理控制反应器中气体的流速
C.反应器前段加热,后段冷却D.提高原料气中 所占比例
所占比例
Ⅱ.一种新的循环利用方案是用Bosch反应代替Sabatier反应。Bosch反应中 和
和 生成了C和
生成了C和 。
。
(5)①已知 、
、 的生成焓分别为
的生成焓分别为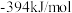 、
、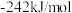 ,Bosch反应的热化学方程式为
,Bosch反应的热化学方程式为_________________ 。(生成焓指一定条件下由对应单质生成1mol化合物时的反应热)
(6)一定条件下,若无催化剂Bosch反应必须在高温下才能启动,而使用催化剂,则在较低温度下就能启动,试分析原因是_________________ 。
(7)Bosch反应的优点是_________________ 。
 用Sabatier反应处理,实现空间站中
用Sabatier反应处理,实现空间站中 的循环利用。
的循环利用。Sabatier反应:
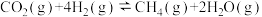 ;
;水电解反应:
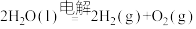 。
。I.将原料气按
 置于密闭容器中发生Sabatier反应,测得
置于密闭容器中发生Sabatier反应,测得 的物质的量分数与温度的关系如下图所示(曲线Ⅱ表示平衡曲线)。
的物质的量分数与温度的关系如下图所示(曲线Ⅱ表示平衡曲线)。
(1)在密闭恒温(高于100℃)恒容装置中进行该反应,下列能说明达到平衡状态的是
A.混合气体密度不再改变B.混合气体压强不再改变
C.混合气体平均摩尔质量不再改变D.

(2)380℃以后曲线I与曲线Ⅱ重合并且下降的原因是
(3)200℃达到平衡时体系的总压强为p,该反应平衡常数
 的计算表达式为
的计算表达式为 总压
总压 物质的量分数)
物质的量分数)(4)Sabatier反应在空间站运行时,下列措施能提高
 转化率的是
转化率的是A.适当减压B.合理控制反应器中气体的流速
C.反应器前段加热,后段冷却D.提高原料气中
 所占比例
所占比例Ⅱ.一种新的循环利用方案是用Bosch反应代替Sabatier反应。Bosch反应中
 和
和 生成了C和
生成了C和 。
。(5)①已知
 、
、 的生成焓分别为
的生成焓分别为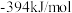 、
、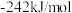 ,Bosch反应的热化学方程式为
,Bosch反应的热化学方程式为(6)一定条件下,若无催化剂Bosch反应必须在高温下才能启动,而使用催化剂,则在较低温度下就能启动,试分析原因是
(7)Bosch反应的优点是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

①该反应是____ 反应(填“吸热”、“放热”)。
②当反应达到平衡时,升高温度,A的转化率___ (填“增大”、“减小”、“不变”),原因是____ 。
③反应体系中加入催化剂对反应热是否有影响?____ (填“有”、“无”),原因是____ 。
④在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1____ ,E2____ (填“增大”、“减小”、“不变”)。
(2)已知由氢气和氧气反应生成1 mol水蒸气,放出241.8kJ热量。
①写出该反应的热化学方程式___ 。
②若1g水蒸气转化成液态水放热2.494kJ,则反应H2(g)+1/2O2(g)=H2O(l)的ΔH=_ kJ·mol-1。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
①该反应是
②当反应达到平衡时,升高温度,A的转化率
③反应体系中加入催化剂对反应热是否有影响?
④在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
(2)已知由氢气和氧气反应生成1 mol水蒸气,放出241.8kJ热量。
①写出该反应的热化学方程式
②若1g水蒸气转化成液态水放热2.494kJ,则反应H2(g)+1/2O2(g)=H2O(l)的ΔH=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成 和
和 。其化学方程式如下:
。其化学方程式如下: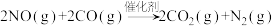 。为了测定在催化剂甲作用下的反应速率,在t℃时用气体传感器测得不同时间的NO和CO浓度如表:
。为了测定在催化剂甲作用下的反应速率,在t℃时用气体传感器测得不同时间的NO和CO浓度如表:
请回答以下各题,均不考虑温度变化对催化效率的影响:
(1)求2s内的平均反应速率
_______ 。
(2)写出该反应的平衡常数表达式_______ ,并计算该温度下的反应平衡常数K_______ 。
(3)假设在某密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是_______ 。
a.选用更有效的催化剂 b.升高反应体系的温度
c.缩小容器的体积 d.降低反应体系的温度
(4)研究表明:在使用等质量催化剂时,增大催化剂表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
①请在空格中填入剩余的实验条件数据_______ 。
②请在给出的坐标图中,画出上表中Ⅱ和Ⅲ条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明曲线的实验编号_______ 。

 和
和 。其化学方程式如下:
。其化学方程式如下: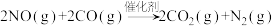 。为了测定在催化剂甲作用下的反应速率,在t℃时用气体传感器测得不同时间的NO和CO浓度如表:
。为了测定在催化剂甲作用下的反应速率,在t℃时用气体传感器测得不同时间的NO和CO浓度如表:| 时间/s | 0 | 2 | 4 | 5 |
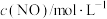 | 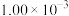 | 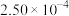 |  |  |
 | 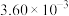 | 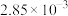 | 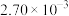 | 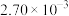 |
(1)求2s内的平均反应速率

(2)写出该反应的平衡常数表达式
(3)假设在某密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
a.选用更有效的催化剂 b.升高反应体系的温度
c.缩小容器的体积 d.降低反应体系的温度
(4)研究表明:在使用等质量催化剂时,增大催化剂表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验编号 | T/℃ | NO初始浓度 | CO初始浓度 | 催化剂的比表面积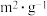 |
| Ⅰ | 280 |  |  | 82 |
| Ⅱ |  |  | 124 | |
| Ⅲ | 350 |  |  | 124 |
②请在给出的坐标图中,画出上表中Ⅱ和Ⅲ条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明曲线的实验编号

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】按要求回答问题:
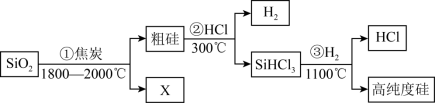
(1)由SiO2制备高纯度硅的工业流程如图所示:
①写出SiO2转化为Si(粗)的化学方程式:____________________________________________ 。
②可以循环使用的物质为_________________________ 。
(2)为了有效实现NO和NO2的相互转化,设计如图实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。
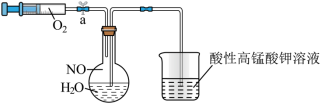
①打开止水夹,推动针筒活塞,使氧气进入烧瓶,首先观察到烧瓶中的现象是____________ ,产生此现象的化学方程式为______________________________________________ 。
②关上止水夹,轻轻摇动烧瓶,写出发生的化学方程式________________________________ 。
(3)以 Fe 和 Cu 为电极,稀 H2SO4 为电解质溶液形成的原电池中:
①H+向________ 极移动(填“正”或“负”)。
②若有 1 mol e- 流过导线,则理论上负极质量减少________ g。
③若将稀硫酸换成浓硝酸,正极电极方程式为:______________________ 。
(1)由SiO2制备高纯度硅的工业流程如图所示:

①写出SiO2转化为Si(粗)的化学方程式:
②可以循环使用的物质为
(2)为了有效实现NO和NO2的相互转化,设计如图实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。

①打开止水夹,推动针筒活塞,使氧气进入烧瓶,首先观察到烧瓶中的现象是
②关上止水夹,轻轻摇动烧瓶,写出发生的化学方程式
(3)以 Fe 和 Cu 为电极,稀 H2SO4 为电解质溶液形成的原电池中:
①H+向
②若有 1 mol e- 流过导线,则理论上负极质量减少
③若将稀硫酸换成浓硝酸,正极电极方程式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】能源、材料和污染已成为当今科学研究的热点。请回答下列问题:
(1)Fe3O4又称磁性氧化铁,可作还原剂。配平下列化学方程式,并标出电子转移的方向与数目___ 。
________K2Cr2O7+________Fe3O4+________H2SO4→________Cr2(SO4)3+________Fe2(SO4)3+________K2SO4+________H2O
(2)新型铝—氧电池用于潜水艇动力源,其原理可以看作铝在强碱溶液中发生吸氧腐蚀。铝氧电池在使用过程中,铝电极发生___ 反应(填“氧化”“还原”),写出反应后铝元素的存在形式___ (写微粒符号)。
(3)二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要,完成下列填空:
①方法一:活性炭法2C(s)+2SO2(g) S2(g)+2CO2(g)
S2(g)+2CO2(g)
上述反应的化学平衡常数表达式为___ ;若在2L的密闭容器中进行上述反应,5min时容器中气体质量增加24g,则SO2的反应速率为___ ;为了加快吸收SO2,可采取的措施有___ 。
②方法二:氨水脱硫法该法采用喷雾吸收法,雾化的氨水与烟气中的SO2直接接触吸收,一定温度下,往0.1mol/L氨水中加入少量NH4Cl固体,下列数值变小的是___
A. B.c(NH3·H2O) C.
B.c(NH3·H2O) C.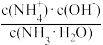 D.c(NH
D.c(NH )
)
③方法三:钠碱循环法
第一步是用Na2SO3水溶液吸收SO2,得到酸性的NaHSO3溶液;
第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。
则在NaHSO3溶液中离子浓度关系正确的是___ 。
A.c(Na+)>c(HSO )>c(H+)>c(SO
)>c(H+)>c(SO )>c(OH-)
)>c(OH-)
B.c(Na+)=2c(SO )+c(HSO
)+c(HSO )
)
C.c(H2SO3)+c(H+)=c(SO )+c(OH-)
)+c(OH-)
D.c(Na+)+c(H+)=c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
(1)Fe3O4又称磁性氧化铁,可作还原剂。配平下列化学方程式,并标出电子转移的方向与数目
________K2Cr2O7+________Fe3O4+________H2SO4→________Cr2(SO4)3+________Fe2(SO4)3+________K2SO4+________H2O
(2)新型铝—氧电池用于潜水艇动力源,其原理可以看作铝在强碱溶液中发生吸氧腐蚀。铝氧电池在使用过程中,铝电极发生
(3)二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要,完成下列填空:
①方法一:活性炭法2C(s)+2SO2(g)
 S2(g)+2CO2(g)
S2(g)+2CO2(g)上述反应的化学平衡常数表达式为
②方法二:氨水脱硫法该法采用喷雾吸收法,雾化的氨水与烟气中的SO2直接接触吸收,一定温度下,往0.1mol/L氨水中加入少量NH4Cl固体,下列数值变小的是
A.
 B.c(NH3·H2O) C.
B.c(NH3·H2O) C.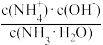 D.c(NH
D.c(NH )
)③方法三:钠碱循环法
第一步是用Na2SO3水溶液吸收SO2,得到酸性的NaHSO3溶液;
第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。
则在NaHSO3溶液中离子浓度关系正确的是
A.c(Na+)>c(HSO
 )>c(H+)>c(SO
)>c(H+)>c(SO )>c(OH-)
)>c(OH-)B.c(Na+)=2c(SO
 )+c(HSO
)+c(HSO )
)C.c(H2SO3)+c(H+)=c(SO
 )+c(OH-)
)+c(OH-)D.c(Na+)+c(H+)=c(SO
 )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】下图A、B、C三个烧杯中分别盛有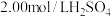 溶液,D中烧杯内盛有
溶液,D中烧杯内盛有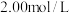 的
的 溶液。
溶液。
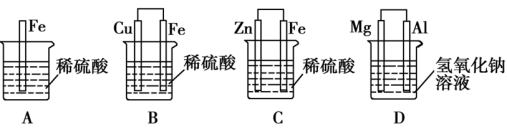
(1)A中反应的离子方程式是_______ 。
(2)B中Cu极属于原电池中的_______ (填“正”或“负”)极;Fe极附近溶液呈_______ 色。
(3)C中被腐蚀的金属是_______ (填化学式),A、B、C中铁被腐蚀的速率,由快到慢的顺序是_______ (用“>”表示)。
(4)写出D中总反应的离子方程式:_______ ,D中铝极发生_______ (填“氧化”或“还原”)反应。
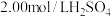 溶液,D中烧杯内盛有
溶液,D中烧杯内盛有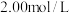 的
的 溶液。
溶液。
(1)A中反应的离子方程式是
(2)B中Cu极属于原电池中的
(3)C中被腐蚀的金属是
(4)写出D中总反应的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2L密闭容器内,400°C时发生反应:CO(g)+2H2(g) CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
(1)图中表示CH3OH的物质的量浓度变化的曲线是_______ (填字母)。
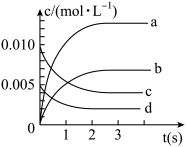
(2)用H2表示从0~2s内该反应的平均速率v(H2)_______ 。随着反应的进行,该反应的速率逐渐减慢的原因是_______ 。
(3)该反应是一个放热反应,说明该反应中破坏1molCO和2molH2的化学键吸收的能量_______ 形成lmolCH3OH释放的能量(填“<”、“=”或“>”)。
(4)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2 +6H2O则电池放电时通入空气的电极为
+6H2O则电池放电时通入空气的电极为_______ (“正”或“负”)极;该电池负极的电极反应式是_______ 从电极反应式来看,每消耗1molCH3OH转移_______ mol电子。
(5)若已知:在CO2加氢合成CH3OH的体系中,同时发生以下反应:
反应i:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应ii:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
某温度下,向容积为1L的密闭容器中通入1molCO2(g)和5molH2(g),10min后体系达到平衡,此时H2的转化率为8%,CH3OH的选择性为50%。(已知:CH3OH的选择性=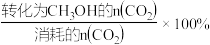 ),则平衡时气体的总物质的量是
),则平衡时气体的总物质的量是_______ mol。
 CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CH3OH)(mol) | 0 | 0.009 | 0.012 | 0.013 | 0.013 |
(1)图中表示CH3OH的物质的量浓度变化的曲线是

(2)用H2表示从0~2s内该反应的平均速率v(H2)
(3)该反应是一个放热反应,说明该反应中破坏1molCO和2molH2的化学键吸收的能量
(4)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2
 +6H2O则电池放电时通入空气的电极为
+6H2O则电池放电时通入空气的电极为(5)若已知:在CO2加氢合成CH3OH的体系中,同时发生以下反应:
反应i:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)反应ii:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)某温度下,向容积为1L的密闭容器中通入1molCO2(g)和5molH2(g),10min后体系达到平衡,此时H2的转化率为8%,CH3OH的选择性为50%。(已知:CH3OH的选择性=
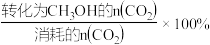 ),则平衡时气体的总物质的量是
),则平衡时气体的总物质的量是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)已知键能H-H 436kJ/mol,N-H391kJ/mol,N≡N946 kJ/mol。则N2(g)+3H2(g) 2NH3(g)生成1molNH3
2NH3(g)生成1molNH3___________ (填吸收或放出)___________ kJ热量。
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
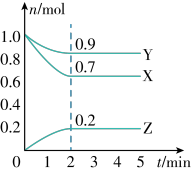
①该反应的化学方程式为___________ 。反应开始至2min,以气体Z表示的平均反应速率为___________ 。平衡时X的转化率为___________ 。
② 2min反应达到平衡,容器内混合气体的平均相对分子质量比起始时___________  填“大”、“小”或“相等”,下同
填“大”、“小”或“相等”,下同 ,混合气体密度比起始时
,混合气体密度比起始时___________ 。
(3)如图所示。

①甲中SO 移向
移向___________ (填“铝片”或“镁片”),转移电子0.5mol时,正极产生气体标况下的体积为___________ 。
②乙中负极为___________ (填“铝片”或“镁片”)写出其电极反应式式:___________ 。
(1)已知键能H-H 436kJ/mol,N-H391kJ/mol,N≡N946 kJ/mol。则N2(g)+3H2(g)
 2NH3(g)生成1molNH3
2NH3(g)生成1molNH3(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为
② 2min反应达到平衡,容器内混合气体的平均相对分子质量比起始时
 填“大”、“小”或“相等”,下同
填“大”、“小”或“相等”,下同 ,混合气体密度比起始时
,混合气体密度比起始时(3)如图所示。

①甲中SO
 移向
移向②乙中负极为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】二甲醚具有优良的燃烧性能,被称为21世纪的“清洁能源”,以下为其中一种合成二甲醚的方法:在一定温度、压强和催化剂作用下,在同一反应器中进行如下反应:
①CO2(g)+3H2(g) CH3OH(g) +H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g) +H2O(g) △H1=-49.1 kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) △H3=+ 41.2 kJ·mol-1
CO(g)+H2O(g) △H3=+ 41.2 kJ·mol-1
(1)写出CO2(g)加H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式是_______ 。
(2)一定条件下,原料气中n(H2)/n(CO2)比值和温度对CO2转化率影响的实验数据如下图。

①温度为T1 K时,在1 L反应容器中投入2mol CO2 和8mol H2进行反应,试计算达到平衡时CO2的浓度为_______________________ 。
②结合数据图,归纳CO2平衡转化率受外界条件影响的变化规律:
a________________________________________________________________________ 。
b________________________________________________________________________ 。
(3)为研究初始投料比与二甲醚产率关系,在一定温度和压强下,投入一定物质的量的H2、CO、CO2进行试验,实验发现二甲醚的平衡产率随原料气中n(CO)/〔n(CO)+n(CO2)〕比值增大而增大,试分析其原因________________ 。
(4)下图是科学家现正研发的,以实现反应①在常温常压下进行的装置。
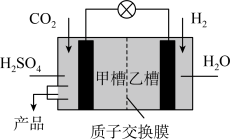
写出甲槽的电极反应_____________________________________ 。
①CO2(g)+3H2(g)
 CH3OH(g) +H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g) +H2O(g) △H1=-49.1 kJ·mol-1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+ 41.2 kJ·mol-1
CO(g)+H2O(g) △H3=+ 41.2 kJ·mol-1(1)写出CO2(g)加H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式是
(2)一定条件下,原料气中n(H2)/n(CO2)比值和温度对CO2转化率影响的实验数据如下图。

①温度为T1 K时,在1 L反应容器中投入2mol CO2 和8mol H2进行反应,试计算达到平衡时CO2的浓度为
②结合数据图,归纳CO2平衡转化率受外界条件影响的变化规律:
a
b
(3)为研究初始投料比与二甲醚产率关系,在一定温度和压强下,投入一定物质的量的H2、CO、CO2进行试验,实验发现二甲醚的平衡产率随原料气中n(CO)/〔n(CO)+n(CO2)〕比值增大而增大,试分析其原因
(4)下图是科学家现正研发的,以实现反应①在常温常压下进行的装置。

写出甲槽的电极反应
您最近一年使用:0次



