化学能可以与热能、电能等相互转化,下列说法正确的是
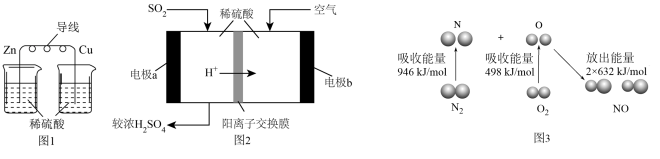

| A.图1:能将化学能转化为电能 |
| B.图2:电极b为负极,发生氧化反应 |
| C.图2:当电路中转移1mol电子时,电极上消耗的n(SO2):n(O2)=2:1 |
| D.图3:1 mol N2 (g)和1mol O2 (g)完全反应生成2mol NO(g)的过程中放出180kJ能量 |
更新时间:2023-06-14 15:12:28
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】2mol金属钠和1 mol氯气反应的能量关系如图所示,下列说法不正确的是
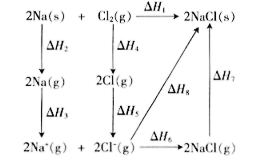

A. |
B.在相同条件下,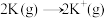 的△H3' 的△H3'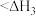 |
C. |
D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】肼(N2H4)通常为液态,可用作火箭发射的燃料,其燃烧过程的能量变化如图所示。下列说法正确的是

| A.热化学方程式为N2H4+O2=N2+2H2O △H=(E1-E2) kJ/mol |
| B.反应中断裂化学键吸收的总能量大于形成化学键释放的总能量 |
| C.肼的燃烧热△H=-(E2-E1) kJ/mol |
| D.其他条件均相同,若反应生成液态水,放出的能量大于(E2-E1) kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】甲醇是重要的化工原料,工业上由CO、 和
和 合成甲醇的主要反应如下:
合成甲醇的主要反应如下:
I.

II.

III.

已知:反应Ⅲ中相关化学键的数据如下表
则 键的键能a为
键的键能a为
 和
和 合成甲醇的主要反应如下:
合成甲醇的主要反应如下:I.


II.


III.


已知:反应Ⅲ中相关化学键的数据如下表
| 化学键 |  |  |  |  |  |
键能/ | 436 | 343 | a | 465 | 413 |
 键的键能a为
键的键能a为| A.1076 | B.826 | C.779 | D.538 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列叙述正确的是
| A.电解MgCl2溶液得到金属Mg |
B.一定温度下,反应CH3Cl(g)+Cl2(g) CH2Cl2(l)+HCl(g)能自发进行,该反应的ΔH>0 CH2Cl2(l)+HCl(g)能自发进行,该反应的ΔH>0 |
| C.氢氧燃料电池正极消耗5.6L气体时,电路中通过的电子数为6.02×1023 |
D.反应 的ΔH可通过下式计算:用E表示键能,该反应ΔH = 4E(Si−Cl)+2E(H−H)−2E(Si−Si)−4E(H−Cl) 的ΔH可通过下式计算:用E表示键能,该反应ΔH = 4E(Si−Cl)+2E(H−H)−2E(Si−Si)−4E(H−Cl) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】以NaCl为原料,可制取Na、Na2O2、NaOH和Na2CO3等。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:
(1)N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ•mol-1
2NH3(g) ΔH=-92.4kJ•mol-1
(2)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
(3)2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
下列有关比较正确的是
(1)N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4kJ•mol-1
2NH3(g) ΔH=-92.4kJ•mol-1(2)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
(3)2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O下列有关比较正确的是
| A.键能(E):6E(N−H)>E(N≡N)+3E(H−H) | B.热稳定性:NaHCO3>Na2CO3 |
| C.同浓度溶液的pH:NaHCO3>Na2CO3 | D.沸点:NH3>H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列关于下图所示原电池装置的叙述不正确的是
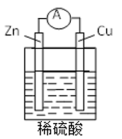

| A.铜片是正极 | B.锌片质量逐渐减少 |
| C.氢离子在铜片表面被氧化 | D.电子从锌片经导线流向铜片 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】关于如图所示装置(假设溶液体积不变),下列叙述正确的是
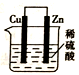

| A.烧杯内溶液中阳离子的物质的量浓度总和逐渐减小 | B.反应一段时间后,溶液逐渐变为蓝色 |
| C.逐渐溶解的一极上发生还原反应 | D.电子从产生大量气泡的一极流出 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】碱性电池具有容量大.放电电流大的特点,因而得到广泛应用。碱性锌锰电池以氢氧化钾溶液为电解液,电池反应方程式为:
Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法中错误的是
Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法中错误的是
| A.电池工作时,电子由正极通过外电路流向负极 |
| B.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq) |
| C.电池工作时,锌失去电子 |
| D.外电路中每通过0.2 mol电子,锌的质量减少6.5 g |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池正极上发生还原反应 |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
您最近一年使用:0次




