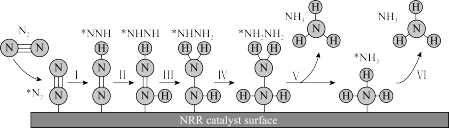
N2+3H2 2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
 2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是| A.增加NH3的浓度不影响反应速率 |
| B.升高体系温度能加快反应速率 |
| C.使用催化剂不影响反应速率 |
| D.若反应在密闭容器中进行,N2和H2的转化率能达到100% |
更新时间:2023-05-15 22:18:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在水溶液中进行的反应: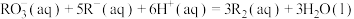 ,已知该反应速率方程为
,已知该反应速率方程为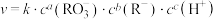 (k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
(k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
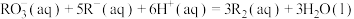 ,已知该反应速率方程为
,已知该反应速率方程为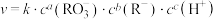 (k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
(k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是实验编号 相关数据 | ① | ② | ③ | ④ | ⑤ |
 | 0.008 | 0.008 | 0.004 | 0.008 | 0.008 |
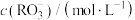 | 0.001 | 0.001 | 0.001 | 0.002 | 0.001 |
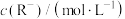 | 0.10 | 0.20 | 0.20 | 0.10 | 0.40 |
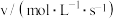 | 2.4×10-8 | 4.8×10-8 | 1.2×10-8 | 4.8×10-8 | v1 |
| A.反应体系的三种物质中,R-(aq)的浓度对反应速率影响最大 |
B.速率常数 的数值为3.75 的数值为3.75 |
| C.a、b、c的值分别为2、1、2 |
| D.实验⑤中,v1=4.8×10-8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列情况中反应速率不加快 的是
| A.将在空气中燃着的木条插入盛有纯氧的集气瓶中 |
| B.用煤粉代替煤块燃烧 |
C.增大合成氨反应(N2+3H2 2NH3)体系的压强 2NH3)体系的压强 |
| D.用0.01 mol·L-1的盐酸代替1 mol·L-1的盐酸与铁反应制取氢气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验方案设计、现象和结论不正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取10mL0.lmol/LNa2S2O3溶液和5mL0.1mol/LNa2S2O3溶液、5mL蒸馏水于两支试管中,然后同时加入10mL0.1mol/LH2SO4溶液 | 前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 在容积不变的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g)向其中通入氩气 2NH3(g)向其中通入氩气 | 反应速率不变,说明化学反应速率不受压强影响 |
| C | 探究温度对化学平衡的影响 | 将装有NO2和N2O4混合气体的连同球分别浸泡在冰水和热水中:2NO2(g)(红棕色) N2O4(g)(无色),△H<0 N2O4(g)(无色),△H<0 | 热水中气体颜色深,冰水中颜色浅,说明其他条件不变时,升高温度,会使化学平衡向吸热方向移动 |
| D | 探究KI与FeCl3反应的限度 | 取5mL0.1mol/L的KI溶液于试管中,加入1mL0.1mol/L的FeCl3溶液,充分反应后滴入5滴15%KSCN溶液 | 溶液变血红色,则KI与FeCl3的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
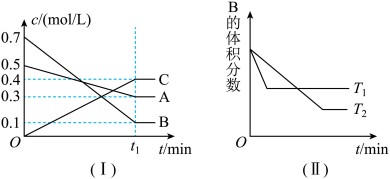
【推荐2】T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为 和
和 时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
 和
和 时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
A. 和 和 温度下分别对应的平衡常数 温度下分别对应的平衡常数 和 和 的关系是: 的关系是: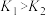 |
B.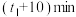 时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 |
C.T℃时,在相同容器中,若由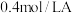 、 、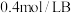 和 和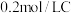 反应,达到平衡后,C的浓度仍为 反应,达到平衡后,C的浓度仍为 |
| D.其他条件不变,升高温度,正、逆反应速率均增大,A的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在2020年第七十五届联合国大会上,我国向世界郑重承诺努力争取在2060年前实现碳中和.将 与甲醇直接合成碳酸二甲酯,不仅能有效减少
与甲醇直接合成碳酸二甲酯,不仅能有效减少 的排放,还可以得到重要有机中间体碳酸二甲酯.一种利用含铈
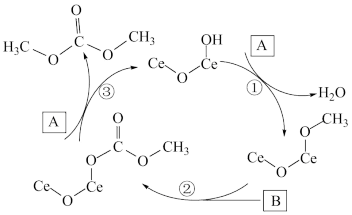
的排放,还可以得到重要有机中间体碳酸二甲酯.一种利用含铈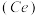 催化剂实现该反应的催化循环原理如下图所示,有关说法正确的是
催化剂实现该反应的催化循环原理如下图所示,有关说法正确的是
 与甲醇直接合成碳酸二甲酯,不仅能有效减少
与甲醇直接合成碳酸二甲酯,不仅能有效减少 的排放,还可以得到重要有机中间体碳酸二甲酯.一种利用含铈
的排放,还可以得到重要有机中间体碳酸二甲酯.一种利用含铈 催化剂实现该反应的催化循环原理如下图所示,有关说法正确的是
催化剂实现该反应的催化循环原理如下图所示,有关说法正确的是
A.物质B为 | B.总反应式为 |
| C.反应②的类型为取代反应 | D.反应过程中Ce的化合价发生了变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列对各个图象的描述正确的是
A.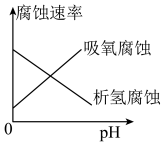 表示析氢腐蚀、吸氧腐蚀速率与金属周围溶液pH的关系 表示析氢腐蚀、吸氧腐蚀速率与金属周围溶液pH的关系 |
B.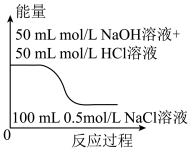 表示物质能量的大小关系 表示物质能量的大小关系 |
C.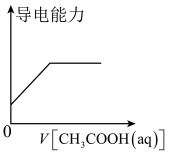 表示在氨水中加入同浓度的醋酸溶液时导电能力变化的情况 表示在氨水中加入同浓度的醋酸溶液时导电能力变化的情况 |
D.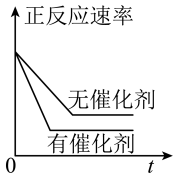 表示有无催化剂情况下正反应速率随时间变化的情况 表示有无催化剂情况下正反应速率随时间变化的情况 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 中含有 中含有 个阳离子 个阳离子 |
B. 乙烷和丙烯的混合气体中所含碳氢键数为 乙烷和丙烯的混合气体中所含碳氢键数为 |
C. 含有中子数为 含有中子数为 |
D. 和 和 于密闭容器中充分反应后, 于密闭容器中充分反应后, 分子总数为 分子总数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设 为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:
为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:
①
②
③
已知:H、Si的电负性依次为2.1、1.8.下列有关说法正确的是
 为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:
为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:①

②

③

已知:H、Si的电负性依次为2.1、1.8.下列有关说法正确的是
A.①中,30g氧化剂含极性键数目为 | B.②中,生成1g 时转移电子数为 时转移电子数为 |
| C.②和③互为可逆反应 | D.②和③的目的是除去粗硅中的杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】根据实验操作和现象,所得到的结论错误的是
| 选项 | 实验操作和现象 | 结论 |
| A | 相同温度下,用pH传感器测定SO2和CO2饱和溶液的pH,后者pH大 | 酸性: |
| B | 向5 mLFeCl3溶液中滴加10 mL等浓度的KI溶液,充分反应后,再滴加KSCN溶液,溶液最终变为血红色 | FeCl3溶液与KI溶液的反应为可逆反应 |
| C | 取两支试管,分别加入2 mL0.2 mol/L的酸性KMnO4溶液,然后分别向两支试管中加入2 mL0.6 mol/L和1.2 mol/L的H2C2O4溶液,后者完全褪色所需时间更短 | 其他条件相同时,增大反应物浓度反应速率增大 |
| D | 向K2Cr2O7溶液中滴加AgNO3溶液,有砖红色沉淀(Ag2CrO4)生成 | Ag2CrO4溶解度比Ag2Cr2O7小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 ,溶液中
,溶液中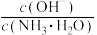 增大
增大
 溶液滴定未知浓度的盐酸,滴定终点读数时俯视,所测结果偏高
溶液滴定未知浓度的盐酸,滴定终点读数时俯视,所测结果偏高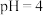 的
的 溶液与
溶液与 的
的 溶液中,前者水的电离程度大
溶液中,前者水的电离程度大 3Z(g) ΔH=-a kJ·molˉ1 (a>0),下列说法正确的是
3Z(g) ΔH=-a kJ·molˉ1 (a>0),下列说法正确的是