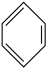
下列说法中正确的是
A.价层电子排布为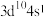 的原子位于第四周期第ⅠA族,属于s区元素 的原子位于第四周期第ⅠA族,属于s区元素 |
B. 为极性分子, 为极性分子, 为非极性分子 为非极性分子 |
C.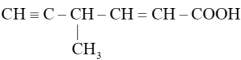 分子中含有2个手性碳原子 分子中含有2个手性碳原子 |
D. 和的中心原 和的中心原 子均为 子均为 杂化, 杂化, 分子呈正四面体形, 分子呈正四面体形, 呈三角锥形 呈三角锥形 |
更新时间:2023-05-23 18:23:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某浅海沉积岩矿物的化学式为X2YZ4W,X、Y、Z、W四种元素为不同主族前20号元素且原子半径依次减小,仅Z、W位于同周期,X、Y的第一电离能均高于同周期相邻主族元素,原子序数满足X+Y+Z+W=52。下列说法错误的是
| A.电负性:X<Y<Z<W |
| B.简单氢化物的沸点:Z>W>Y |
| C.YW3的空间结构为平面三角形 |
| D.XZ2中含有共价键和离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列化学用语表述正确的是
A.基态 的电子排布式: 的电子排布式: | B. 的球棍模型: 的球棍模型: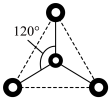 |
C. 分子间的氢键: 分子间的氢键: | D. 键电子云轮廓图: 键电子云轮廓图: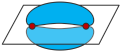 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
A.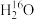 和 和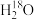 互为同位素 互为同位素 |
B.1molNa2O2中含有的阴离子数目约为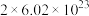 |
C. 和 和 的中心原子杂化方式均为sp3 的中心原子杂化方式均为sp3 |
| D.SeO2属于共价晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列描述中正确的是
A. 的空间构型为三角锥形 的空间构型为三角锥形 |
B. 和 和 的中心原子均为 的中心原子均为 杂化 杂化 |
| C.在所有的元素中,氟的第一电离能最大 |
D. 分子中共含有8个极性键,1个π键 分子中共含有8个极性键,1个π键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】B3N3H6因结构与苯相似而被称为无机苯,其分子结构如图,下列关于B3N3H6的说法不正确 的是
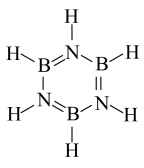

| A.它的分子中所有原子都在同一平面内 |
| B.它的分子中B与N均为sp2杂化 |
| C.它既有σ键又有π键 |
| D.它是极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法不正确的是
A.某粒子空间构型为正四面体,则键角一定是 |
B.某粒子空间构型为平面三角形,则中心原子一定是 杂化 杂化 |
| C.某粒子空间构型为V形,则中心原子一定有孤电子对 |
| D.某分子空间构型为三角锥形,则该粒子一定是极性分子 |
您最近一年使用:0次

 中,阴离子立体构型为平面三角形,C原子的杂化方式为
中,阴离子立体构型为平面三角形,C原子的杂化方式为