将12.0g铜粉缓慢加入到50.0mL某浓度的浓硝酸中,随反应的进行,产生的 和NO总体积(折算成标准状况)随铜粉加入量的变化如图。完成下列问题:
和NO总体积(折算成标准状况)随铜粉加入量的变化如图。完成下列问题:___________ mol。
(2)反应中生成的 和NO的体积之比为
和NO的体积之比为___________ 。
(3)原硝酸的物质的量浓度为___________  。
。
(4)若使铜粉继续溶解,可向反应后的溶液中加入___________。
 和NO总体积(折算成标准状况)随铜粉加入量的变化如图。完成下列问题:
和NO总体积(折算成标准状况)随铜粉加入量的变化如图。完成下列问题: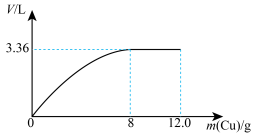
(2)反应中生成的
 和NO的体积之比为
和NO的体积之比为(3)原硝酸的物质的量浓度为
 。
。(4)若使铜粉继续溶解,可向反应后的溶液中加入___________。
| A.稀硫酸 | B. 固体 固体 |
C. 固体 固体 | D. 固体 固体 |
22-23高一下·河北唐山·期末 查看更多[3]
河北省唐山市2022-2023学年高一下学期期末考试化学试题(已下线)合格考汇编9物质的量(已下线)重难点01 浓硫酸、浓硝酸的性质与反应计算-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
更新时间:2023-07-16 17:15:11
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】根据所学知识填空:
(1)2molH2O含有___ 个H2O;
(2)6.02×1023个CO2中,有___ molO;
(3)1.5molNH3的质量为___ ,有___ 个NH3分子;
(4)49gH2SO4约含有___ 个H,O原子的物质的量为___ 。
(1)2molH2O含有
(2)6.02×1023个CO2中,有
(3)1.5molNH3的质量为
(4)49gH2SO4约含有
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】有关物质的量浓度的计算
(1)计算的基本公式:c=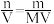 。
。
(2)计算的基本类型和方法:
①已知溶质的质量
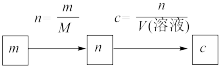
②已知溶液中某种粒子的数目
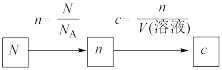
③标准状况下,气体溶质的物质的量浓度的计算
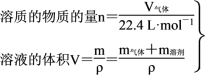 c=
c=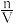
(3)注意:
①物质加入水中,注意溶质的判断。如SO3 H2SO4,Na2O或Na2O2
H2SO4,Na2O或Na2O2 NaOH,Na
NaOH,Na NaOH,NH3
NaOH,NH3 NH3·H2O等。
NH3·H2O等。
②溶液浓度与离子浓度的定量关系要注意电离程度与组成。
如0.1 mol·L-1的K2SO4溶液中c(K+)=0.2 mol·L-1。
(4)物质的量浓度与溶质的质量分数的换算
①换算公式:cB=_______ mol·L-1.M:溶质B的摩尔质量 ρ:溶液密度(g·mL-1)。
②推导方法:设溶液体积为1 L,则cB=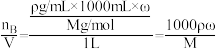 mol·L-1。
mol·L-1。
(5)溶液稀释和混合的计算
①溶液稀释的有关计算:稀释前后溶质的物质的量和质量都保持不变。_______ 。
②溶液混合的计算:混合前后溶质的物质的量或质量不变。_______ 。
注意:无特别指明时,V(混)≠V1+V2;V(混)= ,但溶液的质量守恒:m(混)=m1+m2。
,但溶液的质量守恒:m(混)=m1+m2。
(6)常见物理量之间的换算关系
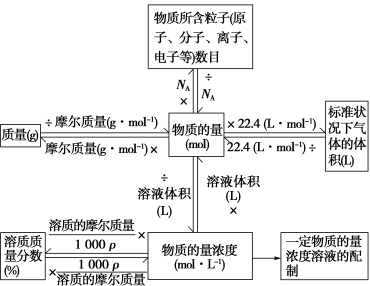
万能公式:n= =cBV
=cBV
(1)计算的基本公式:c=
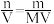 。
。(2)计算的基本类型和方法:
①已知溶质的质量

②已知溶液中某种粒子的数目
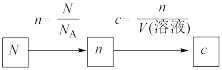
③标准状况下,气体溶质的物质的量浓度的计算
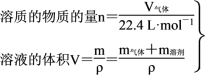 c=
c=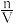
(3)注意:
①物质加入水中,注意溶质的判断。如SO3
 H2SO4,Na2O或Na2O2
H2SO4,Na2O或Na2O2 NaOH,Na
NaOH,Na NaOH,NH3
NaOH,NH3 NH3·H2O等。
NH3·H2O等。②溶液浓度与离子浓度的定量关系要注意电离程度与组成。
如0.1 mol·L-1的K2SO4溶液中c(K+)=0.2 mol·L-1。
(4)物质的量浓度与溶质的质量分数的换算
①换算公式:cB=
②推导方法:设溶液体积为1 L,则cB=
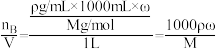 mol·L-1。
mol·L-1。(5)溶液稀释和混合的计算
①溶液稀释的有关计算:稀释前后溶质的物质的量和质量都保持不变。
②溶液混合的计算:混合前后溶质的物质的量或质量不变。
注意:无特别指明时,V(混)≠V1+V2;V(混)=
 ,但溶液的质量守恒:m(混)=m1+m2。
,但溶液的质量守恒:m(混)=m1+m2。(6)常见物理量之间的换算关系

万能公式:n=
 =cBV
=cBV
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】实验室用氯酸钾和二氧化锰制取氧气的反应方程式为:2KClO3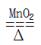 2KCl+3O2。回答下列问题:
2KCl+3O2。回答下列问题:
(1)该反应中被还原的元素名称为__ ,生成2molO2时转移电子的数是__ 。
(2)从反应后的固体混合物中分离出难溶于水的MnO2的具体实验操作名称:__ 。
(3)分离出的MnO2可用于实验室制取Cl2,化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,其离子方程式为
MnCl2+Cl2↑+2H2O,其离子方程式为___ 。
(4)若两个反应中转移的电子的物质的量相同,则生成的O2和Cl2在相同状况下的体积比为___ 。
(5)以上两个反应都用到MnO2,其作用分别___ 。
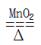 2KCl+3O2。回答下列问题:
2KCl+3O2。回答下列问题:(1)该反应中被还原的元素名称为
(2)从反应后的固体混合物中分离出难溶于水的MnO2的具体实验操作名称:
(3)分离出的MnO2可用于实验室制取Cl2,化学方程式为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,其离子方程式为
MnCl2+Cl2↑+2H2O,其离子方程式为(4)若两个反应中转移的电子的物质的量相同,则生成的O2和Cl2在相同状况下的体积比为
(5)以上两个反应都用到MnO2,其作用分别
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】物质的量是高中化学中常用的物理量,请完成以下有关其计算的内容。
(1)0.2 g H2含有___________________ 个H原子。
(2)标准状况下,含有相同氧原子数的CO与CO2的体积之比为__________ 。
(3)100 mL 某Al2(SO4)3溶液中,c(Al3+) = 2.0 mol/L,则其中c(SO42-) =_________ mol/L。
(4)工业上利用下列反应进行海水中溴元素的富集:Br2 + SO2 + 2H2O = H2SO4 + 2HBr 。若反应中生成了 0.2 mol HBr,则消耗SO2的体积(标准状况)是________________ L。
(1)0.2 g H2含有
(2)标准状况下,含有相同氧原子数的CO与CO2的体积之比为
(3)100 mL 某Al2(SO4)3溶液中,c(Al3+) = 2.0 mol/L,则其中c(SO42-) =
(4)工业上利用下列反应进行海水中溴元素的富集:Br2 + SO2 + 2H2O = H2SO4 + 2HBr 。若反应中生成了 0.2 mol HBr,则消耗SO2的体积(标准状况)是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】将硝酸表现出的性质填在下列各反应操作或现象后:
A.氧化性 B.酸性 C.还原性 D.不稳定性
(1)用硝酸浸洗附有银的试管___ 。
(2)常温下用铁制或铝制容器贮存、运输浓HNO3__ 。
(3)久置的浓硝酸变黄色__ 。
A.氧化性 B.酸性 C.还原性 D.不稳定性
(1)用硝酸浸洗附有银的试管
(2)常温下用铁制或铝制容器贮存、运输浓HNO3
(3)久置的浓硝酸变黄色
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】将1.92 g铜粉与一定量的浓硝酸反应,当铜粉完全反应时收集到气体1.12 L(标准状况下)。则所消耗硝酸的物质的量是________________ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)化合价升高的元素是___________ ,化合价降低的元素是___________ ,发生氧化反应的物质是___________ ,发生还原反应的物质是___________ 。
(2)氧化剂是___________ ,还原剂是___________ , 氧化产物是___________ ,还原产物是___________ 。
(3)HNO3表现出的性质是___________ 、___________ 。
(4)生成1个NO电子转移___________ 。
(1)化合价升高的元素是
(2)氧化剂是
(3)HNO3表现出的性质是
(4)生成1个NO电子转移
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】回答下列问题:
(1)写出俗称“钡餐”的药剂的化学式_______
(2)写出异丁烷的结构简式_______
(3)写出铜与浓硫酸反应的化学方程式_______
(4)写出用淀粉生产葡萄糖的化学方程式_______
(1)写出俗称“钡餐”的药剂的化学式
(2)写出异丁烷的结构简式
(3)写出铜与浓硫酸反应的化学方程式
(4)写出用淀粉生产葡萄糖的化学方程式
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】写出Cu与浓HNO3反应的化学方程式__ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】按要求写出下列反应的方程式:
①铝丝与稀硫酸反应的离子方程式:________ ;
②铝片与氢氧化钠溶液反应的离子方程式:_______ ;
③铜与稀硝酸反应的化学方程式:________ ;
④二氧化氮气体溶于水的化学方程式:_______ 。
①铝丝与稀硫酸反应的离子方程式:
②铝片与氢氧化钠溶液反应的离子方程式:
③铜与稀硝酸反应的化学方程式:
④二氧化氮气体溶于水的化学方程式:
您最近一年使用:0次



