高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂作剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe2+离子.配平制取铁酸钠的化学方程式:
______Fe(NO3)3+______NaOH+______Cl2═____Na2FeO4+____NaCl+6NaNO3+8H2O._______ ,反应中,______ 元素被氧化,每生成8mol H2O转移电子总数为________ 。
______Fe(NO3)3+______NaOH+______Cl2═____Na2FeO4+____NaCl+6NaNO3+8H2O.
2021高三·浙江·专题练习 查看更多[5]
(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题05 氧化还原反应 (热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)
更新时间:2021-03-16 04:05:21
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】苹果酸(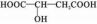 )常用做汽水、糖果的添加剂。
)常用做汽水、糖果的添加剂。
写出苹果酸分别与下列物质反应的化学方程式:
(1) Na_______ 。
(2)Na2CO3_______ 。
(3)CH3CH2OH(H2SO4,△)_______ 。
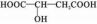 )常用做汽水、糖果的添加剂。
)常用做汽水、糖果的添加剂。写出苹果酸分别与下列物质反应的化学方程式:
(1) Na
(2)Na2CO3
(3)CH3CH2OH(H2SO4,△)
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】下列是中学阶段常见的重要化学物质:
a.氢氧化铁胶体 b.氢氧化钠 c.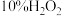 溶液 d.明矾 e.氧化铝 f.稀硫酸酸化的硫酸亚铁溶液 g.84消毒液 h.稀盐酸 i.二氧化硅 j.偏铝酸钠
溶液 d.明矾 e.氧化铝 f.稀硫酸酸化的硫酸亚铁溶液 g.84消毒液 h.稀盐酸 i.二氧化硅 j.偏铝酸钠
请完成下列各题:
(1)属于氧化物的有___________ (填序号,下同),能净水的有___________ ,属于盐的有___________ 。
(2)g的有效成分是___________ (填化学式)。
(3)向f中滴加几滴c,观察到的现象是___________ ,发生反应的离子方程式为___________ 。
(4)向d溶液中加入过量b溶液,发生反应的离子方程式为___________ 。
a.氢氧化铁胶体 b.氢氧化钠 c.
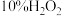 溶液 d.明矾 e.氧化铝 f.稀硫酸酸化的硫酸亚铁溶液 g.84消毒液 h.稀盐酸 i.二氧化硅 j.偏铝酸钠
溶液 d.明矾 e.氧化铝 f.稀硫酸酸化的硫酸亚铁溶液 g.84消毒液 h.稀盐酸 i.二氧化硅 j.偏铝酸钠请完成下列各题:
(1)属于氧化物的有
(2)g的有效成分是
(3)向f中滴加几滴c,观察到的现象是
(4)向d溶液中加入过量b溶液,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】I、磷、硫元素的单质和化合物应用广泛。
(1)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为: 2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10 10C+P4O10=P4+10CO
每生成1mol P4时,就有___________ mol电子发生转移。
(2)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:C6H8O6+I2=C6H6O6+2H++2I- 2 +I2=
+I2= +2I-在一定体积的某维生素C溶液中加入a mol·L-1 I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2, 消耗b mol·L-1Na2S2O3溶液V2mL。该溶液中维生素C的物质的量是
+2I-在一定体积的某维生素C溶液中加入a mol·L-1 I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2, 消耗b mol·L-1Na2S2O3溶液V2mL。该溶液中维生素C的物质的量是___________ mol。
(3)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2 +5
+5 +2H+=I2+5
+2H+=I2+5 +H2O生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
+H2O生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
该实验的目的是___________ ;表中X=___________ mL
Ⅱ、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(4)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是___________ 。
(5)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
 Ce3++
Ce3++ H2O2+
H2O2+ H2O
H2O
 Ce(OH)4↓+
Ce(OH)4↓+
___________
(1)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为: 2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10 10C+P4O10=P4+10CO
每生成1mol P4时,就有
(2)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:C6H8O6+I2=C6H6O6+2H++2I- 2
 +I2=
+I2= +2I-在一定体积的某维生素C溶液中加入a mol·L-1 I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2, 消耗b mol·L-1Na2S2O3溶液V2mL。该溶液中维生素C的物质的量是
+2I-在一定体积的某维生素C溶液中加入a mol·L-1 I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2, 消耗b mol·L-1Na2S2O3溶液V2mL。该溶液中维生素C的物质的量是(3)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2
 +5
+5 +2H+=I2+5
+2H+=I2+5 +H2O生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
+H2O生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示: | 0.01mol·L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol·L-1NaSO3酸性溶液(含淀粉)的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | X | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | Y | 0 |
该实验的目的是
Ⅱ、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(4)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是
(5)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
 Ce3++
Ce3++ H2O2+
H2O2+ H2O
H2O
 Ce(OH)4↓+
Ce(OH)4↓+
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】实验室用氯酸钾和二氧化锰制取氧气的反应方程式为:2KClO3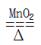 2KCl+3O2。回答下列问题:
2KCl+3O2。回答下列问题:
(1)该反应中被还原的元素名称为__ ,生成2molO2时转移电子的数是__ 。
(2)从反应后的固体混合物中分离出难溶于水的MnO2的具体实验操作名称:__ 。
(3)分离出的MnO2可用于实验室制取Cl2,化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,其离子方程式为
MnCl2+Cl2↑+2H2O,其离子方程式为___ 。
(4)若两个反应中转移的电子的物质的量相同,则生成的O2和Cl2在相同状况下的体积比为___ 。
(5)以上两个反应都用到MnO2,其作用分别___ 。
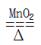 2KCl+3O2。回答下列问题:
2KCl+3O2。回答下列问题:(1)该反应中被还原的元素名称为
(2)从反应后的固体混合物中分离出难溶于水的MnO2的具体实验操作名称:
(3)分离出的MnO2可用于实验室制取Cl2,化学方程式为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,其离子方程式为
MnCl2+Cl2↑+2H2O,其离子方程式为(4)若两个反应中转移的电子的物质的量相同,则生成的O2和Cl2在相同状况下的体积比为
(5)以上两个反应都用到MnO2,其作用分别
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+xOH-Fe3O4↓+S4O
+O2+xOH-Fe3O4↓+S4O +2H2O,反应的离子方程式中x=2。
+2H2O,反应的离子方程式中x=2。_______
 +O2+xOH-Fe3O4↓+S4O
+O2+xOH-Fe3O4↓+S4O +2H2O,反应的离子方程式中x=2。
+2H2O,反应的离子方程式中x=2。
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】氮及其化合物在生产、生活中有着广泛的应用,但同时随意排放氮的化合物也会造成环境污染问题。
Ⅰ.某研究性学习小组设计用如图甲所示的实验装置(夹持仪器省略)制取干燥的氨气并验证NH3具有还原性,回答下列问题:
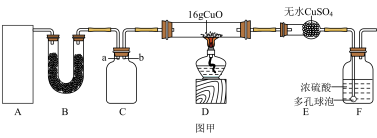
(1)装置C用于收集NH3,应将导管___________ (填“a”或“b”)延长至集气瓶底部。
Ⅱ.以氨气为原料合成硝酸的工业中有含NO、NO2等氮氧化物的尾气排出,有多种方法解决尾气污染环境问题。
(2)写出氨气在制硝酸过程中发生催化氧化反应的化学方程式___________
(3)氨气催化吸收处理尾气法:已知6mol氨气恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为___________ 。
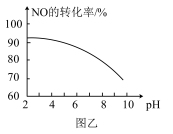
Ⅲ.NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气须处理达标后才能排放。其中NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液的初始pH(用稀盐酸调节)的变化如图乙所示。
的转化率随NaClO溶液的初始pH(用稀盐酸调节)的变化如图乙所示。
(4)在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为
,其离子方程式为___________ 。
(5)NaClO溶液的初始pH越小(c(H+)浓度越大),NO的转化率越高。其原因是___________ 。
Ⅰ.某研究性学习小组设计用如图甲所示的实验装置(夹持仪器省略)制取干燥的氨气并验证NH3具有还原性,回答下列问题:

(1)装置C用于收集NH3,应将导管
Ⅱ.以氨气为原料合成硝酸的工业中有含NO、NO2等氮氧化物的尾气排出,有多种方法解决尾气污染环境问题。
(2)写出氨气在制硝酸过程中发生催化氧化反应的化学方程式
(3)氨气催化吸收处理尾气法:已知6mol氨气恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
Ⅲ.NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气须处理达标后才能排放。其中NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液的初始pH(用稀盐酸调节)的变化如图乙所示。
的转化率随NaClO溶液的初始pH(用稀盐酸调节)的变化如图乙所示。
(4)在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO
 ,其离子方程式为
,其离子方程式为(5)NaClO溶液的初始pH越小(c(H+)浓度越大),NO的转化率越高。其原因是
您最近一年使用:0次
【推荐1】金属钛因具有良好的抗腐蚀能力、熔点高、硬度大、可塑性强、密度小等优点,被誉为“21世纪金属”。工业冶炼钛的第一步反应为:TiO2+2C+2Cl2 TiCl4+2CO。在此反应中,氧化剂是
TiCl4+2CO。在此反应中,氧化剂是__ ,氧化产物是__ ,生成1molTiCl4转移电子的物质的量是__ mol。
 TiCl4+2CO。在此反应中,氧化剂是
TiCl4+2CO。在此反应中,氧化剂是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】储氢碳纳米管的研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的碳纳米颗粒杂质。这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为:2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2M+8H2O+3CO2↑。回答下列问题:
(1)该反应中,生成物M是______ (填化学式)。
(2)该反应中还原剂是______ (填化学式),被还原的元素是______ (填元素符号)。
(3)该反应中,K2Cr2O7表现出______ (填“氧化性”或者“还原性”)。
(4)H2SO4在该反应中表现出______ (填字母)。
(5)用单线桥标明电子转移方向和数目______ 。
(6)每生成2个水分子,转移______ 个电子。
(1)该反应中,生成物M是
(2)该反应中还原剂是
(3)该反应中,K2Cr2O7表现出
(4)H2SO4在该反应中表现出
| A.只有酸性 | B.只有氧化性 | C.酸性和氧化性 | D.酸性和还原性 |
(6)每生成2个水分子,转移
您最近一年使用:0次

 Si+ 2CO↑。
Si+ 2CO↑。

