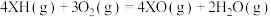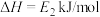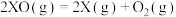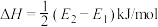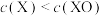标准状况下,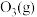 与
与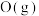 的反应历程如下图。已知:
的反应历程如下图。已知: 和
和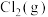 的相对能量为0。
的相对能量为0。
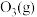 与
与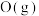 的反应历程如下图。已知:
的反应历程如下图。已知: 和
和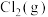 的相对能量为0。
的相对能量为0。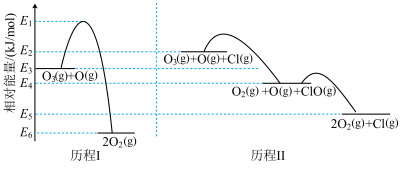
A. |
| B.历程II中,Cl作催化剂 |
C.Cl-Cl键能为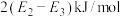 |
D.历程I、历程II中速率最快的反应为: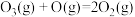 |
更新时间:2023-07-17 07:35:03
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】CH4和CO2可以制造价值更高的化学产品。已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1=a kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) △H2=b kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H3=c kJ·mol-1
则反应CO2(g)+CH4(g) 2CO(g)+2H2(g)的△H用含a、b、c的代数式表示为
2CO(g)+2H2(g)的△H用含a、b、c的代数式表示为
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1=a kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) △H2=b kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H3=c kJ·mol-1
则反应CO2(g)+CH4(g)
 2CO(g)+2H2(g)的△H用含a、b、c的代数式表示为
2CO(g)+2H2(g)的△H用含a、b、c的代数式表示为| A.a+2b-c | B.a+b-2c | C.2a+2b-c | D.a+2b-2c |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知 、
、 、
、 可作为燃料电池的燃料,其相关热化学方程式如下。
可作为燃料电池的燃料,其相关热化学方程式如下。
①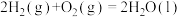
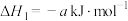
②
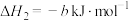
③

④

下列说法正确的是
 、
、 、
、 可作为燃料电池的燃料,其相关热化学方程式如下。
可作为燃料电池的燃料,其相关热化学方程式如下。①
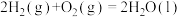
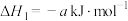
②

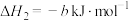
③


④


下列说法正确的是
A.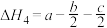 |
B.反应③的 |
C.反应①中若生成 ,则 ,则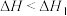 |
D.反应②中的 能表示甲烷的燃烧热 能表示甲烷的燃烧热 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】汽车发动机在工作时,由于电喷,在气缸中会发生反应:N2(g)+O2 (g)=2NO(g)。已知该反应过程中的能量变化如图所示,下列说法中不正确的是

| A.该反应是放热反应 | B.该反应是氧化还原反应 |
| C.该反应过程中有共价键的断裂和形成 | D.使用催化剂可以改变反应速率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】2021年我国科学家实现了二氧化碳到淀粉的人工合成。有关物质的转化过程示意如图:
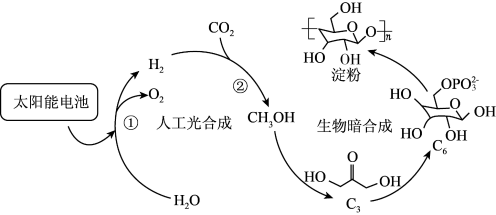
下列说法不正确的是:

下列说法不正确的是:
| A.反应①中分解H2O制备H2需从外界吸收能量 |
| B.反应②中涉及到极性键、非极性键的断裂 |
| C.C6→淀粉的过程中只涉及O-H键的断裂和形成 |
| D.核磁共振、X射线衍射等技术可检测合成淀粉与天然淀粉的结构组成是否一致 |
您最近一年使用:0次
【推荐1】工业上利用炭和水蒸气反应:C(s)+H2O(g)  CO(g)+H2(g)、CO(g)+H2O(g)
CO(g)+H2(g)、CO(g)+H2O(g)  CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO
CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO 能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。
能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。
甲醇与水蒸气重整可获得清洁能源,在催化剂作用下发生如下两步反应:
反应①:CH3OH(g)=CO(g)+2H2(g);ΔH1
反应②: CO(g)+H2O(g)=CO2(g)+H2(g);ΔH2
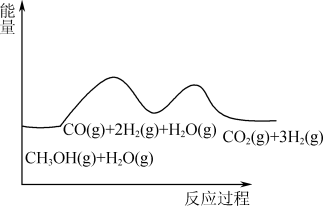
根据能量变化示意图,下列说法不正确的是
 CO(g)+H2(g)、CO(g)+H2O(g)
CO(g)+H2(g)、CO(g)+H2O(g)  CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO
CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO 能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。
能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。甲醇与水蒸气重整可获得清洁能源,在催化剂作用下发生如下两步反应:
反应①:CH3OH(g)=CO(g)+2H2(g);ΔH1
反应②: CO(g)+H2O(g)=CO2(g)+H2(g);ΔH2
根据能量变化示意图,下列说法不正确的是

| A.总反应的热化学方程式为CH3OH(g)+H2O(g)=CO2(g)+3H2(g);ΔH=ΔH1+ΔH2 |
| B.1 mol CO(g)和1 mol H2O(g)的总键能大于1 mol CO2(g)和1 mol H2(g)的总键能 |
| C.甲醇与水蒸气催化重整的总反应速率取决于反应①的速率 |
| D.催化剂在反应中改变了活化能,加快了反应速率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】中国科学家研究在Pd/SVG催化剂上H2还原NO生成N2和NH3的路径,各基元反应及活化能Ea(kJ·mol-1)如图所示,下列说法错误的是
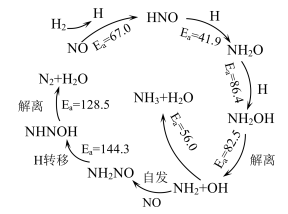

| A.生成NH3的各基元反应中,N元素均被还原 |
| B.在Pd/SVG催化剂上,NO更容易被H2还原为NH3 |
C.决定NO生成NH3速率的基元反应为NH2NO NHNOH NHNOH |
D.生成N2的总反应方程式为2NO+2H2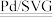 N2+2H2O N2+2H2O |
您最近一年使用:0次

 教授研究了铑
教授研究了铑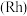 配合物催化醛酮氢化反应,提出的反应机理如图所示,1、2、3、4四种反应的反应热分别为
配合物催化醛酮氢化反应,提出的反应机理如图所示,1、2、3、4四种反应的反应热分别为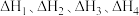 ,下列说法错误的是
,下列说法错误的是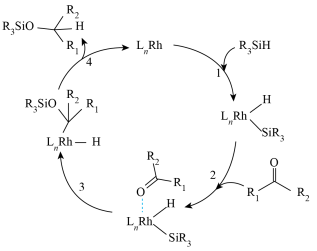
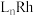 在氢化反应中作催化剂
在氢化反应中作催化剂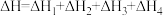
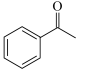 与
与 发生上述反应可生成
发生上述反应可生成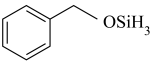

 的平衡转化率
的平衡转化率
 kJ·mol
kJ·mol
 反应生成X或XO的能量-历程变化如图。在恒温恒容的密闭容器中加入一定量的XH和
反应生成X或XO的能量-历程变化如图。在恒温恒容的密闭容器中加入一定量的XH和 时测得
时测得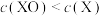 ,下列有关说法不正确的是
,下列有关说法不正确的是