工业上制备纯碱的原理为:NaCl+CO2+NH3+H2O=NH4Cl+NaHCO3,请回答下列问题:
(1)上述反应体系中出现的几种短周期元素中,第二周期元素电负性由大到小的顺序是_____ 。
(2)反应体系中出现的非金属元素,可形成多种化合物,其中和铵根离子空间构型相同,且属于气态有机物的电子式是_____ ,该分子为_____ (填“极性”或“非极性”)分子;
(3)PH3分子与NH3分子结构相似PH3相对分子质量大于NH3,但NH3沸点高于PH3,其原因是:_____ ;
(4)复兴号高铁车体材质用到Mn、Co等元素。Mn的一种配合物化学式[Mn(CO)5(CH3CN)],
①Mn原子的配位数为_____ ;
②CH3CN中C原子的杂化类型为:_____ ;
③CH3CN中σ键与π键数目之比为:_____ ;
(5)化合物FeF3熔点高于1000°C而Fe(CO)5的熔点却低于0°C,FeF3熔点远高于Fe(CO)5的原因可能是_____ ;
(6)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O;
①FeO立方晶胞结构如图甲所示,则Fe2+的配位数为_____ ;
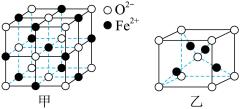
②Cu2O立方晶胞结构如图乙所示,若晶胞参数为apm,则该晶体的密度为_____ g/cm3(用含a、NA的代数式表示,NA代表阿伏加德罗常数的值)。
(1)上述反应体系中出现的几种短周期元素中,第二周期元素电负性由大到小的顺序是
(2)反应体系中出现的非金属元素,可形成多种化合物,其中和铵根离子空间构型相同,且属于气态有机物的电子式是
(3)PH3分子与NH3分子结构相似PH3相对分子质量大于NH3,但NH3沸点高于PH3,其原因是:
(4)复兴号高铁车体材质用到Mn、Co等元素。Mn的一种配合物化学式[Mn(CO)5(CH3CN)],
①Mn原子的配位数为
②CH3CN中C原子的杂化类型为:
③CH3CN中σ键与π键数目之比为:
(5)化合物FeF3熔点高于1000°C而Fe(CO)5的熔点却低于0°C,FeF3熔点远高于Fe(CO)5的原因可能是
(6)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O;
①FeO立方晶胞结构如图甲所示,则Fe2+的配位数为

②Cu2O立方晶胞结构如图乙所示,若晶胞参数为apm,则该晶体的密度为
更新时间:2023-06-21 06:45:57
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】乙酸( )是一种有机一元酸,为食醋的酸味及刺激性气味的来源。它与甲酸甲酯(
)是一种有机一元酸,为食醋的酸味及刺激性气味的来源。它与甲酸甲酯(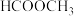 )互为同分异构体。
)互为同分异构体。
(1)组成乙酸的元素的电负性由大到小的顺序是_______ (用元素符号表示)。
(2)乙酸与甲酸甲酯的熔、沸点如下表:
造成二者相差较大的原因是_______ 。
(3)甲酸甲酯经碱性水解可得到 ,该微粒的空间构型是
,该微粒的空间构型是_______ 。
(4)纯的乙酸在低于熔点时会冻结成冰状晶体,所以无水乙酸又称为冰醋酸。
①确定固态乙酸是晶体的最可靠的科学方法是_______ 。
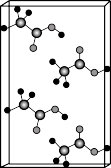
②已知乙酸的晶胞结构如图所示,其密度是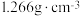 。该晶胞中乙酸的分子数是
。该晶胞中乙酸的分子数是_______ ;若用 表示阿伏加德罗常数的值,则该晶胞的体积为
表示阿伏加德罗常数的值,则该晶胞的体积为_______ 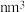 (列出计算式)。
(列出计算式)。
 )是一种有机一元酸,为食醋的酸味及刺激性气味的来源。它与甲酸甲酯(
)是一种有机一元酸,为食醋的酸味及刺激性气味的来源。它与甲酸甲酯(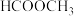 )互为同分异构体。
)互为同分异构体。(1)组成乙酸的元素的电负性由大到小的顺序是
(2)乙酸与甲酸甲酯的熔、沸点如下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| 乙酸 | 16.6 | 117.9 |
| 甲酸甲酯 | -99.8 | 31.5 |
造成二者相差较大的原因是
(3)甲酸甲酯经碱性水解可得到
 ,该微粒的空间构型是
,该微粒的空间构型是(4)纯的乙酸在低于熔点时会冻结成冰状晶体,所以无水乙酸又称为冰醋酸。
①确定固态乙酸是晶体的最可靠的科学方法是
②已知乙酸的晶胞结构如图所示,其密度是
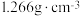 。该晶胞中乙酸的分子数是
。该晶胞中乙酸的分子数是 表示阿伏加德罗常数的值,则该晶胞的体积为
表示阿伏加德罗常数的值,则该晶胞的体积为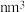 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁、钻、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)基态钴原子的价电子排布式为________ ,铁、钴、镍的基态原子核外未成对电子数最少的是_____________
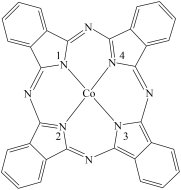
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是__________ (填1、2、3、4),三种非金属原子的电负性由大到小的顺序为____ (用相应的元素符号表示);碳原子的杂化轨道类型为_________
(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO) x晶体属于_______ (填晶体类型),若配合物Fe(CO) x的中心原子价电子数与配体提供电子数之和为18,则x=_________
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO______ FeO(填“>”“<”或“=”),原因是___________________________ 。
(5)NiAs的晶胞结构如图所示:
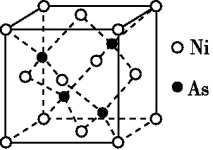
①镍离子的配位数为_________ 。
②若阿伏伽德罗常数的值为NA,晶体密度为pg.cm-1,则该晶胞中最近的离子之间的距离为_____ cm。(写出计算表达式)
(1)基态钴原子的价电子排布式为
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是

(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO) x晶体属于
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
(5)NiAs的晶胞结构如图所示:

①镍离子的配位数为
②若阿伏伽德罗常数的值为NA,晶体密度为pg.cm-1,则该晶胞中最近的离子之间的距离为
您最近一年使用:0次
【推荐3】下图是元素周期表中的前四周期,回答下列问题。

(1)a元素的基态原子的电子排布图是图①、②中的一个。
① ②
②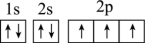
另一个电子排布图错误的原因是它不符合_______ (填字母)。
A.构造原理 B.泡利原理 C.洪特规则
b元素的正二价离子的价层电子排布图是_______ 。
(2)b、e两种元素的第四电离能大小关系为I4(Fe)_______ I4(Co) (填“>”“<”或“=”),原因是_______ 。
(3)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为_______ (填元素符号)。
(4)某元素的原子价层电子排布式为nsn-1npn+1,该基态原子核外电子空间运动状态有_______ 种。
(5)d元素的下列粒子中,电离最外层一个电子所需能量最大的是_______(填字母)。
(6)下列现象与原子核外电子跃迁有关的是_______(填字母)

(1)a元素的基态原子的电子排布图是图①、②中的一个。
①
 ②
②
另一个电子排布图错误的原因是它不符合
A.构造原理 B.泡利原理 C.洪特规则
b元素的正二价离子的价层电子排布图是
(2)b、e两种元素的第四电离能大小关系为I4(Fe)
(3)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为
(4)某元素的原子价层电子排布式为nsn-1npn+1,该基态原子核外电子空间运动状态有
(5)d元素的下列粒子中,电离最外层一个电子所需能量最大的是_______(填字母)。
A. | B. | C.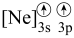 | D.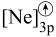 |
| A.激光 | B.LED灯光 | C.金属导电 | D.核辐射 |
您最近一年使用:0次
【推荐1】四羰基镍[Ni(CO)4]主要用于制高纯镍粉,也用于制造塑料中间体。回答下列问题:
(1)Ni在周期表中的位置_______ 。Ni基态原子排布式中3d能级上未成对电子数为_______
(2)Ni(CO)4中三种元素电负性由小到大的顺序为_______
(3)Ni(CO)4为正四面体的配合物。它不溶于水,易溶于乙醇、乙醚等有机溶剂,原因是_______ 。1 mol Ni(CO)4中含有_______ mol σ键。
(4)已知碳的一种单质结构如图1所示,层间距离为335 pm,层内的碳原子的核间距为142 pm。
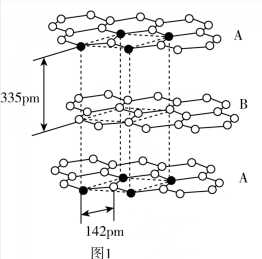
①该单质的晶体类型为_______
②从图1中取出该物质的晶胞如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图2中原子1的坐标为(0,0,0),原子2的坐标为(1,1,1),则原子3和原子4的坐标分别为_______ 、_______ 。
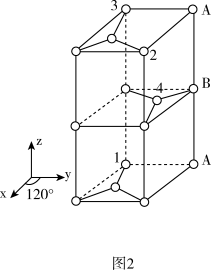
③根据图1中所给的数据,阿伏加德罗常数的值为NA,石墨的密度为_______ g/cm3。(列出计算式)
(1)Ni在周期表中的位置
(2)Ni(CO)4中三种元素电负性由小到大的顺序为
(3)Ni(CO)4为正四面体的配合物。它不溶于水,易溶于乙醇、乙醚等有机溶剂,原因是
(4)已知碳的一种单质结构如图1所示,层间距离为335 pm,层内的碳原子的核间距为142 pm。

①该单质的晶体类型为
②从图1中取出该物质的晶胞如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图2中原子1的坐标为(0,0,0),原子2的坐标为(1,1,1),则原子3和原子4的坐标分别为

③根据图1中所给的数据,阿伏加德罗常数的值为NA,石墨的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】我国科学家成功研制出新型半导体材料(Cs2 AgBiBr6),有望提高器件性能。请回答下列问题:
(1)基态铋(Bi)原子与砷同主族且比磷原子多3个电子层,则基态铋原子价层电子排布图为________ ;基态铯原子最外层电子云轮廓图为________ (填名称)。。
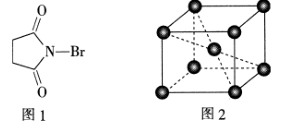
(2)N-溴代琥珀酰亚胺(N—BromoSuccinimide,简称NBS)是一种溴代试剂,结构简式如图1所示。NBS中碳原子的杂化类型是_____ ;1 mol NBS含_____ molσ键。
(3) Ag(NH3) 生中NH3的键角∠HNH大于游离态NH3的键角∠HNH,其主要原因是
生中NH3的键角∠HNH大于游离态NH3的键角∠HNH,其主要原因是___________ 。Ag(NH3) 中配位数为
中配位数为___________ 。
(4)CsF、CsCl、CsBr 、CsI的熔点依次为682℃、645℃、636℃、621℃ ,呈现该变化的原因是___________ 。
(5)溴有多种含氧酸,如HBrO、HBrO2、HBrO3、HBrO4。H、O、Br三种元素的电负性从小到大的顺序为___________ ;BrO 的空间构型是
的空间构型是___________ 。
(6)铯单质的晶胞如图2所示。已知:铯晶体的密度为d g·cm-3,NA为阿伏加德罗常数的值。两个铯原子之间的最短距离为___________ pm(用含 d、NA的代数式表示)。
(1)基态铋(Bi)原子与砷同主族且比磷原子多3个电子层,则基态铋原子价层电子排布图为
(2)N-溴代琥珀酰亚胺(N—BromoSuccinimide,简称NBS)是一种溴代试剂,结构简式如图1所示。NBS中碳原子的杂化类型是

(3) Ag(NH3)
 生中NH3的键角∠HNH大于游离态NH3的键角∠HNH,其主要原因是
生中NH3的键角∠HNH大于游离态NH3的键角∠HNH,其主要原因是 中配位数为
中配位数为(4)CsF、CsCl、CsBr 、CsI的熔点依次为682℃、645℃、636℃、621℃ ,呈现该变化的原因是
(5)溴有多种含氧酸,如HBrO、HBrO2、HBrO3、HBrO4。H、O、Br三种元素的电负性从小到大的顺序为
 的空间构型是
的空间构型是(6)铯单质的晶胞如图2所示。已知:铯晶体的密度为d g·cm-3,NA为阿伏加德罗常数的值。两个铯原子之间的最短距离为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、M、G为前四周期元素,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX,1 mol ZX含有的电子总数为12NA;Y、M同主族,可形成MY2、MY3两种分子;G的核电荷数为29。请回答下列问题:
(1)G原子基态时的核外电子排布式为_______ ,ZX的电子式为________ 。
(2)X2M的燃烧热ΔH=-a kJ·mol-1,写出X2M燃烧热的热化学反应方程式:________ 。
(3)向G的硫酸盐溶液中逐滴加入氨水,产生的现象为_______ ,写出该反应加入氨水至过量的离子方程式为________ ,然后加入乙醇,现象为_______ ,加入乙醇的作用为________ 。
(1)G原子基态时的核外电子排布式为
(2)X2M的燃烧热ΔH=-a kJ·mol-1,写出X2M燃烧热的热化学反应方程式:
(3)向G的硫酸盐溶液中逐滴加入氨水,产生的现象为
您最近一年使用:0次
【推荐1】已知A、B、C、D、E、F为前4周期的6种元素,原子序数依次增大,其中A位于周期表中s区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层电子数的3倍;F元素位于元素周期表的第4行、第11列。试回答下列问题:
(1)基态F原子的核外电子排布式为___ 。
(2)下列关于B2A2的说法中正确的是___ (填选项序号)
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是含极性键和非极性键的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序为___ (用元素符号表示)。
(4)C的简单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有___ (填选项符号)
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为___ ;B和E的最高价氧化物中,熔沸点较高的是___ (写化学式)。
(6)F单质的晶体堆积方式为面心立方最密堆积,其配位数为___ ;若F的相对原子质量为M,它的晶胞棱长为acm,则F晶体的密度为___ g·cm-3。(阿伏加 德罗常数为NA)
(1)基态F原子的核外电子排布式为
(2)下列关于B2A2的说法中正确的是
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是含极性键和非极性键的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序为
(4)C的简单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为
(6)F单质的晶体堆积方式为面心立方最密堆积,其配位数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】D、E、X、Y、Z是短周期元素,且原子序数逐渐增大,它们的最简单氢化物分子的空间结构依次是正四面体、三角锥形、正四面体、角形(V形)、直线形,回答下列问题:
(1)D的氢化物的结构式为___________ ,该分子为___________ (填“极性”或“非极性”)分子。
(2)X的价电子排布式为___________ ,Y的最高价氧化物的VSEPR模型为___________
(3)HZO分子的的中心原子价层电子对数为___________
(4)Y和Z的简单离子的半径大小为___________ (用离子符号和“>”、“=”或“<”表示)。
(1)D的氢化物的结构式为
(2)X的价电子排布式为
(3)HZO分子的的中心原子价层电子对数为
(4)Y和Z的简单离子的半径大小为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硼、镓、氮的化合物在生产、生活中有广泛用途。
(1)氮化镓(GaN)是新型的半导体材料。基态Ga原子的价电子排布图为___________ ;基态N原子的核外有___________ 种空间运动状态的电子。
(2)氟硼酸铵(NH4BF4)是合成氮化硼纳米管的原料之一,该物质中第二周期元素的电负性由大到小的顺序是___________ 。
(3)鉴定镍、钴、铜、钯等可用双氰胺,其结构如下图(3)所示。则该分子中碳原子的杂化方式有_______ ;该分子中σ键与π键数目之比为_______ ;该分子中键能最大的是________ 键。
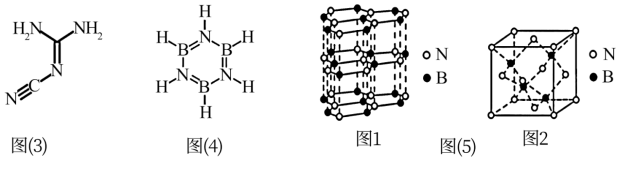
(4)硼与氮形成类似苯的化合物硼氮苯(B3N3H6),俗称无机苯,其结构如上图(4),则硼氮苯属于___________ 分子(填“极性”或“非极性”)。
(5)氮化硼是一种性能优异的新型材料,其主要结构如上图(5)所示,有六方氮化硼(图1)和立方氮化硼(图2),前者与石墨结构类似。
①50.0g六方氮化硼晶体中含有六元环的数目为___________ ;
②立方氮化硼中N的配位数为___________ ;
③已知立方氮化硼密度为dg·cm-3,NA代表阿伏加德罗常数,立方氮化硼晶胞中面心上6个N原子相连构成正八面体,该正八面体的边长为___________ pm(列式即可)。
(1)氮化镓(GaN)是新型的半导体材料。基态Ga原子的价电子排布图为
(2)氟硼酸铵(NH4BF4)是合成氮化硼纳米管的原料之一,该物质中第二周期元素的电负性由大到小的顺序是
(3)鉴定镍、钴、铜、钯等可用双氰胺,其结构如下图(3)所示。则该分子中碳原子的杂化方式有

(4)硼与氮形成类似苯的化合物硼氮苯(B3N3H6),俗称无机苯,其结构如上图(4),则硼氮苯属于
(5)氮化硼是一种性能优异的新型材料,其主要结构如上图(5)所示,有六方氮化硼(图1)和立方氮化硼(图2),前者与石墨结构类似。
①50.0g六方氮化硼晶体中含有六元环的数目为
②立方氮化硼中N的配位数为
③已知立方氮化硼密度为dg·cm-3,NA代表阿伏加德罗常数,立方氮化硼晶胞中面心上6个N原子相连构成正八面体,该正八面体的边长为
您最近一年使用:0次
【推荐1】我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。回答下列问题:
(1)氮原子价层电子的轨道表达式(电子排布图)为___ 。
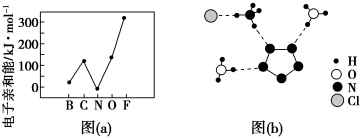
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___ ;氮元素的E1呈现异常的原因是___ 。
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。
①从结构角度分析,R中两种阳离子的相同之处为___ ,不同之处为____ 。(填标号)
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②图(b)中虚线代表氢键,其表示式为(NH4+)N-H┄Cl、____ 、____ 。
(4)R的晶体密度为d g·cm-3,其立方晶胞参数为anm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为____ 。
(1)氮原子价层电子的轨道表达式(电子排布图)为
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。
①从结构角度分析,R中两种阳离子的相同之处为
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②图(b)中虚线代表氢键,其表示式为(NH4+)N-H┄Cl、

(4)R的晶体密度为d g·cm-3,其立方晶胞参数为anm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国具有悠久的历史,在春秋时期已经开始冶铁,在西汉就有湿法炼铜( )。
)。
(1)基态铁原子的电子排布式为
_______ 。
(2)铁氰化钾 是检验
是检验 的重要试剂,在铁氰化钾的组成元素中,属于第2周期的元素的第一电离能由小到大的顺序是
的重要试剂,在铁氰化钾的组成元素中,属于第2周期的元素的第一电离能由小到大的顺序是_______ ,碳原子的杂化类型是________ 。
(3) 是一种浅黄色液体,熔点
是一种浅黄色液体,熔点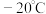 ,沸点103℃,易溶于苯等有机溶剂,不溶于水。
,沸点103℃,易溶于苯等有机溶剂,不溶于水。 是
是_________ 分子(填“极性”或“非极性”)
(4)铜常见化合价为 、
、 价,高温下
价,高温下 比
比 更稳定的原因是
更稳定的原因是__________ 。
(5) 比
比 的熔点高的原因是
的熔点高的原因是_____________ 。
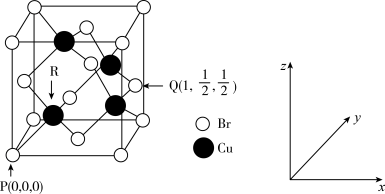
(6)一种铜的溴化物晶胞结构如图所示,由图可知,该晶体的化学式为_____________ ,与每个 紧邻的
紧邻的 有
有___________ 个,由图中的P点和Q点的原子坐标参数,可确定R点的原子坐标参数为_____ 。若 原子与最近的
原子与最近的 原子的核间距为
原子的核间距为 ,则该晶体的密度计算表达式为
,则该晶体的密度计算表达式为
______  。
。
 )。
)。(1)基态铁原子的电子排布式为

(2)铁氰化钾
 是检验
是检验 的重要试剂,在铁氰化钾的组成元素中,属于第2周期的元素的第一电离能由小到大的顺序是
的重要试剂,在铁氰化钾的组成元素中,属于第2周期的元素的第一电离能由小到大的顺序是(3)
 是一种浅黄色液体,熔点
是一种浅黄色液体,熔点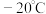 ,沸点103℃,易溶于苯等有机溶剂,不溶于水。
,沸点103℃,易溶于苯等有机溶剂,不溶于水。 是
是(4)铜常见化合价为
 、
、 价,高温下
价,高温下 比
比 更稳定的原因是
更稳定的原因是(5)
 比
比 的熔点高的原因是
的熔点高的原因是(6)一种铜的溴化物晶胞结构如图所示,由图可知,该晶体的化学式为
 紧邻的
紧邻的 有
有 原子与最近的
原子与最近的 原子的核间距为
原子的核间距为 ,则该晶体的密度计算表达式为
,则该晶体的密度计算表达式为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(1)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H)。
请回答下列问题:
①比较下列两组物质的熔点高低(填“>”或“<”=)
SiC_____________ Si;SiCl4_____________ SiO2
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g)该反应的反应热△H=
Si(s)+4HCl(g)该反应的反应热△H=_____________ kJ/mol.
(2)已知化合物Na2O的晶胞如图。
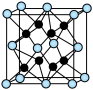
①其中O2-离子的配位数为________ ,
②该化合物与MgO相比,熔点较高的是________ 。(填化学式)
③已知该化合物的晶胞边长为apm,则该化合物的密度为___ g·cm-3(只要求列出算式,不必计算出数值,阿伏加 德罗常数的数值为NA)。
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
①比较下列两组物质的熔点高低(填“>”或“<”=)
SiC
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
 Si(s)+4HCl(g)该反应的反应热△H=
Si(s)+4HCl(g)该反应的反应热△H=(2)已知化合物Na2O的晶胞如图。

①其中O2-离子的配位数为
②该化合物与MgO相比,熔点较高的是
③已知该化合物的晶胞边长为apm,则该化合物的密度为
您最近一年使用:0次



