含氯、硫、磷等元素的化合物是重要的化工原料,有关比较中不正确 的是
| A.原子半径:P > S > Cl | B.第一电离能:P < S < Cl |
| C.电负性: P < S < Cl | D.最简单氢化物的热稳定性:P < S < Cl |
更新时间:2023-07-29 17:05:46
|
相似题推荐
【推荐1】下列有关叙述不正确 的是
| A.N原子的第一电离能大于О原子 | B.HF的热稳定性和沸点均大于 |
C. 和 和 化学键类型相同 化学键类型相同 | D.BN和SiC熔化克服的作用力相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的是
| A.质量数相同的原子互为同位素 |
| B.0族元素的化学性质不活泼,其单质不发生任何反应 |
| C.同主族元素从上到下,元素的金属性逐渐增强 |
| D.在金属元素与非金属元素的分界线附近可以寻找制造催化剂的元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
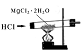
【推荐1】下列实验设计能够达到目的的是
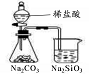
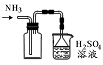
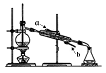
A | B | C | D |
制取无水MgCl2 | 比较非金属性:C>Si | 用如图装置收集NH3 | 实验室模拟石油分馏 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知Te为第五周期第ⅥA族元素。下列结论正确的是
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>H2SiO3
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>H2SiO3
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
| A.②⑤⑦ | B.②④⑥ | C.②④⑤⑥⑦ | D.②⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素 X、Y、Z、W 原子序数依次增大,X 原子的最外层电子数是其周期数的 3 倍, Z 是短周期元素中原子半径最大的,0.1mol·L-1 的 W 最高价氧化物对应的水化物的水溶液 pH=1。 下列说法正确的是
| A.第一电离能的大小顺序:X>Y>W>Z |
| B.由于氢键的作用导致气态氢化物的稳定性 X>W |
| C.ZY 的水溶液使蓝色石蕊试纸显红色 |
| D.Z 分别与其它三种元素组成的二元化合物均含有离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知X、Y两元素同周期,且电负性X>Y,下列说法错误的是
| A.X与Y形成化合物时,X可以显正价,Y显负价 |
| B.气态氢化物的稳定性:HaX大于HbY |
| C.最高价含氧酸的酸性:X对应酸的酸性强于Y对应酸的酸性 |
| D.第一电离能Y可能大于X |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】C、N、O、Al、Si、Cu是常见的六种元素,下列说法错误的是
| A.Si位于元素周期表第三周期第 ⅣA 族 |
| B.O、Na、P、Cl四种元素中电负性最大的是Cl, 其中P原子的核外电子排布式为 1s22s22p63s23p3 |
| C.基态锗(Ge)原子的电子排布式是1s22s22p63s23p63d104s24p2 ,Ge的最高价氯化物的分子式是GeCl4 |
| D.Ge的最高价氯化物的沸点低于其溴化物的沸点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
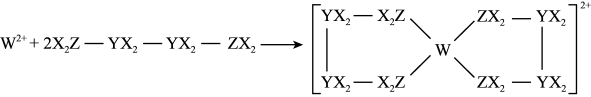
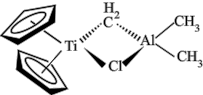
【推荐2】科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
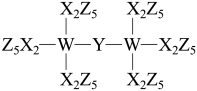
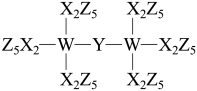
| A.元素X、Y、Z的最高正价等于其原子的最外层电子数 |
B.电负性: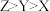 |
| C.Z的单质与水能发生置换反应 |
| D.原子序数为82的元素与W位于同一主族 |
您最近一年使用:0次

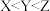
 杂化
杂化

