下列元素性质描述错误的是
A. 、 、 、 、 半径依次减小 半径依次减小 | B.N、O、F的第一电离能依次增大 |
| C.Na、Mg、Al的电负性依次增大 | D. 、 、 、 、 的还原性依次增强 的还原性依次增强 |
22-23高二上·江西萍乡·期末 查看更多[2]
更新时间:2023-07-30 19:30:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
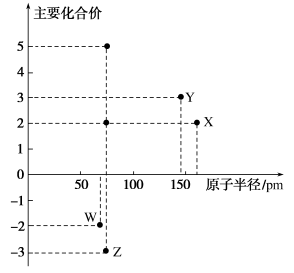
【推荐1】某新型漂白剂(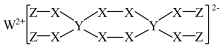 )可用于漂白各种动物毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X 的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述不正确的是
)可用于漂白各种动物毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X 的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述不正确的是
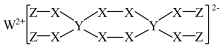 )可用于漂白各种动物毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X 的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述不正确的是
)可用于漂白各种动物毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X 的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述不正确的是| A.WX、WZ2均是离子化合物 |
| B.W、X、Y对应的原子半径顺序为:W>X>Y |
| C.X、Y与Z均可以形成化合物 |
| D.Y的最高价氧化物对应水化物为弱酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.原子半径:P<S<Cl |
| B.电负性:C<N<O |
| C.热稳定性:HF<HCl<HBr |
| D.第一电离能:Na<Mg<Al |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知Ra(镭)是第七周期ⅡA族元素,原子序数为88。它是居里夫妇首先发现的一种元素。有关它的性质推断不正确的是
| A.镭单质很活泼,可与冷水反应 | B.它的硫酸盐可能难溶于水 |
| C.镭单质的硬度,熔沸点都比镁单质的高 | D.镭元素具有放射性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据同主族元素性质的递变规律分析下列推断正确的是
①钾的金属性比钠强,因此钾可以从氯化钠溶液中置换出钠
②卤素单质与水的反应均可用化学方程式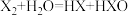 表示
表示
③硫化氢比硒化氢稳定
④氢氧化钡比氢氧化钙的碱性强
⑤钠、钾、铷三种单质中,铷的熔点最高
⑥砹单质的颜色比碘单质的颜色深
⑦已知同主族元素中,核电荷数氯大于氟,故原子半径氯大于氟
①钾的金属性比钠强,因此钾可以从氯化钠溶液中置换出钠
②卤素单质与水的反应均可用化学方程式
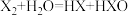 表示
表示③硫化氢比硒化氢稳定
④氢氧化钡比氢氧化钙的碱性强
⑤钠、钾、铷三种单质中,铷的熔点最高
⑥砹单质的颜色比碘单质的颜色深
⑦已知同主族元素中,核电荷数氯大于氟,故原子半径氯大于氟
| A.①②④⑦ | B.②③⑤⑥ | C.①④⑤⑦ | D.③④⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】W、X、Y、Z为原子序数依次增大的短周期主族元素,Z原子的质子数等于W原子与Y原子质子数之和,W的价层电子数为偶数,X原子核外未成对电子数与W的相同,四种元素中只有Y为金属元素。下列说法正确的是
A.第一电离能: |
| B.X与Y形成的化合物可能含有共价键 |
C.电负性: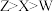 |
| D.W与Z形成的化合物具有可燃性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】几种短周期元素的原子半径及某些化合价见下表。判断下列说法正确的是( )
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1、+7 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A.A的单质能将E的单质从HE3的溶液中置换出来 |
| B.A、H、J的离子半径由大到小的顺序是A>J>H |
| C.H、I、J的第一电离能大小顺序是H>I>J |
| D.I的单质在DB2中燃烧生成两种化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】氨硼烷 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。氨硼烷在催化剂作用下水解放出氢气:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。氨硼烷在催化剂作用下水解放出氢气: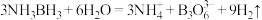 ,
, 的结构如图。下列说法正确的是
的结构如图。下列说法正确的是
 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。氨硼烷在催化剂作用下水解放出氢气:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。氨硼烷在催化剂作用下水解放出氢气: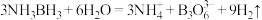 ,
, 的结构如图。下列说法正确的是
的结构如图。下列说法正确的是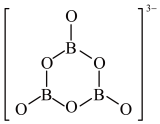
| A.基态B原子电子占据最高能级的电子云轮廓图为球形 |
| B.第一电离能:O>N>B |
| C.原子半径:N>B>H |
D. 中各原子均在同一平面内 中各原子均在同一平面内 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】现有四种元素的基态原子的电子排布式如下:①[Ne]3s23p3; ②[Ne]3s23p4;③1s22s22p63s23p5。则下列有关比较中正确的是
| A.最高正化合价:①>③>② |
| B.单质氧化性:①>②>③ |
| C.电负性:①>③>② |
| D.最高价氧化物的水合物的酸性:③>②>① |
您最近一年使用:0次

 溶液
溶液
 的漂白性将其作为葡萄酒的抗氧化剂
的漂白性将其作为葡萄酒的抗氧化剂 中所含阳离子和阴离子的比例是1∶2
中所含阳离子和阴离子的比例是1∶2

