工业上用铬铁矿(主要成分为 ,含
,含 、
、 杂质)生产红矾钠(
杂质)生产红矾钠( )的工艺流程如下:
)的工艺流程如下:
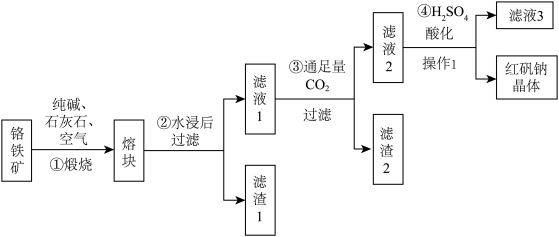
(1)熔块的主要成分 ,
,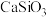 ,
, 和氧化铁,则滤渣1的主要成分是
和氧化铁,则滤渣1的主要成分是_______ (填化学式)。
(2)上述四个步骤中,发生氧化还原反应的是___________ (填序号),被氧化的元素是___________ (填元素符号)。
(3)操作1的名称:___________ 。
(4)向橙红色的红钒钠溶液中滴入氢氧化钠溶液,变为黄色 溶液,写出该转化过程的离子方程式:
溶液,写出该转化过程的离子方程式:___________ 。
 ,含
,含 、
、 杂质)生产红矾钠(
杂质)生产红矾钠( )的工艺流程如下:
)的工艺流程如下:
(1)熔块的主要成分
 ,
,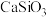 ,
, 和氧化铁,则滤渣1的主要成分是
和氧化铁,则滤渣1的主要成分是(2)上述四个步骤中,发生氧化还原反应的是
(3)操作1的名称:
(4)向橙红色的红钒钠溶液中滴入氢氧化钠溶液,变为黄色
 溶液,写出该转化过程的离子方程式:
溶液,写出该转化过程的离子方程式:
更新时间:2023-07-03 11:16:13
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】利用硫铁矿烧渣(主要成分为Fe3O4、FeO、SiO2等)和粉煤灰(主要成分为Al2O3、Fe2O3、FeO等),制备高效水处理剂聚合硫酸铁铝的流程如下:
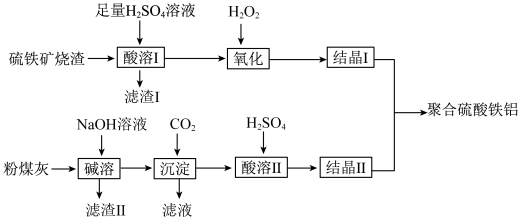
已知:SiO2既不溶于H2SO4溶液,也不和H2SO4溶液反应。
(1)“酸溶Ⅰ”得到的溶液中所含的金属阳离子主要有___________ 。
(2)“氧化”时,若用氯水代替H2O2,
①发生反应的离子方程式为___________ 。
②与使用氯水相比,“氧化”时使用H2O2的优点是___________ 。
(3)“碱溶”时,Al2O3发生反应的化学方程式为___________ 。
(4)在流程中可以循环利用的是___________ (填“滤渣Ⅰ”、“滤渣Ⅱ”或“滤渣Ⅰ和滤渣Ⅱ”)。
(5)向Fe3O4、FeO的固体混合物中,加入足量H2SO4溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中离子浓度比为c(Cu2+):c(Fe2+)=2:7,则固体混合物中物质的量比n(Fe3O4):n(FeO)为___________ 。

已知:SiO2既不溶于H2SO4溶液,也不和H2SO4溶液反应。
(1)“酸溶Ⅰ”得到的溶液中所含的金属阳离子主要有
(2)“氧化”时,若用氯水代替H2O2,
①发生反应的离子方程式为
②与使用氯水相比,“氧化”时使用H2O2的优点是
(3)“碱溶”时,Al2O3发生反应的化学方程式为
(4)在流程中可以循环利用的是
(5)向Fe3O4、FeO的固体混合物中,加入足量H2SO4溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中离子浓度比为c(Cu2+):c(Fe2+)=2:7,则固体混合物中物质的量比n(Fe3O4):n(FeO)为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】醋酸亚铬是一种氧气吸收剂, 通常以二水盐[Cr(CH3COO)2]2 ·2H2O(式量:376)的形式存在,难溶于冷水,易溶于盐酸。其制备原理和实验装置:
制备原理:
实验装置:(如图所示)

(1)仪器 A 的名称是__________ 。
(2)装好试剂后按上述装置进行实验,完成下表内容。
(3)洗涤产品后干燥、称量,得到 1.0g 固体。列式表示产率:____ (不必计算出结果,K2Cr2O7式量:294)。在实验中如果盐酸过量,会导致产率偏________ 。(填“高”或“低”)
制备原理:

实验装置:(如图所示)

(1)仪器 A 的名称是
(2)装好试剂后按上述装置进行实验,完成下表内容。
| 操作步骤 | 实验现象 | 发生反应的离子方程式 |
| 关闭① | 抽滤瓶中锌粒溶解,溶液由橙色逐渐变成蓝色,有少量气泡 | ③ |
| 抽滤瓶中产生大量气体时快速加入适量盐酸,关闭K2和④ | 抽滤瓶中⑥ | Zn+2H+=Zn2++H2↑ |
| 当溶液完全转移后,迅速塞紧锥形瓶,用冷水冷却 | 锥形瓶中有深红色晶体析出 | ⑦ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】 是一种易溶于水且不与水反应的黄绿色气体,沸点为11℃,具有强氧化性,是一种常用的消毒剂,可用于污水杀菌和饮用水净化,可通过
是一种易溶于水且不与水反应的黄绿色气体,沸点为11℃,具有强氧化性,是一种常用的消毒剂,可用于污水杀菌和饮用水净化,可通过 与酸性
与酸性 溶液反应制备,某化学兴趣小组同学设计了如下装置制备
溶液反应制备,某化学兴趣小组同学设计了如下装置制备 并探究其性质。
并探究其性质。

已知:浓硫酸与 固体反应可用来制备
固体反应可用来制备 ,二氧化硫易溶于水,具有还原性,在水溶液中易被氧化成
,二氧化硫易溶于水,具有还原性,在水溶液中易被氧化成 ,回答下列问题:
,回答下列问题:
(1)A中盛装 固体的仪器名称为
固体的仪器名称为_______ 。
(2)通过装置B中反应制备 ,此反应的离子方程式为
,此反应的离子方程式为_______ 。
(3)欲制备一瓶 ,选择上图中的装置,其接口的连接顺序为a-g-h
,选择上图中的装置,其接口的连接顺序为a-g-h_______ 。
(4)装置D盛放冰水的目的_______ ,装置E的作用是_______ 。
(5)证明 的氧化性比
的氧化性比 强的实验方案是
强的实验方案是_______ 。
(6)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力(还原产物均为氯离子)。
的氧化能力(还原产物均为氯离子)。 的有效氯含量为
的有效氯含量为_______ 克(计算结果保留一位小数)。
 是一种易溶于水且不与水反应的黄绿色气体,沸点为11℃,具有强氧化性,是一种常用的消毒剂,可用于污水杀菌和饮用水净化,可通过
是一种易溶于水且不与水反应的黄绿色气体,沸点为11℃,具有强氧化性,是一种常用的消毒剂,可用于污水杀菌和饮用水净化,可通过 与酸性
与酸性 溶液反应制备,某化学兴趣小组同学设计了如下装置制备
溶液反应制备,某化学兴趣小组同学设计了如下装置制备 并探究其性质。
并探究其性质。
已知:浓硫酸与
 固体反应可用来制备
固体反应可用来制备 ,二氧化硫易溶于水,具有还原性,在水溶液中易被氧化成
,二氧化硫易溶于水,具有还原性,在水溶液中易被氧化成 ,回答下列问题:
,回答下列问题:(1)A中盛装
 固体的仪器名称为
固体的仪器名称为(2)通过装置B中反应制备
 ,此反应的离子方程式为
,此反应的离子方程式为(3)欲制备一瓶
 ,选择上图中的装置,其接口的连接顺序为a-g-h
,选择上图中的装置,其接口的连接顺序为a-g-h(4)装置D盛放冰水的目的
(5)证明
 的氧化性比
的氧化性比 强的实验方案是
强的实验方案是(6)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力(还原产物均为氯离子)。
的氧化能力(还原产物均为氯离子)。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】图中,A为一种中学化学中常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色实验均为黄色。
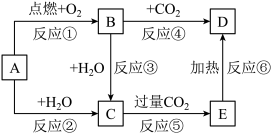
(1)写出下列物质的化学式:B___ 。
(2)以上6个反应中属于氧化还原反应的有___ (填写编号)。
(3)写出A →C反应的离子方程式___ 。
(4)写出B→C反应的离子方程式:___ ;E→D的化学方程式:___ 。
(5)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量分数为___ 。

(1)写出下列物质的化学式:B
(2)以上6个反应中属于氧化还原反应的有
(3)写出A →C反应的离子方程式
(4)写出B→C反应的离子方程式:
(5)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】甲、乙同学对 及其化合物的相关性质与用途进行探究。
及其化合物的相关性质与用途进行探究。
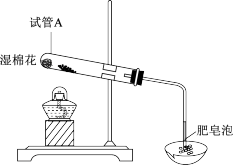
(1)实验I:甲、乙两同学分别用下图装置进行 粉与水蒸气反应的实验。
粉与水蒸气反应的实验。
①证明生成的气体是氢气,依据的现象是_______ 。
②该反应的化学方程式是_______ 。
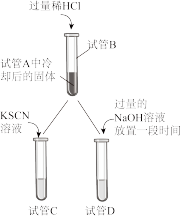
(2)实验Ⅱ:甲、乙同学分别对各自实验Ⅰ反应后的黑色固体进行研究。冷却后取试管A中的固体加入过量稀 ,充分反应后将溶液分成两份,进行如下操作。已知:
,充分反应后将溶液分成两份,进行如下操作。已知: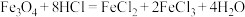
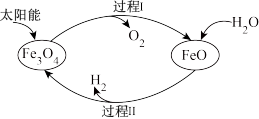
(3)查阅资料:认识 的重要用途。资料:纳米级
的重要用途。资料:纳米级 可用于以太阳光为热源分解水制
可用于以太阳光为热源分解水制 ,过程如下图所示。下列说法中正确的是_______。
,过程如下图所示。下列说法中正确的是_______。
 及其化合物的相关性质与用途进行探究。
及其化合物的相关性质与用途进行探究。
(1)实验I:甲、乙两同学分别用下图装置进行
 粉与水蒸气反应的实验。
粉与水蒸气反应的实验。①证明生成的气体是氢气,依据的现象是
②该反应的化学方程式是
(2)实验Ⅱ:甲、乙同学分别对各自实验Ⅰ反应后的黑色固体进行研究。冷却后取试管A中的固体加入过量稀
 ,充分反应后将溶液分成两份,进行如下操作。已知:
,充分反应后将溶液分成两份,进行如下操作。已知: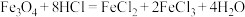
| 操作过程 | 现象及结论 | |
| 甲同学 | 乙同学 | |
| 试管B中固体全部溶解,得到溶液M | 试管B固体全部溶解,同时有大量气泡产生,得到溶液N |
| 试管C溶液变红 | 试管C溶液没有变红,用离子方程式解释原因: | |
| 若试管D开始有红褐色和灰绿色沉淀生成,最终全部变为红褐色。则溶液M中存在的阳离子有: | 试管D实验现象是 | |
 的重要用途。资料:纳米级
的重要用途。资料:纳米级 可用于以太阳光为热源分解水制
可用于以太阳光为热源分解水制 ,过程如下图所示。下列说法中正确的是_______。
,过程如下图所示。下列说法中正确的是_______。
A.过程I的反应: |
B.过程Ⅱ的反应: |
| C.过程I和过程Ⅱ都发生了氧化还原反应 |
D.纳米级 在光解水制 在光解水制 过程中起催化作用 过程中起催化作用 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】根据所学知识填写下列空白:
(1)现有下列十种物质:①HCl气体②Cu③C2H5OH④CO2⑤CuSO4•5H2O⑥NaHCO3⑦Ba(OH)2溶液⑧熔融Na2SO4⑨液氨⑩空气。
所给物质能导电的是_______ ;属于强电解质的是_______ ;属于非电解质的是_______ (填所给物质的序号)。
(2)如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。
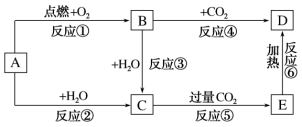
请填写下列空白:
①写出反应②的实验现象:_______ 。
②以上反应中属于氧化还原反应的有_______ (填编号)。
③反应②的离子反应方程式为_______ ;反应④的化学方程式为_______ ;向D中滴入少量盐酸的离子方程式为_______ 。
(1)现有下列十种物质:①HCl气体②Cu③C2H5OH④CO2⑤CuSO4•5H2O⑥NaHCO3⑦Ba(OH)2溶液⑧熔融Na2SO4⑨液氨⑩空气。
所给物质能导电的是
(2)如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。

请填写下列空白:
①写出反应②的实验现象:
②以上反应中属于氧化还原反应的有
③反应②的离子反应方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
“酸浸氧化”中,VO+和VO2+被氧化成 ,同时还有
,同时还有__ 离子被氧化。写出VO+转化为 反应的离子方程式
反应的离子方程式___ 。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
回答下列问题:
“酸浸氧化”中,VO+和VO2+被氧化成
 ,同时还有
,同时还有 反应的离子方程式
反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】【化学——选修2:化学与技术】
某工厂用软锰矿(含MnO2约70% 及A12O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料)。

已知:①A是 的混合液。
的混合液。
②IV中的电解方程式为:
(l)A中属于还原产物的是________________________ 。
(2)加入MnCO3、Zn2(OH)2CO3的作用________________________ 。
II需要加热的原因是:____________________ 。C的化学式是 _______________ 。
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是_________________ 。
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是_____________ 。
(5)要从Na2SO4溶液中得到芒硝(Na2SO4·10H2O),需进行的操作有蒸发浓缩、___________ 、过滤、洗涤、干燥等。
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是__________ 。
某工厂用软锰矿(含MnO2约70% 及A12O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料)。

已知:①A是
 的混合液。
的混合液。②IV中的电解方程式为:

(l)A中属于还原产物的是
(2)加入MnCO3、Zn2(OH)2CO3的作用
II需要加热的原因是:
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是
(5)要从Na2SO4溶液中得到芒硝(Na2SO4·10H2O),需进行的操作有蒸发浓缩、
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】无水 AlCl3 (178℃升华)遇潮湿空气即产生大量白雾。实验室模拟用Al和氯气通过如图装置制备无水AlCl3。回答下列问题:
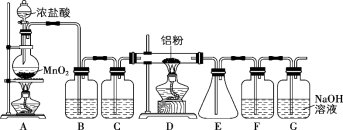
(1)盛装浓盐酸的仪器的名称是____________ 。
(2)写出圆底烧瓶中反应的化学方程式____________ 。
(3)实验开始前应先___________ ,然后加入药品,再点燃A处酒精灯开始反应,待观察到______________ 时,最后点燃D处酒精灯。
(4)写出D中发生反应的化学方程式是_______________ 。
(5)甲同学认为装置F和G可以用一个装置代替,该装置是__________ 。
(6)乙同学认为该装置存在一处缺陷,为弥补此缺陷可以在D和E之间进行改进,改进的方法为:_______________ 。

(1)盛装浓盐酸的仪器的名称是
(2)写出圆底烧瓶中反应的化学方程式
(3)实验开始前应先
(4)写出D中发生反应的化学方程式是
(5)甲同学认为装置F和G可以用一个装置代替,该装置是
(6)乙同学认为该装置存在一处缺陷,为弥补此缺陷可以在D和E之间进行改进,改进的方法为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】磷酸二氢铵 和草酸亚铁晶体
和草酸亚铁晶体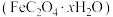 可用于制备电池正极材料。
可用于制备电池正极材料。
I.某研究小组用磷酸吸收氨气制 ,装置如图所示(夹持和搅拌装置已省略)。
,装置如图所示(夹持和搅拌装置已省略)。
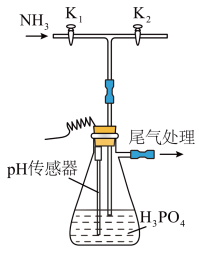
(1)实验过程中,当出现倒吸现象时,___________ (填写实验操作,下同),当上述现象消失后,___________ ,继续通入氨气。
(2)常温下,磷酸盐溶液中含磷物种的分布系数与pH的关系如图所示,据图示分析,若本实验不选用pH传感器,还可选用___________ 作指示剂,当溶液颜色发生相应变化时,停止通 ,即可制得
,即可制得 溶液。若此时继续向溶液中通入少量氨气,发生反应的离子方程式为
溶液。若此时继续向溶液中通入少量氨气,发生反应的离子方程式为___________ 。

II.利用草酸制备草酸亚铁晶体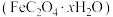 的流程如图所示:
的流程如图所示:
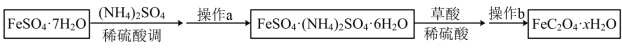
已知:i.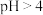 时,
时, 易被氧气氧化;
易被氧气氧化;
ii.几种物质的溶解度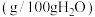 如表:
如表:
(3)操作a是蒸发浓缩,___________ (填操作)。
(4)为测定草酸亚铁晶体中结晶水含量,将石英玻璃管(若两端开关 和
和 ,设为装置A)称重,记为
,设为装置A)称重,记为 ,将样品装入石英玻璃管中,再次将装置A称重,记为
,将样品装入石英玻璃管中,再次将装置A称重,记为 。按如图所示连接好装置进行实验。
。按如图所示连接好装置进行实验。
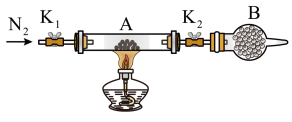
下列实验操作的正确顺序为___________ (填序号)。
①点燃酒精灯,小火加热 ②停止通入氮气,关闭 、
、 ③打开
③打开 、
、
④熄灭酒精灯,冷却至室温 ⑤缓缓通入氮气 ⑥称重A
 和草酸亚铁晶体
和草酸亚铁晶体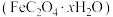 可用于制备电池正极材料。
可用于制备电池正极材料。I.某研究小组用磷酸吸收氨气制
 ,装置如图所示(夹持和搅拌装置已省略)。
,装置如图所示(夹持和搅拌装置已省略)。
(1)实验过程中,当出现倒吸现象时,
(2)常温下,磷酸盐溶液中含磷物种的分布系数与pH的关系如图所示,据图示分析,若本实验不选用pH传感器,还可选用
 ,即可制得
,即可制得 溶液。若此时继续向溶液中通入少量氨气,发生反应的离子方程式为
溶液。若此时继续向溶液中通入少量氨气,发生反应的离子方程式为
II.利用草酸制备草酸亚铁晶体
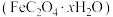 的流程如图所示:
的流程如图所示: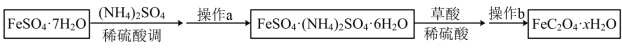
已知:i.
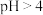 时,
时, 易被氧气氧化;
易被氧气氧化;ii.几种物质的溶解度
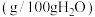 如表:
如表: |  |  | |
| 20℃ | 48 | 75 | 37 |
| 60℃ | 101 | 88 | 38 |
(4)为测定草酸亚铁晶体中结晶水含量,将石英玻璃管(若两端开关
 和
和 ,设为装置A)称重,记为
,设为装置A)称重,记为 ,将样品装入石英玻璃管中,再次将装置A称重,记为
,将样品装入石英玻璃管中,再次将装置A称重,记为 。按如图所示连接好装置进行实验。
。按如图所示连接好装置进行实验。
下列实验操作的正确顺序为
①点燃酒精灯,小火加热 ②停止通入氮气,关闭
 、
、 ③打开
③打开 、
、
④熄灭酒精灯,冷却至室温 ⑤缓缓通入氮气 ⑥称重A
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯乙酸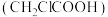 是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法为
是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法为 ,已知:
,已知: 易与水反应;冰醋酸为不含水的纯醋酸;装置①选择
易与水反应;冰醋酸为不含水的纯醋酸;装置①选择 和浓盐酸制取氯气。学习小组用如图所示装置进行探究,请回答下列问题。
和浓盐酸制取氯气。学习小组用如图所示装置进行探究,请回答下列问题。

(1)装置 的名称为
的名称为_______ ,装置⑥使用倒扣的漏斗的原因是_______ 。
(2)试剂 为
为_______ 。
(3)装置⑥的主要作用是吸收尾气,避免污染空气,除与 反应外,还发生其他主要反应的化学方程式为
反应外,还发生其他主要反应的化学方程式为_______ ,_______ 。
(4)观察实验现象,能说明产物有 生成的实验现象是
生成的实验现象是_______ 。有同学认为该实验可以定量测定生成的 ,你认为
,你认为_______ (填“合理”或“不合理”),你的理由是_______ 。
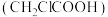 是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法为
是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法为 ,已知:
,已知: 易与水反应;冰醋酸为不含水的纯醋酸;装置①选择
易与水反应;冰醋酸为不含水的纯醋酸;装置①选择 和浓盐酸制取氯气。学习小组用如图所示装置进行探究,请回答下列问题。
和浓盐酸制取氯气。学习小组用如图所示装置进行探究,请回答下列问题。
(1)装置
 的名称为
的名称为(2)试剂
 为
为(3)装置⑥的主要作用是吸收尾气,避免污染空气,除与
 反应外,还发生其他主要反应的化学方程式为
反应外,还发生其他主要反应的化学方程式为(4)观察实验现象,能说明产物有
 生成的实验现象是
生成的实验现象是 ,你认为
,你认为
您最近一年使用:0次