下列说法中正确的是
| A.除最外层外,原子各电子层上电子数均已达到2n2个电子 |
| B.最外层只有一个电子的原子失去1个电子后,都变成稀有气体元素原子的电子层结构 |
| C.金属元素与非金属元素结合形成的化合物都是离子化合物 |
| D.同主族元素中(稀有气体元素除外),一般原子半径越大,金属性越强 |
更新时间:2023-07-16 16:36:49
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】运用元素周期律分析下面的推断,其中错误的是
| A.硒化氢(H2Se)是无色、有毒、比硫化氢稳定的气体 |
| B.硼的氧化物的水化物可能具有两性 |
| C.砹(At)为有色固体;HAt不稳定;AgAt感光性很强,且不溶于水也不溶于酸 |
| D.Na、K、Rb的金属性依次增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于卤族元素的叙述正确的是
| A.随着核电荷数增加,它们单质的熔点、沸点均逐渐升高 |
B.随着核电荷数的增加,它们单质与 反应的剧烈程度逐渐增大 反应的剧烈程度逐渐增大 |
| C.随着核电荷数的增加,它们相应简单离子的还原性逐渐减弱 |
| D.随着核电荷数的增加,它们的最高价氧化物对应水化物的酸性逐渐增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Y、Z的原子序数和X、Z、W的原子序数均成等差数列,X和Z可形成如图所示的离子,下列说法正确的是


| A.简单离子半径: W>Y>X>Z |
| B.X、W的氢化物的分解温度: X>W |
| C.Y、Z分别与W形成的化合物中化学键类型相同 |
| D.将物质的量为1:2的单质Y、Z投入足量水中,单质Y、Z均完全溶解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期元素X、Y、Z、M的原子序数依次增大,已知元素X的一种高硬度单质是宝石,Y2+电子层结构与氖相同,Z的质子数为偶数,室温下M单质为淡黄色固体。下列叙述不正确的是
| A.M元素位于周期表中的第3周期VIA族 |
| B.Z元素最高价氧化物是制造光导纤维的主要原料 |
| C.化合物XM2 中含有极性共价键和非极性共价键 |
| D.简单离子半径:Y<M |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.2Na2O2+2CO2= 2Na2CO3+O2,该反应同时既有离子键、极性共价键和非极性共价键的断裂又有其形成 |
| B.H2O的热稳定性比H2S强,是由于H2O的分子间作用力较大 |
| C.KCl、HCl、KOH的水溶液都能导电,所以它们都属于离子化合物 |
| D.加热无水Na2CO3固体使之熔化,不需要破坏化学键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】黑火药是中国古代四大发明之一,其爆炸反应为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A. 是共价化合物 是共价化合物 | B.爆炸时吸收热量 |
| C.反应中C作氧化剂 | D.每消耗0.1molS,同时生成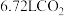 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是 ( )
| A.将过量的氨水加入到CuSO4溶液中,最终得到蓝色沉淀 |
| B.电子排布式(22Ti)1s22s22p63s23p10违反了洪特规则 |
| C.由于氢键的作用,H2O的稳定性强于H2S |
| D.H-Cl的键能为431.8 kJ•mol﹣1,H-I的键能为298.7 kJ•mol﹣1,这可以说明HCl分子比HI分子稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.铅蓄电池中,当正极质量增加6.4g时,电路中通过的电子数为0.2NA |
| B.1L 0.1mol/L的K2CO3溶液中,所含阴离子数目小于0.1NA |
| C.标准状况下22.4L氯化氢气体溶于足量水中,所得溶液中含HCl分子数目为NA |
| D.物质的量相等的基态氧原子和碳原子中,未成对电子数均为2NA |
您最近一年使用:0次

 反应,类比推出
反应,类比推出 反应
反应 可写成
可写成 ,类比推出
,类比推出 可写成
可写成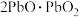
 )的碳循环,如图所示,下列说法错误的是
)的碳循环,如图所示,下列说法错误的是
 过程中形成的是发射光谱
过程中形成的是发射光谱

