金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol•L-1)如图所示。
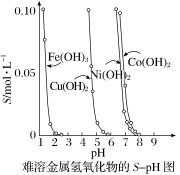
(1)pH=3时溶液中铜元素的主要存在形式是________ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为_______ (填字母)。
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,________ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是_________ 。

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,
更新时间:2023-09-19 14:27:31
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化学在生产生活中有着广泛的应用,请回答下列问题:
(1)家里常用的物品有①厕所清洁剂 ②厨房清洁剂 ③食醋 ④肥皂 ⑤苏打水,其中呈碱性的有________ (填序号)。
(2)浓度均为0.1mol/L的5种溶液:①氨水 ② ③
③ ④
④ ⑤
⑤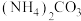 ,其中
,其中 由大到小的顺序为
由大到小的顺序为_________ (用序号表示)。
(3)水垢中含有 ,难用酸除去,可先用
,难用酸除去,可先用 溶液浸泡处理后转化为疏松、易溶于酸的
溶液浸泡处理后转化为疏松、易溶于酸的 ,再用酸处理。用
,再用酸处理。用 溶液浸泡处理的反应为
溶液浸泡处理的反应为__________ (用离子方程式表示)。
(4)牙齿表面有一层坚硬的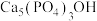 (羟基磷灰石)物质保护着。它在唾液中存在下列平衡:
(羟基磷灰石)物质保护着。它在唾液中存在下列平衡: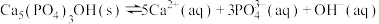 。当人进食后,口腔中的细菌在分解食物的过程中会产生有机酸,这时牙齿就会受到腐蚀,其原因是
。当人进食后,口腔中的细菌在分解食物的过程中会产生有机酸,这时牙齿就会受到腐蚀,其原因是_________________ 。
(1)家里常用的物品有①厕所清洁剂 ②厨房清洁剂 ③食醋 ④肥皂 ⑤苏打水,其中呈碱性的有
(2)浓度均为0.1mol/L的5种溶液:①氨水 ②
 ③
③ ④
④ ⑤
⑤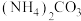 ,其中
,其中 由大到小的顺序为
由大到小的顺序为(3)水垢中含有
 ,难用酸除去,可先用
,难用酸除去,可先用 溶液浸泡处理后转化为疏松、易溶于酸的
溶液浸泡处理后转化为疏松、易溶于酸的 ,再用酸处理。用
,再用酸处理。用 溶液浸泡处理的反应为
溶液浸泡处理的反应为(4)牙齿表面有一层坚硬的
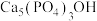 (羟基磷灰石)物质保护着。它在唾液中存在下列平衡:
(羟基磷灰石)物质保护着。它在唾液中存在下列平衡: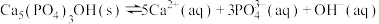 。当人进食后,口腔中的细菌在分解食物的过程中会产生有机酸,这时牙齿就会受到腐蚀,其原因是
。当人进食后,口腔中的细菌在分解食物的过程中会产生有机酸,这时牙齿就会受到腐蚀,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铵盐是实验室常用试剂。回答下列问题:
(1)NH4Cl溶液中 水解的离子方程式为
水解的离子方程式为_____ ;加入镁粉可产生大量气体,该气体的成分是______ (写化学式)。
(2)物质的量浓度相同的下列四种铵盐的溶液中,c( )从大到小的顺序为
)从大到小的顺序为______ (用标号表示)。
A.(NH4)2CO3 B.CH3COONH4 C.NH4HSO4 D.NH4Cl
(3)少量Mg(OH)2能溶于CH3COONH4浓溶液(呈中性)的原因是______ (用文字和方程式说明)。
(4)甲醛法测定铵盐中氮的质量分数的实验步骤如下:步骤I.称取a g (NH4)2SO4样品,用水溶解后定容于250 mL容量瓶中;步骤II.取出25.00 mL溶液于锥形瓶中,加入足量中性甲醛溶液[4 +6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
+6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
①滴定到终点时,溶液颜色的变化是__________ 。
②该(NH4)2SO4样品中氮的质量分数为______ (用含a、c、V的代数式表示)。
③推测下列铵盐中不能用该法测定其中氮的质量分数的是______ (填标号)。
A.NH4Cl B.NH4HCO3 C.NH4NO3 D.CH3COONH4
(1)NH4Cl溶液中
 水解的离子方程式为
水解的离子方程式为(2)物质的量浓度相同的下列四种铵盐的溶液中,c(
 )从大到小的顺序为
)从大到小的顺序为A.(NH4)2CO3 B.CH3COONH4 C.NH4HSO4 D.NH4Cl
(3)少量Mg(OH)2能溶于CH3COONH4浓溶液(呈中性)的原因是
(4)甲醛法测定铵盐中氮的质量分数的实验步骤如下:步骤I.称取a g (NH4)2SO4样品,用水溶解后定容于250 mL容量瓶中;步骤II.取出25.00 mL溶液于锥形瓶中,加入足量中性甲醛溶液[4
 +6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
+6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。①滴定到终点时,溶液颜色的变化是
②该(NH4)2SO4样品中氮的质量分数为
③推测下列铵盐中不能用该法测定其中氮的质量分数的是
A.NH4Cl B.NH4HCO3 C.NH4NO3 D.CH3COONH4
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】镁、铝及其化合物在生产生活中具有重要的作用。
(1)下列实验能比较镁和铝的金属性强弱的是________ (填字母序号)。
a.测定镁和铝的导电性强弱
b.测定等质量的镁片和铝片与相同浓度的盐酸反应的速率
c.向0.1mol/LAlCl3和0.1mol/LMgCl2中加过量NaOH 溶液
(2)镁铝尖品石(MgAl2O4)常做耐火材料。共沉淀制备尖品石的方法是:用AICl3和MgCl2的混合溶液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。为使Mg2+、Al3+同时生成沉淀,应该把________ (填“a”或“b”)滴入另一溶液中。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2,写出反应化学方程式为_____ 。
(4)聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3可制取聚合铝。实验步骤如下:
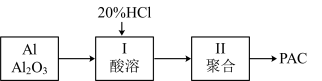
①写出酸溶过程中发生的非氧化还原反应的离子方程式:___________ 。
②聚合铝(PAC)的分子式为[Al2(OH)aCIb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-): 3n(Al3+),当B= 时,b=
时,b=________ 。 (填入合适数字)
③制取聚合铝的方法有多种,若将步骤Ⅰ后的溶液pH直接调制4.2-4.5时,将在过程Ⅱ发生聚合而得到某种聚合铝Alm(OH)nCl3m-n,写出生成该聚合铝的离子反应方程式是__________ 。
(1)下列实验能比较镁和铝的金属性强弱的是
a.测定镁和铝的导电性强弱
b.测定等质量的镁片和铝片与相同浓度的盐酸反应的速率
c.向0.1mol/LAlCl3和0.1mol/LMgCl2中加过量NaOH 溶液
(2)镁铝尖品石(MgAl2O4)常做耐火材料。共沉淀制备尖品石的方法是:用AICl3和MgCl2的混合溶液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。为使Mg2+、Al3+同时生成沉淀,应该把
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2,写出反应化学方程式为
(4)聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3可制取聚合铝。实验步骤如下:

①写出酸溶过程中发生的非氧化还原反应的离子方程式:
②聚合铝(PAC)的分子式为[Al2(OH)aCIb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-): 3n(Al3+),当B=
 时,b=
时,b=③制取聚合铝的方法有多种,若将步骤Ⅰ后的溶液pH直接调制4.2-4.5时,将在过程Ⅱ发生聚合而得到某种聚合铝Alm(OH)nCl3m-n,写出生成该聚合铝的离子反应方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】水溶液中的离子平衡是以化学平衡理论为基础的进一步探究。
(1)常温下,等体积的0.10mol/L氨水与0.10mol/L烧碱溶液相比,c(OH-)的大小关系为前者_____ 后者(填“大于”“等于”或“小于”,下同);常温下,pH均为5的氯化铵溶液与盐酸相比,溶液中水的电离程度前者_____ 后者,两者均稀释10倍,pH的大小关系为前者_____ 后者。
(2)醋酸钠溶液呈碱性,其原因是_____ (用离子方程式表示)。
(3)常温下,Ksp(FeS)=6.3×10-18、Ksp(CuS)=1.3×10-36,则FeS的溶解度_____ CuS的溶解度(填“大于”“等于”或“小于”);在处理含有Cu2+的污水时,可向其中加入FeS固体作为沉淀剂,FeS逐渐溶解,Cu2+转化为CuS沉淀,用沉淀溶解平衡原理解释其原因为_____ 。
(1)常温下,等体积的0.10mol/L氨水与0.10mol/L烧碱溶液相比,c(OH-)的大小关系为前者
(2)醋酸钠溶液呈碱性,其原因是
(3)常温下,Ksp(FeS)=6.3×10-18、Ksp(CuS)=1.3×10-36,则FeS的溶解度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】沉淀溶解平衡在生产、科研和环保等领域有着许多应用。
(1)除去硫酸铜溶液中混有的少量铁离子,可向溶液中加入Cu(OH)2,调节溶液的PH,铁离子就会全部转化为Fe(OH)3沉淀除去。
已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小等于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过计算确定应调节溶液的pH范围是______ 。(已知lg5=0.7)
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度AgSCN>AgI
①写出步骤2中溶液变为红色的离子方程式:____________________ 。
②步骤3中现象a是____________________________ 。
③用化学平衡原理解释步骤4中的实验现象:_________________________________ 。
(1)除去硫酸铜溶液中混有的少量铁离子,可向溶液中加入Cu(OH)2,调节溶液的PH,铁离子就会全部转化为Fe(OH)3沉淀除去。
已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小等于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过计算确定应调节溶液的pH范围是
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度AgSCN>AgI
| 操作步骤 | 现象 |
| 步骤1:向2 mL 0.005 mol·L-1 AgNO3溶液中加入2 mL 0.005 mol·L-1 KSCN溶液,静置 | 出现白色沉淀 |
| 步骤2:取1 mL上层清液于试管中,滴加1滴2 mol·L-1 Fe(NO3)3溶液 | 溶液变为红色 |
| 步骤3:向步骤2的溶液中继续加入5滴3 mol·L-1 AgNO3溶液 | 现象a,溶液红色变浅 |
| 步骤4:向步骤1余下的浊液中加入5滴3 mol·L-1 KI溶液 | 出现黄色沉淀 |
①写出步骤2中溶液变为红色的离子方程式:
②步骤3中现象a是
③用化学平衡原理解释步骤4中的实验现象:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图所示:横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-物质的量浓度的对数,回答下列问题。
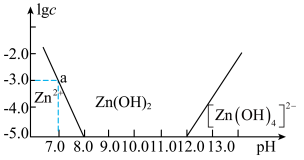
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为___ 。
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=___ 。
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是___ 。
(4)泡沫灭火器内装有NaHCO3饱和溶液;灭火器内另有一容器中装有Al2(SO4) 3溶液,该溶液呈酸性的原因是:___ (用离子方程式表示)。当意外失火时,使泡沫灭火器倒过来即可使药液混合,喷出CO2和Al(OH)3,阻止火势蔓延。其相关化学反应的离子方程式为:___ 。

(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是
(4)泡沫灭火器内装有NaHCO3饱和溶液;灭火器内另有一容器中装有Al2(SO4) 3溶液,该溶液呈酸性的原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡。请根据所学知识回答下列问题:
(1) 的
的 溶液的pH约为4.0,请分析
溶液的pH约为4.0,请分析 溶液显酸性的原因:
溶液显酸性的原因:_______ 。
(2)实验室配制 溶液时,需将
溶液时,需将 溶解在较浓盐酸中,然后加水稀释,这样操作的目的是
溶解在较浓盐酸中,然后加水稀释,这样操作的目的是_______ 。
(3)KCN溶液中存在水解平衡: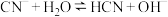 ,25℃时其平衡常数
,25℃时其平衡常数
_______ 。[已知:25℃时,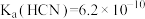 ]
]
(4)已知:25℃时,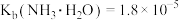 ,
, 的
的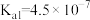 、
、 。则
。则 溶液的pH
溶液的pH_______ (填“>”“<”或“=”)7。
(5)已知:离子的浓度小于 ,可认为该离子不存在;25℃时,
,可认为该离子不存在;25℃时,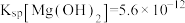 ,
,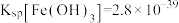 ,某地海水样品经
,某地海水样品经 处理后,所含离子及其浓度如表所示(
处理后,所含离子及其浓度如表所示( 和
和 未列出)。
未列出)。
则a_______ (填“>”“<”或“=”)0.16。
(1)
 的
的 溶液的pH约为4.0,请分析
溶液的pH约为4.0,请分析 溶液显酸性的原因:
溶液显酸性的原因:(2)实验室配制
 溶液时,需将
溶液时,需将 溶解在较浓盐酸中,然后加水稀释,这样操作的目的是
溶解在较浓盐酸中,然后加水稀释,这样操作的目的是(3)KCN溶液中存在水解平衡:
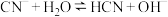 ,25℃时其平衡常数
,25℃时其平衡常数
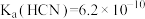 ]
](4)已知:25℃时,
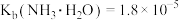 ,
, 的
的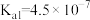 、
、 。则
。则 溶液的pH
溶液的pH(5)已知:离子的浓度小于
 ,可认为该离子不存在;25℃时,
,可认为该离子不存在;25℃时,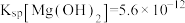 ,
,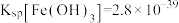 ,某地海水样品经
,某地海水样品经 处理后,所含离子及其浓度如表所示(
处理后,所含离子及其浓度如表所示( 和
和 未列出)。
未列出)。| 离子 |  |  |  |  |  |
浓度/( ) ) | a | 0.05 | 0.10 | 0.50 | 0.58 |
则a
您最近一年使用:0次

 可作为沉淀剂除去废水中的
可作为沉淀剂除去废水中的 ,写出该过程的离子方程式
,写出该过程的离子方程式 还原
还原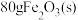 生成
生成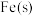 和
和 ,放热
,放热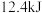 ,请写出该反应的热化学方程式:
,请写出该反应的热化学方程式: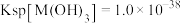 ,要使溶液中的
,要使溶液中的 降至
降至 ,则应调节溶液
,则应调节溶液


