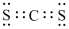离子液体M的结构如图所示,下列说法错误的是
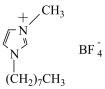

| A.电负性由大到小的顺序是F>N>B |
| B.阴离子的空间结构为正四面体形 |
| C.M因含有机基团而使其熔点较低 |
| D.M分子中C-C键的键能大于C-N键的键能 |
更新时间:2023-08-10 15:51:11
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为18,X、Z基态原子的p轨道上均有2个未成对电子,W与X位于同一主族。下列说法正确的是
| A.WX2分子为极性分子 |
| B.元素电负性:Z>W |
| C.原子半径:r(W)>r(Z)>r(Y) |
| D.最高价氧化物水化物的酸性:Z>W |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知W、X、Y、Z为短周期元素,原子序数依次增大。W、Z同主族,X、Y、Z同周期,其中只有X为金属元素。下列说法一定错误的是
| A.电负性:W>Z>Y>X |
| B.气态氢化物熔沸点:W > Z |
| C.简单离子的半径:W>X>Z |
| D.若X与W原子序数之差为5,则形成化合物的化学式为X3W2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】CsF是离子晶体,其晶格能可通过下图的循环计算得到,以下说法错误的是
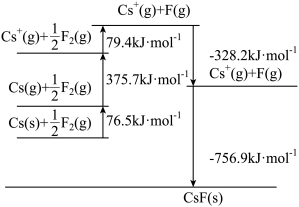

| A.Cs原子的第一电离能为452.2 kJ·mol−1 |
| B.F-F键的键能为158.8 kJ·mol−1 |
| C.CsF的晶格能756.9kJ·mol−1 |
| D.1molCs(s)转变成Cs(g)所要吸收的能量为76.5kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知H2O2分子的空间结构可在二面角中表示(如图所示),则有关H2O2结构的说法不正确 的是
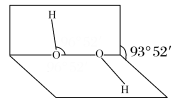
| A.分子中含有极性键和非极性键 | B.H2O2是非极性分子,难溶于水 |
| C.O采用sp3杂化 | D.H-O与O-O形成的键角小于109°28′ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】离子液体是一种由离子构成的液体,在低温下也能以液态存在,是一种很有研究价值的溶剂。研究显示最常见的离子液体主要由如图所示正离子和负离子构成,图中正离子有令人惊奇的稳定性,它的电子在其环外结构中高度离域。下列说法错误的是


| A.图中负离子的空间结构为正四面体形 |
| B.该化合物中存在配位键和氢键 |
| C.离子液体可用作溶剂,且具有良好的导电性 |
| D.图中正离子中碳原子的杂化方式为sp2、sp3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法中正确的是
| A.分子中键能越高,键长越长,则分子越稳定 |
| B.元素周期表中的ⅠA族(除H外)和ⅦA族元素的原子间通常不能形成共价键 |
| C.水分子可表示为H—O—H,分子中键角为180° |
| D.根据等电子原理,CH4和NH3具有相似的化学键特征,物理性质相近。 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各组物质的熔点均与化学键无关的是
| A.CaO与CO2 | B.NaCl与HCl | C.MgO与SiO2 | D.Cl2与I2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在通常条件下,下列比较正确的是
| A.熔点:CO2>KCl>SiO2 | B.水溶性:HCl>CH4>SO2 |
| C.键角:CH4>H2O>NH3 | D.键能:H—F键>H—Cl键>H—Br键 |
您最近一年使用:0次

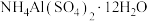 可用作净水剂、媒染剂等。下列说法正确的是
可用作净水剂、媒染剂等。下列说法正确的是
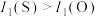
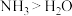
 为平面形分子
为平面形分子 杂化,键角均是120°
杂化,键角均是120° 的热稳定性高于
的热稳定性高于
 在
在 中的溶解度比在水中大
中的溶解度比在水中大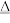 4S2(g)、CH4(g)+2S2(g)=CS2(g)+2H2S(g)制备CS2。下列说法正确的是
4S2(g)、CH4(g)+2S2(g)=CS2(g)+2H2S(g)制备CS2。下列说法正确的是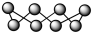 )为极性分子
)为极性分子