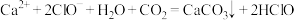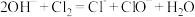焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。利用烟道气中的SO2生产Na2S2O5的工艺为:
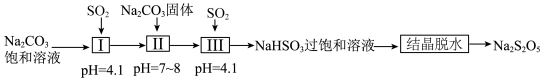
下列对I、II、III中主要发生反应的离子方程式判断错误的是

| 弱电解质 | 电离常数 |
| H2CO3 | Ka1=4.5×10-7,Ka2=4.7×10-11 |
| H2SO3 | Ka1=1.4×10-2,Ka2=6.0×10-8 |
A.I中 +2SO2+H2O=CO2+2 +2SO2+H2O=CO2+2 |
B.II中 +2 +2 =CO2↑+H2O+2 =CO2↑+H2O+2 |
C.III中 +SO2+H2O=2 +SO2+H2O=2 |
D.III中 +SO2=CO2+ +SO2=CO2+ |
更新时间:2023-08-10 15:51:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列离子方程式正确的是
A.加热TiCl4浓溶液制备TiO2·xH2O:Ti4++(x+2)H2O TiO2·xH2O+4H+ TiO2·xH2O+4H+ |
B.(NH4)2Fe(SO4)2溶液中加入少量KOH溶液: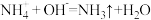 |
| C.钢铁发生吸氧腐蚀时的正极反应:O2+4H++4e-=2H2O |
| D.酸性KI溶液中通入O2:4H++2I-+O2=2H2O+I2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】宏观辨识与微观探析是化学学科核心素养之一、下列表示对应化学反应的离子方程式正确的是
A.向 溶液中滴加稀盐酸: 溶液中滴加稀盐酸: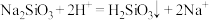 |
B.向NaOH溶液中通入少量 : : |
C.将 气体通入 气体通入 溶液中验证亚硫酸酸性强于次氯酸: 溶液中验证亚硫酸酸性强于次氯酸: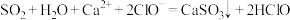 |
D.过量的Fe和稀硝酸反应: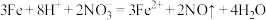 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某溶液中存在较多的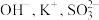 ,该溶液中还可能大量存在的离子是
,该溶液中还可能大量存在的离子是
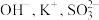 ,该溶液中还可能大量存在的离子是
,该溶液中还可能大量存在的离子是A. | B. | C. | D. |
您最近半年使用:0次
【推荐2】下列离子在未知溶液中的检验方法正确的是
| 离子 | 检验方法 | |
| A | CO | 加入足量盐酸,将生成的无色无味气体通入澄清石灰水,观察是否变浑浊 |
| B | SO | 先加入稀硝酸,再滴加氯化钡溶液,观察是否有白色沉淀生成 |
| C | Ag+ | 加入NaCl溶液,观察是否有白色沉淀生成 |
| D | HSO | 加入BaCl2溶液,无明显现象,再加入稀盐酸,产生能使澄清石灰水变浑浊的刺激性气味气体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】“价—类”二维图是研究物质性质的一种方法,下图是a~f表示的是含硫物质。下列说法正确的是
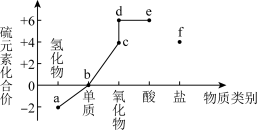

| A.a可用硫化亚铁与稀硝酸反应制取 |
| B.b在足量的纯氧中燃烧,可一步转化为d |
| C.c能使溴水褪色,证明c有漂白性 |
| D.f既有氧化性又有还原性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,已知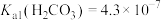 ,
, 。某二元酸
。某二元酸 及其钠盐的溶液中,
及其钠盐的溶液中, 、
、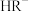 、
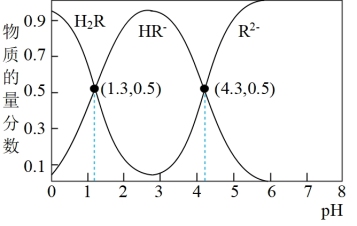
、 三者的物质的量分数随溶液pH变化关系如图所示。下列叙述正确的是
三者的物质的量分数随溶液pH变化关系如图所示。下列叙述正确的是
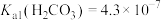 ,
, 。某二元酸
。某二元酸 及其钠盐的溶液中,
及其钠盐的溶液中, 、
、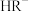 、
、 三者的物质的量分数随溶液pH变化关系如图所示。下列叙述正确的是
三者的物质的量分数随溶液pH变化关系如图所示。下列叙述正确的是
A. 的电离平衡常数 的电离平衡常数 |
B.向 溶液中加入少量 溶液中加入少量 溶液,发生的反应是: 溶液,发生的反应是: |
C.等体积、等浓度的NaOH溶液与 溶液混合后,溶液中: 溶液混合后,溶液中: |
D.在 的溶液中: 的溶液中: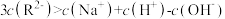 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
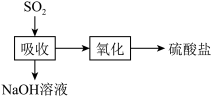
【推荐2】一种吸收SO2再经氧化得到硫酸盐的过程如图所示。室温下,用0.1mol。L-1NaOH溶液吸收SO2,若通入SO2所引起的溶液体积变化和H2O挥发可忽略,溶液中含硫物种的浓度c总=c(H2SO3)+c(HSO ))+c(SO
))+c(SO )。H2SO3的电离常数分别为Ka1=1.29x10-2,Ka2=6.24×10-8。下列说法正确的是
)。H2SO3的电离常数分别为Ka1=1.29x10-2,Ka2=6.24×10-8。下列说法正确的是
 ))+c(SO
))+c(SO )。H2SO3的电离常数分别为Ka1=1.29x10-2,Ka2=6.24×10-8。下列说法正确的是
)。H2SO3的电离常数分别为Ka1=1.29x10-2,Ka2=6.24×10-8。下列说法正确的是
A.“吸收”所得溶液中:c(Na+)+C(H+)=c(HSO )+c(SO )+c(SO )+c(OH-) )+c(OH-) |
| B.若“吸收”所得溶液中c总=0.1mol・L-1溶液中:Kw>Ka1・Ka2 |
C.若“吸收"所得溶液pH=7,则溶液中c(SO )>c(H2SO3) )>c(H2SO3) |
D.“氧化”时调节溶液pH约为5,主要发生反应2SO +O2=2 +O2=2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
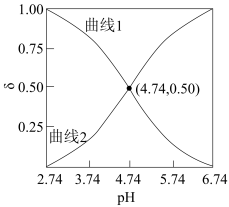
【推荐3】25℃,醋酸溶液中CH3COOH、CH3COO-的分布系数δ与pH的关系如图。其中,δ(CH3COO-)= 。下列叙述错误的是
。下列叙述错误的是
 。下列叙述错误的是
。下列叙述错误的是
| A.曲线2代表δ(CH3COO-) |
| B.25℃,CH3COOH的电离常数Ka=10-4.74 |
C.δ(CH3COOH)=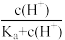 |
| D.该关系图不适用于CH3COOH、CH3COONa混合溶液 |
您最近半年使用:0次

 :
: