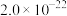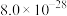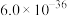锌的化学性质与铝相似,工业上有较高的利用价值。某含锌废催化剂的主要成分为氧化锌,还含有镍、铁、铅等元素杂质,采用“氨浸除杂蒸发煅烧”新工艺生产高纯碱式碳酸锌,达到了废物综合利用的目的,工艺流程如图,请回答下列问题。
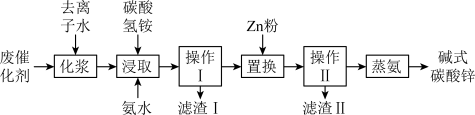
已知:“浸取”步骤后生成了锌氨配合物(配位数为4)和镍氨配合物进行后续生产。
(1) 的电子排布式为
的电子排布式为______ 。
(2)“浸取”步骤中,废催化剂中氧化锌发生反应的化学方程式为______ 。
(3)“浸取”中锌的浸出率对本工艺至关重要,图一、图二是锌浸出率分别受温度、氨水与碳酸氢铵比(氮元素浓度固定)的影响。请分析:
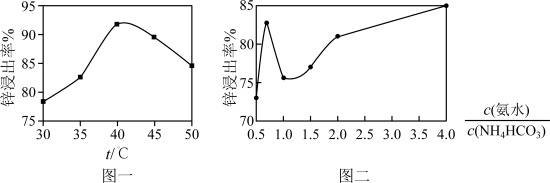
(1)图一中选择的适宜温度为42℃左右,温度不宜过高的原因是______ 。
(2)图二中随着氨水与碳酸氢铵比的增大,锌的浸出率先增大后减小,然后再增大。
当 时,溶液
时,溶液 值升高,锌的主要存在形式为
值升高,锌的主要存在形式为______ 。
(4)滤渣Ⅱ的成分为过量的 外,还有
外,还有______ 。(填化学式)
(5)“蒸氨”操作中锌氨溶液最终以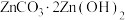 形式从溶液中析出,经过滤洗涤、干燥后得到碱式碳酸锌,其化学反应方程式为:
形式从溶液中析出,经过滤洗涤、干燥后得到碱式碳酸锌,其化学反应方程式为:______ 。
(6)整个过程中可以循环利用的物质为______ 。

已知:“浸取”步骤后生成了锌氨配合物(配位数为4)和镍氨配合物进行后续生产。
(1)
 的电子排布式为
的电子排布式为(2)“浸取”步骤中,废催化剂中氧化锌发生反应的化学方程式为
(3)“浸取”中锌的浸出率对本工艺至关重要,图一、图二是锌浸出率分别受温度、氨水与碳酸氢铵比(氮元素浓度固定)的影响。请分析:

(1)图一中选择的适宜温度为42℃左右,温度不宜过高的原因是
(2)图二中随着氨水与碳酸氢铵比的增大,锌的浸出率先增大后减小,然后再增大。
当
 时,溶液
时,溶液 值升高,锌的主要存在形式为
值升高,锌的主要存在形式为(4)滤渣Ⅱ的成分为过量的
 外,还有
外,还有(5)“蒸氨”操作中锌氨溶液最终以
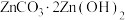 形式从溶液中析出,经过滤洗涤、干燥后得到碱式碳酸锌,其化学反应方程式为:
形式从溶液中析出,经过滤洗涤、干燥后得到碱式碳酸锌,其化学反应方程式为:(6)整个过程中可以循环利用的物质为
更新时间:2023-08-16 18:15:08
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】铜元素是一种金属化学元素,也是人体所必须的一种微量元素, 铜也是人类最早发现的金属,是人类广泛使用的一种金属,属于重金属。
(1)写出基态铜原子的价层电子排布式_________________ 。
(2)简单金属离子在水溶液中的颜色大多与价层电子中含有的未成对电子数有关,如Fe3+呈黄色,Fe2+呈绿色,Cu2+呈蓝色等。预测Cu+为_____ 色,解释原因________________ 。
(3)X射线研究证明,CuCl2的结构为链状,如图所示,它含有的化学键类型为_________ ,在它的水溶液中加入过量氨水,得到 [Cu(NH3)4]Cl2溶液, [Cu(NH3)4]Cl2中H-N-H的夹角_________ (填“大于”、“等于”或“小于”)NH3分子中的H-N-H的夹角,原因是___________ 。
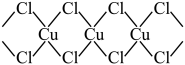
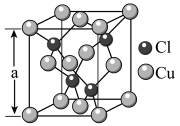
(4)某种铜的氯化物晶体结构如图:此晶体中铜原子的配位数是__________ ,若氯原子位于铜形成的四面体的体心,且铜原子与铜原子、铜原子与氯原子都是采取最密堆积方式,则氯原子与铜原子半径之比为__________________ 。
(1)写出基态铜原子的价层电子排布式
(2)简单金属离子在水溶液中的颜色大多与价层电子中含有的未成对电子数有关,如Fe3+呈黄色,Fe2+呈绿色,Cu2+呈蓝色等。预测Cu+为
(3)X射线研究证明,CuCl2的结构为链状,如图所示,它含有的化学键类型为

(4)某种铜的氯化物晶体结构如图:此晶体中铜原子的配位数是

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】工业上,从铜镍矿(主要成分为铜氧化物、镍氧化物,含有 、
、 、
、 等杂质)中提取镍和铜的一种工艺流程如下:
等杂质)中提取镍和铜的一种工艺流程如下:
②当溶液中某离子浓度c≤10-5mol/L时,可认为该离子沉淀完全。
③
(1)基态 原子的价电子排布图为
原子的价电子排布图为___________ 。
(2)浸出过程中通入 的目的是
的目的是___________ 。
(3)萃取时发生反应: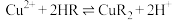 (HR、CuR2在有机层,
(HR、CuR2在有机层, 在水层)。
在水层)。___________ 。
(4)写出用惰性电极电解 溶液发生反应的化学方程式:
溶液发生反应的化学方程式:___________ 。
(5)黄钠铁矾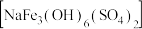 比
比 更易形成沉淀,则生成黄钠铁矾的离子方程式是
更易形成沉淀,则生成黄钠铁矾的离子方程式是___________ 。
(6)第二次使用 调节溶液
调节溶液 ,使
,使 沉淀完全,应将
沉淀完全,应将 调节至
调节至___________ (保留2位小数)。
 、
、 、
、 等杂质)中提取镍和铜的一种工艺流程如下:
等杂质)中提取镍和铜的一种工艺流程如下: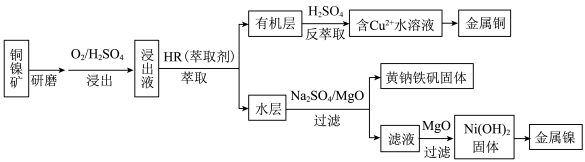
| 物质 |  |  |  |  |
 |  |  |  | 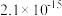 |
③

(1)基态
 原子的价电子排布图为
原子的价电子排布图为(2)浸出过程中通入
 的目的是
的目的是(3)萃取时发生反应:
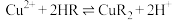 (HR、CuR2在有机层,
(HR、CuR2在有机层, 在水层)。
在水层)。①某种 的结构简式为
的结构简式为 ,该分子中可能与
,该分子中可能与 形成配位键的原子有
形成配位键的原子有
(4)写出用惰性电极电解
 溶液发生反应的化学方程式:
溶液发生反应的化学方程式:(5)黄钠铁矾
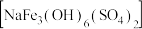 比
比 更易形成沉淀,则生成黄钠铁矾的离子方程式是
更易形成沉淀,则生成黄钠铁矾的离子方程式是(6)第二次使用
 调节溶液
调节溶液 ,使
,使 沉淀完全,应将
沉淀完全,应将 调节至
调节至
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】近期我国学者研制出低成本的电解“水制氢”催化剂——镍掺杂的磷化钴三元纳米片电催化剂(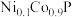 )。回答下列问题:
)。回答下列问题:
(1)Co在元素周期表中的位置为_________ ,Co2+价层电子排布式为______________ 。
(2)Co、Ni可形成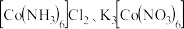 、
、 、
、 等多种配合物。
等多种配合物。
① 的空间构型为
的空间构型为__________ , 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为_________ 。
②C、N、O、S四种元素中,第一电离能最大的是_____________ 。
③ 中含有σ键的数目为
中含有σ键的数目为__________ ;已知NF3比NH3的沸点小得多,试解释原因________________________________________ 。
(3)常用丁二酮肟来检验Ni2+,反应如下:
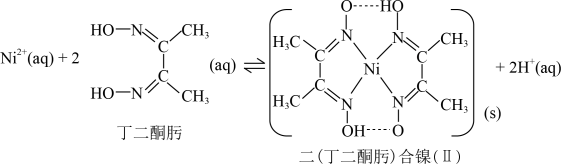
①1个二(丁二酮肟)合镍(Ⅱ)中含有_________________ 个配位键。
②上述反应的适宜 为
为_________________ (填字母序号)
A.12 B.5~10 C.1

(4)磷化硼是一种备受关注的耐磨涂料,其晶体中磷原子作面心立方最密堆积,硼原子填入四面体空隙中(如图)。已知磷化硼晶体密度为 ,计算晶体中硼原子和磷原子的最近核间距为
,计算晶体中硼原子和磷原子的最近核间距为___________  。
。
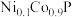 )。回答下列问题:
)。回答下列问题:(1)Co在元素周期表中的位置为
(2)Co、Ni可形成
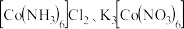 、
、 、
、 等多种配合物。
等多种配合物。①
 的空间构型为
的空间构型为 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为②C、N、O、S四种元素中,第一电离能最大的是
③
 中含有σ键的数目为
中含有σ键的数目为(3)常用丁二酮肟来检验Ni2+,反应如下:

①1个二(丁二酮肟)合镍(Ⅱ)中含有
②上述反应的适宜
 为
为A.12 B.5~10 C.1

(4)磷化硼是一种备受关注的耐磨涂料,其晶体中磷原子作面心立方最密堆积,硼原子填入四面体空隙中(如图)。已知磷化硼晶体密度为
 ,计算晶体中硼原子和磷原子的最近核间距为
,计算晶体中硼原子和磷原子的最近核间距为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】碱式碳酸铋片[主要成分(BiO)2CO3]可用于治疗慢性胃炎及缓解胃酸过多引起的胃病。由菱铋矿(主要成分为nBi2O3·mCO2·H2O,含杂质SiO2、CuS等)制备(BiO)2CO3的一种工艺如图:
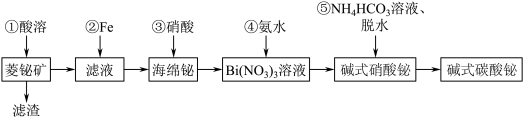
试回答下列问题:
(1)为提高①的“酸溶”速率,可以采取的措施是__________ (任写一种)。
(2)①中酸溶解率与接触时间及溶液的pH之间的关系如图,据此分析,“酸溶”的最佳条件为__________ ;滤渣的主要成分是__________ 。

(3)“酸溶”后溶液必须保持强酸性,以防止铋元素流失,原理是__________ 。
(4)②中得到“海绵铋”的离子方程式为__________ 。
(5)④中反应的化学反应方程式为__________ 。
(6)25℃时,向浓度均为0.1mol·L-1的Fe2+、Cu2+、Bi3+的混合溶液中滴加Na2S溶液,当Fe2+恰好沉淀完全时,所得溶液c(Cu2+):c(Bi3+)=__________ 。(忽略Na2S溶液所带来的体积变化)。
资料:①有关溶度积数据见表:
②溶液中的离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全。

试回答下列问题:
(1)为提高①的“酸溶”速率,可以采取的措施是
(2)①中酸溶解率与接触时间及溶液的pH之间的关系如图,据此分析,“酸溶”的最佳条件为

(3)“酸溶”后溶液必须保持强酸性,以防止铋元素流失,原理是
(4)②中得到“海绵铋”的离子方程式为
(5)④中反应的化学反应方程式为
(6)25℃时,向浓度均为0.1mol·L-1的Fe2+、Cu2+、Bi3+的混合溶液中滴加Na2S溶液,当Fe2+恰好沉淀完全时,所得溶液c(Cu2+):c(Bi3+)=
资料:①有关溶度积数据见表:
| 难溶物质 | FeS | CuS | Bi2S3 |
| Ksp(25℃) | 6.3×10-18 | 6.3×10-36 | 1.6×10-20 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】某铜钴矿石主要含有CoOOH、CoCO3、Cu2(OH)2CO3和SiO2,其中还含有一定量的Fe2O3、MgO和CaO等。由该矿石制备Co2O3的部分工艺过程如下:
I.将粉碎的矿石用过量的稀H2SO4和Na2SO3溶液浸泡,过滤,分离除去沉淀a。
II.浸出液除去含铜的化合物后,向溶液中先加入NaClO3溶液,再加入一定浓度的Na2CO3溶液,过滤,分离除去沉淀b[主要成分是Na2Fe6(SO4)4(OH)12]。
III.向上述滤液中加入足量NaF溶液,过滤,分离除去沉淀c。
IV.III中滤液加入浓Na2CO3溶液,获得CoCO3沉淀。
V.将CoCO3溶解在盐酸中,再加入(NH4)2C2O4溶液,产生 CoC2O4·2H2O沉淀。分离出沉淀,将其在400℃~600℃ 煅烧,即得到Co2O3。
请回答:
(1)I 中,沉淀a的成分是_____ ,稀硫酸溶解CoCO3的化学方程式是_____ , 加入Na2SO3溶液的主要作用是_________ 。
(2)根据图1、图2分析:
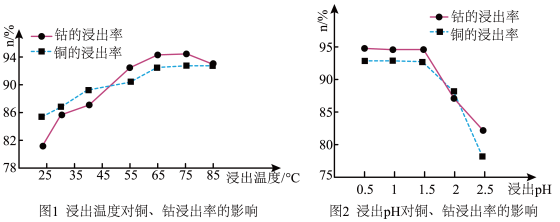
①矿石粉末浸泡的适宜条件应是:温度_____ 、pH_____ 。
②图2中铜、钴浸出率下降的可能原因是_____ 。
(3)II中,浸出液中的金属离子与NaClO3反应的离子方程式:ClO +
+_____ +_____ == Cl- +_____ + _____
(4)I中,检验铁元素完全除去的试剂是_____ ,实验现象是_____ 。
(5)I中,沉淀c的成分是CaF2、_____ (填化学式)。
(6)V中,加入Na2CO3的作用是_____ 。
(7)V中,分离出纯净的CoC2O4·2H2O的操作是_____ 。
I.将粉碎的矿石用过量的稀H2SO4和Na2SO3溶液浸泡,过滤,分离除去沉淀a。
II.浸出液除去含铜的化合物后,向溶液中先加入NaClO3溶液,再加入一定浓度的Na2CO3溶液,过滤,分离除去沉淀b[主要成分是Na2Fe6(SO4)4(OH)12]。
III.向上述滤液中加入足量NaF溶液,过滤,分离除去沉淀c。
IV.III中滤液加入浓Na2CO3溶液,获得CoCO3沉淀。
V.将CoCO3溶解在盐酸中,再加入(NH4)2C2O4溶液,产生 CoC2O4·2H2O沉淀。分离出沉淀,将其在400℃~600℃ 煅烧,即得到Co2O3。
请回答:
(1)I 中,沉淀a的成分是
(2)根据图1、图2分析:

①矿石粉末浸泡的适宜条件应是:温度
②图2中铜、钴浸出率下降的可能原因是
(3)II中,浸出液中的金属离子与NaClO3反应的离子方程式:ClO
 +
+(4)I中,检验铁元素完全除去的试剂是
(5)I中,沉淀c的成分是CaF2、
(6)V中,加入Na2CO3的作用是
(7)V中,分离出纯净的CoC2O4·2H2O的操作是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】硝矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O及少量氧化铁。
利用明矾石制备K2SO4的工艺流程如下所示:
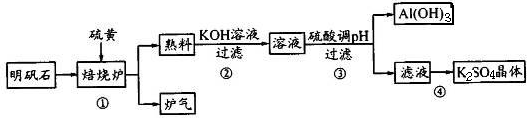
(1)焙烧炉中发生如下反应,请在方程式中表示出电子转移的方向和数目____________________
2Al2(SO4)3+3S 2Al2O3+9SO2↑
2Al2O3+9SO2↑
(2)步骤②涉及Al2O3的离子方程式为____________________ 。
(3)步骤③调pH生成AI{OH)。的离子方程式为____________________ ;不能用CO2来调pH,理由是____________________ .
(4)步骤④的主要操作步骤是____________________ ,过滤、洗涤和干燥
(5)炉气回收可做多种用途,请举一例:____________________ 。
利用明矾石制备K2SO4的工艺流程如下所示:

(1)焙烧炉中发生如下反应,请在方程式中表示出电子转移的方向和数目
2Al2(SO4)3+3S
 2Al2O3+9SO2↑
2Al2O3+9SO2↑(2)步骤②涉及Al2O3的离子方程式为
(3)步骤③调pH生成AI{OH)。的离子方程式为
(4)步骤④的主要操作步骤是
(5)炉气回收可做多种用途,请举一例:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】 和
和 是非常重要的化工原料,可利用锌精矿(主要成分为ZnS)和软锰矿(主要成分为
是非常重要的化工原料,可利用锌精矿(主要成分为ZnS)和软锰矿(主要成分为 )联合制备,其杂质的组成基本相似,包括
)联合制备,其杂质的组成基本相似,包括 、PbO和Fe、Cu的氧化物等。工艺流程如下:
、PbO和Fe、Cu的氧化物等。工艺流程如下:
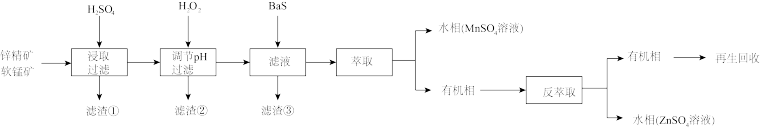
已知:
I.常温下,一些难溶电解质的溶度积常数如下表:
II.反萃取:是萃取的逆过程,即被萃取物从有机相返回水相的过程。
回答下列问题:
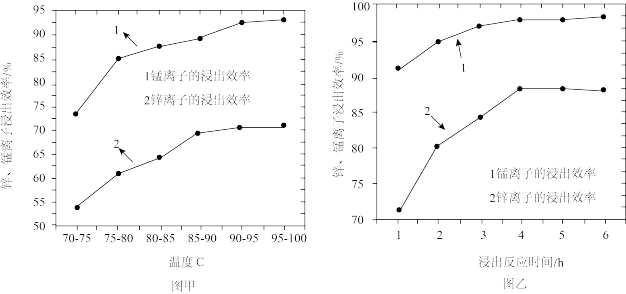
(1)浸取过程中温度和时间对锌和锰浸出率的影响如图甲和图乙所示。从浸出率和节约原料的角度考虑,适宜的浸出温度和时间分别为______________ 、______________ 。
(2)已知滤渣①中含有硫单质,锌精矿和软锰矿在硫酸中浸取生成 和
和 的化学方程式为
的化学方程式为_________ 。
(3)加入 的目的是
的目的是______________ (用离子方程式表示)。
(4)将浸取液的pH调节为5左右,使 形成沉淀而除去,可选用的试剂为 (填字母)
形成沉淀而除去,可选用的试剂为 (填字母)
(5)滤渣③的主要成分是______________ 。
(6)若除铁液中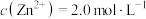 ,加入BaS溶液后,恰好沉淀完成,此时是否有ZnS沉淀生成?
,加入BaS溶液后,恰好沉淀完成,此时是否有ZnS沉淀生成?_____________ (列式计算)。已知当溶液中离子浓度小于 ,认为沉淀完全。
,认为沉淀完全。
(7)从 水相经过
水相经过________ ,过滤,洗涤,干燥等实验操作可以得到 。
。
 和
和 是非常重要的化工原料,可利用锌精矿(主要成分为ZnS)和软锰矿(主要成分为
是非常重要的化工原料,可利用锌精矿(主要成分为ZnS)和软锰矿(主要成分为 )联合制备,其杂质的组成基本相似,包括
)联合制备,其杂质的组成基本相似,包括 、PbO和Fe、Cu的氧化物等。工艺流程如下:
、PbO和Fe、Cu的氧化物等。工艺流程如下:
已知:
I.常温下,一些难溶电解质的溶度积常数如下表:
难溶电解质 | ZnS | MnS | PbS | CuS |
|
|
|
|
|
回答下列问题:
(1)浸取过程中温度和时间对锌和锰浸出率的影响如图甲和图乙所示。从浸出率和节约原料的角度考虑,适宜的浸出温度和时间分别为

(2)已知滤渣①中含有硫单质,锌精矿和软锰矿在硫酸中浸取生成
 和
和 的化学方程式为
的化学方程式为(3)加入
 的目的是
的目的是(4)将浸取液的pH调节为5左右,使
 形成沉淀而除去,可选用的试剂为 (填字母)
形成沉淀而除去,可选用的试剂为 (填字母)A. | B.ZnO | C.NaOH | D.MnO |
(6)若除铁液中
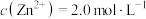 ,加入BaS溶液后,恰好沉淀完成,此时是否有ZnS沉淀生成?
,加入BaS溶液后,恰好沉淀完成,此时是否有ZnS沉淀生成? ,认为沉淀完全。
,认为沉淀完全。(7)从
 水相经过
水相经过 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
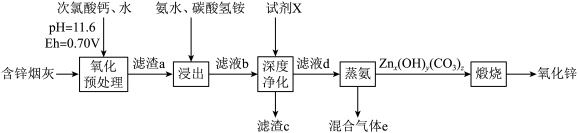
【推荐2】氧化锌是一种白色粉末,可溶于酸、氢氧化钠溶液、氨水和氨水-铵盐缓冲溶液中,它在橡胶、涂料、医疗及食品等行业有着广泛应用。一种由含锌烟灰(含有ZnO、CuO、PbO、FeO、 、MnO、
、MnO、 、CdO等)制备氧化锌工艺如图:
、CdO等)制备氧化锌工艺如图:
ⅰ)二价金属氧化物如Fe(Ⅱ)、Mn(Ⅱ)与氨络合可生成 、
、 ;
;
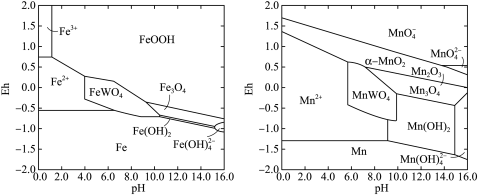
ⅱ)Fe、Mn元素对应优势微粒与溶液的pH及氧化剂氧化电位(Eh)关系如图:
(1) 基态核外电子能级共
基态核外电子能级共_____ 个。
(2)“氧化预处理”时,加入 溶液的目的为将含锌烟灰中的铁(Ⅱ)和锰(Ⅱ)分别氧化,写出氧化铁(Ⅱ)的离子方程式为
溶液的目的为将含锌烟灰中的铁(Ⅱ)和锰(Ⅱ)分别氧化,写出氧化铁(Ⅱ)的离子方程式为_____ 。
(3)“浸出”时生成多种配离子,其中生成 的离子方程式为
的离子方程式为_____ 。
(4)“深度净化”时,可采用加入足量锌粉。该方案所得滤渣c中除了含Zn、Cd之外,还含有(填化学式)_____ 。
(5)“蒸氨”时得混合气体e和固体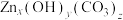 。气体e可返回至
。气体e可返回至_____ 工序循环利用;取11.2固体,经充分“煅烧”后得到氧化锌8.1g,同时产生的气体通入到足量 溶液中,得沉淀9.85g,则固体
溶液中,得沉淀9.85g,则固体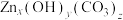 的化学式为
的化学式为_____ 。
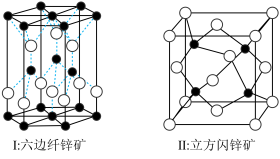
(6)氧化锌有六边纤锌矿和立方闪锌矿两种常见晶体结构,晶胞结构如图。六边纤锌矿和立方闪锌矿中锌的配位数分别为_____ 、_____ 。
 、MnO、
、MnO、 、CdO等)制备氧化锌工艺如图:
、CdO等)制备氧化锌工艺如图:
ⅰ)二价金属氧化物如Fe(Ⅱ)、Mn(Ⅱ)与氨络合可生成
 、
、 ;
;ⅱ)Fe、Mn元素对应优势微粒与溶液的pH及氧化剂氧化电位(Eh)关系如图:

(1)
 基态核外电子能级共
基态核外电子能级共(2)“氧化预处理”时,加入
 溶液的目的为将含锌烟灰中的铁(Ⅱ)和锰(Ⅱ)分别氧化,写出氧化铁(Ⅱ)的离子方程式为
溶液的目的为将含锌烟灰中的铁(Ⅱ)和锰(Ⅱ)分别氧化,写出氧化铁(Ⅱ)的离子方程式为(3)“浸出”时生成多种配离子,其中生成
 的离子方程式为
的离子方程式为(4)“深度净化”时,可采用加入足量锌粉。该方案所得滤渣c中除了含Zn、Cd之外,还含有(填化学式)
(5)“蒸氨”时得混合气体e和固体
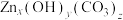 。气体e可返回至
。气体e可返回至 溶液中,得沉淀9.85g,则固体
溶液中,得沉淀9.85g,则固体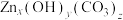 的化学式为
的化学式为(6)氧化锌有六边纤锌矿和立方闪锌矿两种常见晶体结构,晶胞结构如图。六边纤锌矿和立方闪锌矿中锌的配位数分别为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
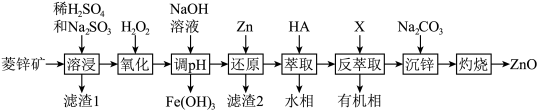
【推荐3】ZnO是一种难溶于水的白色固体,在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上由菱锌矿(主要成分为ZnCO3、ZnO,还含有少量Ni2O3、FeO、MgCO3、PbO2等杂质)制备ZnO的工艺流程如图所示:
②“溶浸”后的溶液所含金属离子主要有:Zn2+、Fe2+、Ni2+、Mg2+;
③氧化性顺序:Ni2+>Zn2+。
回答下列问题:
(1)基态Zn原子核外电子排布式为___________ 。
(2)滤渣1的化学式是___________ ,“溶浸”过程中Ni2O3发生反应的离子方程式是___________ 。
(3)已知“氧化”后溶液中c(Zn2+)=1.2mol·L-1,“调pH”的pH范围是___________ (保留两位有效数字)。(已知:溶液中离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是___________ 。
(4)有机萃取剂HA与ZnSO4反应的化学方程式为2HA+ZnSO4 ZnA2+H2SO4,则“反萃取”时加入试剂X的化学式是
ZnA2+H2SO4,则“反萃取”时加入试剂X的化学式是___________ 。
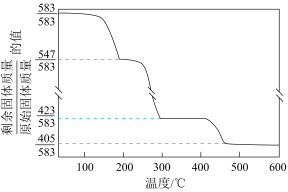
(5)在“沉锌”与“灼烧”之间进行的操作是___________ ,“沉锌”得到碱式碳酸锌[化学式为2ZnCO3·3Zn(OH)2·2H2O],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是___________ (填化学式)。
②“溶浸”后的溶液所含金属离子主要有:Zn2+、Fe2+、Ni2+、Mg2+;
③氧化性顺序:Ni2+>Zn2+。
回答下列问题:
(1)基态Zn原子核外电子排布式为
(2)滤渣1的化学式是
(3)已知“氧化”后溶液中c(Zn2+)=1.2mol·L-1,“调pH”的pH范围是
(4)有机萃取剂HA与ZnSO4反应的化学方程式为2HA+ZnSO4
 ZnA2+H2SO4,则“反萃取”时加入试剂X的化学式是
ZnA2+H2SO4,则“反萃取”时加入试剂X的化学式是(5)在“沉锌”与“灼烧”之间进行的操作是
您最近一年使用:0次