硼是第ⅢA族唯一的非金属元素,是农作物生长必需的微量营养元素。硼的单质及化合物都有重要用途。回答下列问题:
(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别是___________ 、___________ (填标号)。
A. B.
B. 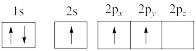
C. D.
D.
(2)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图所示),若其中有两个原子为 ,其余为
,其余为 ,则该结构单元有
,则该结构单元有___________ 种不同的结构类型。

(3)氨硼烷( )含氢量高热稳定性好,是一种具有潜力的固体储氢材料。
)含氢量高热稳定性好,是一种具有潜力的固体储氢材料。
①在第二周期中,第一电离能介于B和N之间的有___________ 种元素。
②原子个数和价电子数目均相等的微粒互称为等电子体。则与 电子数也相等的等电子体分子是
电子数也相等的等电子体分子是___________ (写分子式)。
(4)硼酸是一元弱酸,但 本身不能电离,只能通过结合来自水中的
本身不能电离,只能通过结合来自水中的 而释放出
而释放出 ,则在水溶液中
,则在水溶液中 的电离方程式为
的电离方程式为___________ 。
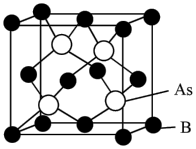
(5)硼与第ⅤA族元素组成的化合物氮化硼(BN)、磷化硼(BP)、砷化硼(BAs)的晶体结构与单晶硅相似,其中氮化硼(BN)和磷化硼(BP)是受到高度关注的耐磨涂料,砷化硼(BAs)是一种超高热导率半导体材料。
①氮化硼晶体的熔点要比磷化硼晶体高,其原因是___________ 。
②砷化硼(BAs)的晶胞结构如下图所示,已知阿伏加德罗常数的值为 ,若晶胞中B原子到As原子最近距离为a pm,则该晶体的密度ρ=
,若晶胞中B原子到As原子最近距离为a pm,则该晶体的密度ρ=___________  (列出含a、
(列出含a、 的计算式即可)。
的计算式即可)。
(6)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点,B点原子的分数坐标分别为(0,0,0)、(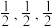 ),则C点原子的分数坐标为
),则C点原子的分数坐标为___________ 晶胞中C、D间距离
___________  。
。

(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别是
A.
 B.
B. 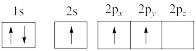
C.
 D.
D.
(2)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图所示),若其中有两个原子为
 ,其余为
,其余为 ,则该结构单元有
,则该结构单元有
(3)氨硼烷(
 )含氢量高热稳定性好,是一种具有潜力的固体储氢材料。
)含氢量高热稳定性好,是一种具有潜力的固体储氢材料。①在第二周期中,第一电离能介于B和N之间的有
②原子个数和价电子数目均相等的微粒互称为等电子体。则与
 电子数也相等的等电子体分子是
电子数也相等的等电子体分子是(4)硼酸是一元弱酸,但
 本身不能电离,只能通过结合来自水中的
本身不能电离,只能通过结合来自水中的 而释放出
而释放出 ,则在水溶液中
,则在水溶液中 的电离方程式为
的电离方程式为(5)硼与第ⅤA族元素组成的化合物氮化硼(BN)、磷化硼(BP)、砷化硼(BAs)的晶体结构与单晶硅相似,其中氮化硼(BN)和磷化硼(BP)是受到高度关注的耐磨涂料,砷化硼(BAs)是一种超高热导率半导体材料。
①氮化硼晶体的熔点要比磷化硼晶体高,其原因是
②砷化硼(BAs)的晶胞结构如下图所示,已知阿伏加德罗常数的值为
 ,若晶胞中B原子到As原子最近距离为a pm,则该晶体的密度ρ=
,若晶胞中B原子到As原子最近距离为a pm,则该晶体的密度ρ= (列出含a、
(列出含a、 的计算式即可)。
的计算式即可)。
(6)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为
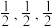 ),则C点原子的分数坐标为
),则C点原子的分数坐标为
 。
。
更新时间:2023-08-30 09:47:54
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】周期表前四周期的元素a、b、c、d、e,原子序数依次增大,b2a4常做火箭推进剂的燃料,c是地壳中含量最多的元素,d2+离子3d轨道中有6个电子,e单质不溶于稀硫酸,常用作电缆材料。回答下列问题:
(1)区别晶体和非晶体最科学的方法是_______ 。
(2)a2c的VSEPR模型为_______ ,d3+比d2+稳定的原因是_______ 。
(3)向e2+硫酸盐的水溶液中加入过量的氨水,可得到深蓝色透明溶液,加入乙醇可析出深蓝色晶体。该深蓝色晶体是_______ (化学式),写出上述过程中发生反应的离子方程式__________________________________ , _____________________________________ 。
(4)已知某化合物是由b和d两种元素组成的晶体,其晶胞结构如图所示,则该晶体的化学式为_______ 。若该晶体的密度是ρ g/cm3,则晶胞中两个最近的 d的核间距为__________________ cm(用含ρ的代数式表示)

(1)区别晶体和非晶体最科学的方法是
(2)a2c的VSEPR模型为
(3)向e2+硫酸盐的水溶液中加入过量的氨水,可得到深蓝色透明溶液,加入乙醇可析出深蓝色晶体。该深蓝色晶体是
(4)已知某化合物是由b和d两种元素组成的晶体,其晶胞结构如图所示,则该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】回答下列问题:
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2);2CHCl3+O2→2HCl+2COCl2,光气(COCl2)分子的立体构型是___________ 形。
(2)某有机物的结构简式为 该有机物分子是
该有机物分子是___________ (填“极性”或“非极性”)分子
(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为___________ ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高很多,原因___________ ;
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为N2H4+HNO2=2H2O+HN3;HN3的酸性和醋酸相近,可微弱电离出H+和N 。下列有关说法正确的是___________(填序号)。
。下列有关说法正确的是___________(填序号)。
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2);2CHCl3+O2→2HCl+2COCl2,光气(COCl2)分子的立体构型是
(2)某有机物的结构简式为
 该有机物分子是
该有机物分子是(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为N2H4+HNO2=2H2O+HN3;HN3的酸性和醋酸相近,可微弱电离出H+和N
 。下列有关说法正确的是___________(填序号)。
。下列有关说法正确的是___________(填序号)。| A.HN3中含有5个σ键 |
| B.HN3中的三个氮原子均采用sp2杂化 |
| C.HN3、HNO2、H2O、N2H4都是极性分子 |
| D.肼(N2H4)的沸点高达113.5℃,说明肼分子间可形成氢键 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】已知铜的配合物A结构如图。请回答下列问题:

(1)写出基态Cu的外围电子排布式_____________________________________ 。
(2)配体氨基乙酸根(H2NCH2COOˉ)受热分解可产生CO2和N2,N2中σ键和π键数目之比是__________ ;N2O与CO2互为等电子体,则N2O的电子式为____________ 。
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醛分子中HCO的键角_____ (选填“大于”、“等于”或“小于”)120°;甲醛能与水形成氢键,请在如图中表示出来_____ 。

(4)立方氮化硼如图与金刚石结构相似,是超硬材料。立方氮化硼晶体内B-N键数与硼原子数之比为___________ ;

(5)Cu晶体的堆积方式如图所示,设Cu原子半径为a,晶体中Cu原子的配位数为________ ,晶体的空间利用率为______ 。(已知: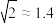 ,列式并计算出结果)
,列式并计算出结果)


(1)写出基态Cu的外围电子排布式
(2)配体氨基乙酸根(H2NCH2COOˉ)受热分解可产生CO2和N2,N2中σ键和π键数目之比是
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醛分子中HCO的键角

(4)立方氮化硼如图与金刚石结构相似,是超硬材料。立方氮化硼晶体内B-N键数与硼原子数之比为

(5)Cu晶体的堆积方式如图所示,设Cu原子半径为a,晶体中Cu原子的配位数为
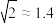 ,列式并计算出结果)
,列式并计算出结果)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】氧、硫、硒、碲等氧族元素在化合物中常表现出多种氧化态,含氧族元素的化合物在研究和生产中有许多重要用途。请回答以下问题:
(1)氧、硫、硒三元素的第一电离能由大到小的顺序为_______________________ (用元素符号回答)。
(2)基态Se原子的价层电子排布式为___________ ,其原子核外有______________ 种运动状态不同的电子。
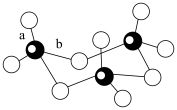
(3)气态SO3为单分子状态,其中S原子的杂化轨道类型为________ 。若SO3的三聚体(SO3)3的环状结构如图所示,则该结构中S原子的杂化轨道类型为____________________ 。
(4)氧族元素的气态氢化物中,H2S的稳定性强于H2Se,原因是________________________________ 。
(5)氧、硫分别与钙形成两种化合物的晶格能大小为 CaO__________ CaS (填“>”,“<”或“=”)。 (6)硫化锌在光导材料、涂料等行业中应用广泛,其晶体结构如图,则该晶体属于________ 晶体,化学式为__________ ,若晶体的密度为ρg·cm-3,则晶胞边长为____________ cm (阿伏伽德罗常数的值用NA表示)。
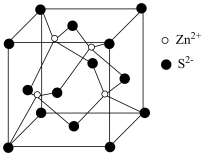
(1)氧、硫、硒三元素的第一电离能由大到小的顺序为
(2)基态Se原子的价层电子排布式为
(3)气态SO3为单分子状态,其中S原子的杂化轨道类型为

(4)氧族元素的气态氢化物中,H2S的稳定性强于H2Se,原因是
(5)氧、硫分别与钙形成两种化合物的晶格能大小为 CaO

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】聚氮化硫 和K3C60是两种不同类型的超导材料。回答下列问题:
和K3C60是两种不同类型的超导材料。回答下列问题:
(1)在基态K原子中,能最最低的空轨道的符号是______ 。
(2)S、N、K三种元素的第一电离能由大到小的顺序是______ 。
(3) 具有类似黄铜的金属光泽和导电性,其结构如下图:
具有类似黄铜的金属光泽和导电性,其结构如下图:

以S2Cl2为原料可制取 : S2Cl2→S4N4
: S2Cl2→S4N4 S2N2
S2N2

① 中N原子的杂化方式是
中N原子的杂化方式是________ 。 的晶体类型是
的晶体类型是_____ 。
②S2Cl2的结构式为__________ ;
(4)K3C60是由足球烯(C60)与金属钾反应生成的盐。
①在K3C60晶胞中,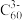 堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,K+填充在空隙中。晶胞中被K+占据的空隙百分比为
堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,K+填充在空隙中。晶胞中被K+占据的空隙百分比为_______ 。

②C60与金刚石互为同素异形体,比较两者的熔沸点并说明理由_____ 。
③C60的结构是一种多面体,如图所示。多面体的顶点数、面数和棱边数的关系遵循欧拉定律:顶点数+面数-棱边数=2。C60分子中所含的五边形和六边形的个数分别为______ 、_______ 。.
 和K3C60是两种不同类型的超导材料。回答下列问题:
和K3C60是两种不同类型的超导材料。回答下列问题:(1)在基态K原子中,能最最低的空轨道的符号是
(2)S、N、K三种元素的第一电离能由大到小的顺序是
(3)
 具有类似黄铜的金属光泽和导电性,其结构如下图:
具有类似黄铜的金属光泽和导电性,其结构如下图:
以S2Cl2为原料可制取
 : S2Cl2→S4N4
: S2Cl2→S4N4 S2N2
S2N2

①
 中N原子的杂化方式是
中N原子的杂化方式是 的晶体类型是
的晶体类型是②S2Cl2的结构式为
(4)K3C60是由足球烯(C60)与金属钾反应生成的盐。
①在K3C60晶胞中,
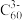 堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,K+填充在空隙中。晶胞中被K+占据的空隙百分比为
堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,K+填充在空隙中。晶胞中被K+占据的空隙百分比为
②C60与金刚石互为同素异形体,比较两者的熔沸点并说明理由
③C60的结构是一种多面体,如图所示。多面体的顶点数、面数和棱边数的关系遵循欧拉定律:顶点数+面数-棱边数=2。C60分子中所含的五边形和六边形的个数分别为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】元素周期表有多种形式。如图分别是两种不同形式元素周期表的局部区域。_______ (选填“金属性”或“非金属性”)越大。
②根据图甲中的信息判断,下列物质中含有离子键的是_______ 。
A.AlF3 B.AlCl3 C.Al2O3 D.Al2S3
(2)①图乙所示第二周期元素中,某一元素的该性质反常偏高,原因是_______ 。
②若将下列元素在图乙中排列,位置最低的元素是_______ 。
A.Na B.K C.Mg D.Ca
(3)图丙表示含义的是元素_______ 。
(4)①图中能正确表示基态N原子轨道表示式的是_______ 。_______ 。
A.能量最低原理 B.泡利原理 C.洪特规则
③基态N原子核外电子共有_______ 种不同的运动状态。
(5)同压下,部分氟化物的熔点见表:
①NaF、MgF2的熔点存在差异的原因是________ 。
②SiF4的熔点明显低于NaF、MgF2,原因是________ 。
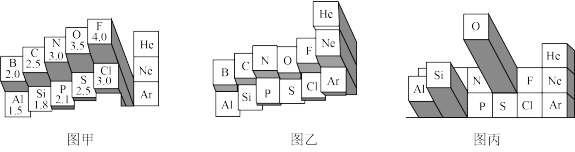
②根据图甲中的信息判断,下列物质中含有离子键的是
A.AlF3 B.AlCl3 C.Al2O3 D.Al2S3
(2)①图乙所示第二周期元素中,某一元素的该性质反常偏高,原因是
②若将下列元素在图乙中排列,位置最低的元素是
A.Na B.K C.Mg D.Ca
(3)图丙表示含义的是元素
| A.原子半径 | B.第一电离能 | C.电负性 | D.在地壳中的含量 |
(4)①图中能正确表示基态N原子轨道表示式的是
A.  B.
B.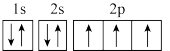
A.能量最低原理 B.泡利原理 C.洪特规则
③基态N原子核外电子共有
(5)同压下,部分氟化物的熔点见表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1266 | 1534 | 183 |
②SiF4的熔点明显低于NaF、MgF2,原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
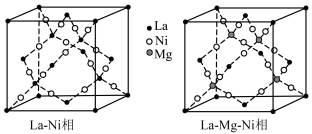
【推荐1】La-Ni相及La-Mg-Ni相均用作贮氢合金材料,以下为二者晶胞结构:
(1)金属镧La位于周期表的____________ 区; 的价电子排布图为
的价电子排布图为____________ ; 与同周期且相邻的元素第一电离能从大到小的顺序为
与同周期且相邻的元素第一电离能从大到小的顺序为____________ .
(2)La-Mg-Ni相的化学式为____________ ,其晶体中与 等距且最近的
等距且最近的 有
有____________ 个;La-Ni相中原子空间利用率为____________ (已知: 原子半径分别为
原子半径分别为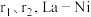 相晶胞参数为a)。
相晶胞参数为a)。
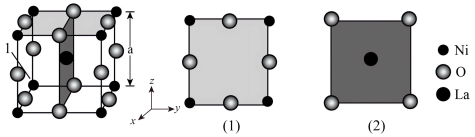
(3)镍酸镧电催化剂立方晶胞如图所示,晶胞参数为a,图(1)和图(2)是晶胞的不同切面。 和
和 的最短距离为
的最短距离为____________ .
②若原子1的分数坐标为 ,则
,则 的分数坐标为
的分数坐标为____________ 。
(1)金属镧La位于周期表的
 的价电子排布图为
的价电子排布图为 与同周期且相邻的元素第一电离能从大到小的顺序为
与同周期且相邻的元素第一电离能从大到小的顺序为(2)La-Mg-Ni相的化学式为
 等距且最近的
等距且最近的 有
有 原子半径分别为
原子半径分别为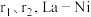 相晶胞参数为a)。
相晶胞参数为a)。(3)镍酸镧电催化剂立方晶胞如图所示,晶胞参数为a,图(1)和图(2)是晶胞的不同切面。
 和
和 的最短距离为
的最短距离为②若原子1的分数坐标为
 ,则
,则 的分数坐标为
的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】金属镍及其化合物在合成材料以及催化剂等方面应用广泛。请回答下列问题:
(1)基态Ni原子的原子结构示意图为_____ 。
(2)NiO、FeO晶体类型与晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为_____ ;又知Ni2+、Fe2+的离子半径分别为69pm、78pm,则NiO熔点_____ FeO(填“>”、“<”、“=”)。
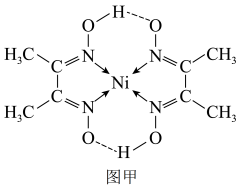
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中Ni2+的配位数为_____ ;元素H、C、N、O、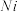 电负性由大到小的顺序为
电负性由大到小的顺序为____ 。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图及晶胞参数如图乙所示。该晶体的化学式为_____ ;晶体密度为_____ g•cm-3(列出含a、b、NA计算表达式,NA表示阿伏加德罗常数的值)。

(1)基态Ni原子的原子结构示意图为
(2)NiO、FeO晶体类型与晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中Ni2+的配位数为
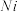 电负性由大到小的顺序为
电负性由大到小的顺序为
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图及晶胞参数如图乙所示。该晶体的化学式为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
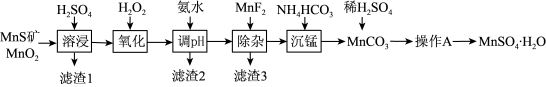
【推荐3】硫酸锰(MnSO4•H2O)是一种粉色晶体,易溶于水,不溶于乙醇,是重要的微量元素肥料之一,工业上由天然二氧化锰与硫化锰矿(还含Fe、Al、Mg、Si等元素的氧化物)制备硫酸锰的工艺如图所示。回答下列问题:
②相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
(1)“溶浸”前需将矿石研成粉末,其目的是_______ 。“滤渣1”中含有S和_______ ;“溶浸”时两种含锰化合物与H2SO4反应的化学方程式为_______ 。
(2)“氧化”时添加适量的MnO2的作用是_______ (用离子方程式表示),若省略“氧化”步骤,造成的后果是_______ 。
(3)加入MnF2的目的是_______ 。
(4)滤液经过_______ (写操作A的名称),可得到粉红色MnSO4•H2O晶体。
(5)构想某锂电池的负极材料晶体是锂原子嵌入石墨烯层间,晶体结构如图。_______ 。
②如图晶体的化学式为_______ ;该晶体中最近的两个碳原子核间距离为142pm,石墨烯层间距离为335pm,则该晶体的密度为_______ g•cm-3(用NA表示阿伏加德罗常数,列式即可)。
②相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(1)“溶浸”前需将矿石研成粉末,其目的是
(2)“氧化”时添加适量的MnO2的作用是
(3)加入MnF2的目的是
(4)滤液经过
(5)构想某锂电池的负极材料晶体是锂原子嵌入石墨烯层间,晶体结构如图。
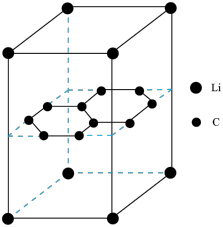
②如图晶体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】钴广泛应用于电池、合金等领域。以含钴废料(主要含 和
和 ,还含有
,还含有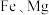 等元素以及
等元素以及 、碳、有机物)为原料制备钴的流程如下:
、碳、有机物)为原料制备钴的流程如下: 难溶于水。
难溶于水。
② (焦亚硫酸钠)常作食品抗氧化剂。
(焦亚硫酸钠)常作食品抗氧化剂。
③常温下,部分氢氧化物沉淀的 如表所示。
如表所示。
④氧化性: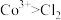 。
。
回答下列问题:
(1)“浸取”时硫酸不宜用浓盐酸代替,其原因是___________ (用离子方程式表示)。
(2)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图1所示,氧化率与 的关系如图2所示(不考虑
的关系如图2所示(不考虑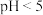 的情况)。
的情况)。___________ 。在此条件下,实际消耗的双氧水远大于理论用量,可能的原因是___________ 。
(3)有人认为“除镁”可以通过调节 代替加入
代替加入 ,请你评价:
,请你评价:___________ (判断是否可行,简述理由)。
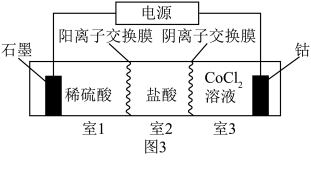
(4)工业上也可利用图3装置实现制备 。
。___________ 。生成 时,室1中溶液理论上减少
时,室1中溶液理论上减少___________ g。
②相较于直接电解 溶液,图3中“三室两膜”装置突出优点是
溶液,图3中“三室两膜”装置突出优点是___________ 。(从绿色化学角度分析)
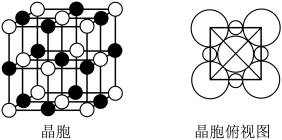
(5)钴的一种氧化物的晶胞如图所示,已知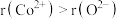 。钴离子的配位数为
。钴离子的配位数为___________ ,晶胞中原子空间利用率为___________ 。[用含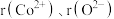 和π的代数式表示,已知:晶胞中原子空间利用率
和π的代数式表示,已知:晶胞中原子空间利用率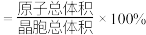 ]
]
 和
和 ,还含有
,还含有 等元素以及
等元素以及 、碳、有机物)为原料制备钴的流程如下:
、碳、有机物)为原料制备钴的流程如下: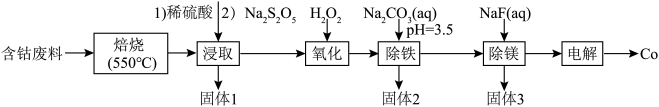
 难溶于水。
难溶于水。②
 (焦亚硫酸钠)常作食品抗氧化剂。
(焦亚硫酸钠)常作食品抗氧化剂。③常温下,部分氢氧化物沉淀的
 如表所示。
如表所示。 |  |  |  |  | |
开始沉淀 | 0.3 | 2.7 | 7.6 | 7.2 | 9.6 |
完全沉淀 | 1.2 | 3.2 | 9.6 | 9.2 | 11.1 |
 。
。回答下列问题:
(1)“浸取”时硫酸不宜用浓盐酸代替,其原因是
(2)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图1所示,氧化率与
 的关系如图2所示(不考虑
的关系如图2所示(不考虑 的情况)。
的情况)。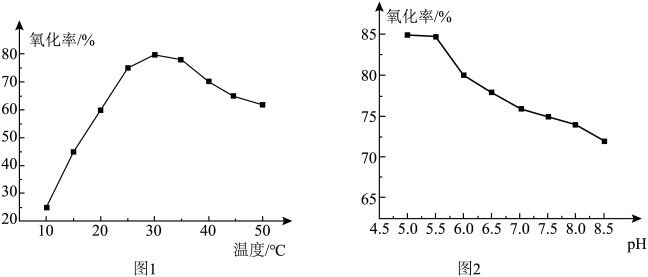
(3)有人认为“除镁”可以通过调节
 代替加入
代替加入 ,请你评价:
,请你评价:(4)工业上也可利用图3装置实现制备
 。
。
 时,室1中溶液理论上减少
时,室1中溶液理论上减少②相较于直接电解
 溶液,图3中“三室两膜”装置突出优点是
溶液,图3中“三室两膜”装置突出优点是(5)钴的一种氧化物的晶胞如图所示,已知
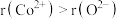 。钴离子的配位数为
。钴离子的配位数为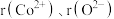 和π的代数式表示,已知:晶胞中原子空间利用率
和π的代数式表示,已知:晶胞中原子空间利用率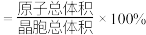 ]
]
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】新型半导体材料如碳化硅(SiC)、氮化镓(GaN)等在国防技术、航空航天及5G技术等领域扮演着重要的角色。回答下列问题:
(1)基态Si原子中,核外电子占据的最高能层的符号为___________ ,占据最高能级的电子的电子云轮廓图形状为___________ ;基态Ga原子的核外电子排布为[Ar]3d104s24p1,其转化为下列激发态时,吸收能量最少的是___________ (填选项字母)。
A.[Ar] B.[Ar]
B.[Ar]
C.[Ar] D.[Ar]
D.[Ar]
(2)C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子结构分析,其原因为___________ 。
(3)GaCl3的熔点为77.9℃,GaF3的熔点为1000℃,试分析GaCl3熔点低于GaF3的原因为___________ ;气态GaCl3常以二聚体形式存在,二聚体中各原子均满足8e-结构,据此写出二聚体的结构式为___________ 。
(4)B和Mg形成的化合物刷新了金属化合物超导温度的最高记录。该化合物的晶体结构单元如图所示,其中Mg原子间形成正六棱柱,6个B原子分别位于六个三棱柱体心。则该化合物的化学式可表示为___________ ;相邻B原子与Mg原子间的最短距离为___________ nm(用含x、y的代数式表示)。

(1)基态Si原子中,核外电子占据的最高能层的符号为
A.[Ar]
 B.[Ar]
B.[Ar]
C.[Ar]
 D.[Ar]
D.[Ar]
(2)C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子结构分析,其原因为
(3)GaCl3的熔点为77.9℃,GaF3的熔点为1000℃,试分析GaCl3熔点低于GaF3的原因为
(4)B和Mg形成的化合物刷新了金属化合物超导温度的最高记录。该化合物的晶体结构单元如图所示,其中Mg原子间形成正六棱柱,6个B原子分别位于六个三棱柱体心。则该化合物的化学式可表示为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】含钴化合物在机械制造、磁性材料等领域具有广泛的应用,请回答下列问题:
(1)基态Co3+的价电子排布图为____ 。
(2)钴的配合物[Co(NH3)5Br](NO3)2
①第一电离能N_____ O(填“大于”、“小于”或“不能确定”);两种配位原子的杂化轨道类型均为____ ;
②钴离子周围配位键数目(配位数)是___ ;N03-的空间构型为____ ;
③已知Br的含氧酸酸性由强到弱的顺序为HBrO4>HBrO3>HBrO2>HBrO,其原因是____ 。
(3)某钴氧化物晶体具有CoO2的层状结构如下图所示(小球表示Co,大球表示O)。下列用粗线面出的结构单元不能描述CoO2)的化学组成的是_____

(4)Co的另一种氧化物的晶胞如图,已知钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,钴原子填在氧原子的___ 填“正八面体”、“正四面体”或“立方体”)空隙;钴原子与跟它次近邻的氧原子之间的距离为____ ;在该钴的氧化物晶体中原子的空间利用率为____ (均用含a、b的计算表达式表示)。

(1)基态Co3+的价电子排布图为
(2)钴的配合物[Co(NH3)5Br](NO3)2
①第一电离能N
②钴离子周围配位键数目(配位数)是
③已知Br的含氧酸酸性由强到弱的顺序为HBrO4>HBrO3>HBrO2>HBrO,其原因是
(3)某钴氧化物晶体具有CoO2的层状结构如下图所示(小球表示Co,大球表示O)。下列用粗线面出的结构单元不能描述CoO2)的化学组成的是

(4)Co的另一种氧化物的晶胞如图,已知钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,钴原子填在氧原子的

您最近一年使用:0次



