CO2与CH4的催化重整有利于减少空气中的CO2,实现碳中和。
已知:①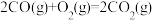 △H1=akJ·mol-1
△H1=akJ·mol-1
② △H2=bkJ·mol-1
△H2=bkJ·mol-1
③ △H3=ckJ·mol-1
△H3=ckJ·mol-1
则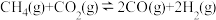 的△H4为
的△H4为
已知:①
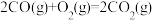 △H1=akJ·mol-1
△H1=akJ·mol-1②
 △H2=bkJ·mol-1
△H2=bkJ·mol-1③
 △H3=ckJ·mol-1
△H3=ckJ·mol-1则
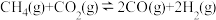 的△H4为
的△H4为| A.(-a-b+c)kJ·mol-1 | B.(a+b-c)kJ·mol-1 |
| C.(-a+b-c)kJ·mol-1 | D.(a-b-c)kJ·mol-1 |
更新时间:2023-08-31 08:04:23
|
相似题推荐
【推荐1】依据下面图示关系,下列说法不正确的是
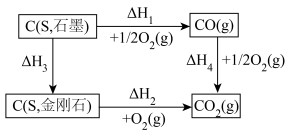
A.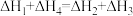 |
B.若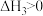 ,则石墨更稳定 ,则石墨更稳定 |
| C.一个化学反应的焓变,只与反应的始态和终态有关,与反应途径无关 |
D.若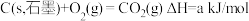 , , ,则 ,则 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知:C(金刚石,s)+O2(g)=CO2(g) △H1,C(石墨,s)+O2(g)=CO2(g) △H2,
C(石墨,s)=C(金刚石,s) △H3=+1.9 kJ∙mol−1,下列说法正确的是
C(石墨,s)=C(金刚石,s) △H3=+1.9 kJ∙mol−1,下列说法正确的是
| A.石墨转化成金刚石的反应是放热反应 |
| B.石墨比金刚石稳定 |
C.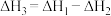 |
| D.相同质量的石墨与金刚石完全燃烧后,前者的热效应高 |
您最近一年使用:0次
【推荐3】下列说法或表示方法错误 的是
| A.盖斯定律实质上是能量守恒定律的体现 |
| B.一定条件下,0.5molN2和1.5molH2充分反应后放出35.5 kJ热量,则N2(g)+3H2(g)⇌2NH3(g) ΔH=-71kJ/mol |
| C.由于反应情况不同,反应热可分为燃烧热,中和热等 |
| D.在稀溶液中:H+(aq)+OH-(aq)=H2O(l);∆H =-57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
您最近一年使用:0次
【推荐1】Li2O和Na2O的能量关系如图所示(M=Li、Na):
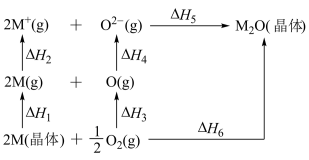
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是

已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
| A.对于Li2O和Na2O,ΔH3均大于0,而ΔH6均小于0 |
| B.Li2O对应的ΔH3+ΔH4等于Na2O对应的ΔH3+ΔH4 |
| C.ΔH5(Li2O)<ΔH5(Na2O) |
| D.对于Na2O,ΔH6<ΔH2+ΔH4+ΔH5 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A | 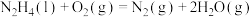 ΔH=-534 kJ·mol-1 ΔH=-534 kJ·mol-1 | N2H4的燃烧热为534 kJ·mol-1 |
| B |  ΔH=-57.3 kJ·mol-1 ΔH=-57.3 kJ·mol-1 | 含40 g NaOH的稀溶液与浓硫酸完全中和,放出的热量等于57.3kJ |
| C | C(s)+ O2(g)=CO(g) ΔH= - 110.5 kJ·mol-1 O2(g)=CO(g) ΔH= - 110.5 kJ·mol-1CO(g)+  O2(g)=CO2(g) ΔH=-283 kJ·mol-1 O2(g)=CO2(g) ΔH=-283 kJ·mol-1 | 2mol C(s) 完全燃烧放出787kJ热量 |
| D | C(石墨,s)= C(金刚石,s) ΔH= +1.5 kJ·mol-1 | 金刚石比石墨稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】通过以下反应均可获取H2。
①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=+131.3kJ·mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+206.1kJ·mol-1
③CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3
下列说法正确的是
①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=+131.3kJ·mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+206.1kJ·mol-1
③CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3
下列说法正确的是
| A.①中反应物的总能量大于生成物的总能量 |
| B.②中使用适当催化剂,可以使ΔH2减小 |
| C.由①、②计算反应CH4(g)=C(s)+2H2(g)的ΔH=-74.8kJ·mol-1 |
| D.若知反应C(s)+CO2(g)=2CO(g)的ΔH,结合ΔH1可计算出ΔH3 |
您最近一年使用:0次



